НЕСОВЕРШЕНСТВА В СТРОЕНИИ МЕТАЛЛОВ
 14 марта, 2016
14 марта, 2016  Oleg Maloletnikov
Oleg Maloletnikov Идеальное расположение атомов в кристаллах, строго соответствующее типу кристаллической решетки, в реальных условиях почти не встречается. В любом реальном кристалле металла или сплава имеются различные несовершенства, т. е. отклонения от абсолютно правильного размещения атомов. Такие несовершенства существенно сказываются на всех свойствах металлов, и прежде всего, на их прочности, пластичности, упругости, коррозионной стойкости и т. п.
 Нарушения правильной кристаллической структуры практически неизбежны уже при образовании монокристаллов. При объединении последних в блоки и образовании поликристаллов создаются, кроме того, дополнительные виды несовершенств. Ниже рассматриваются наиболее важные примеры несовершенств N монокристаллов и поликристаллических —— блоков.
Нарушения правильной кристаллической структуры практически неизбежны уже при образовании монокристаллов. При объединении последних в блоки и образовании поликристаллов создаются, кроме того, дополнительные виды несовершенств. Ниже рассматриваются наиболее важные примеры несовершенств N монокристаллов и поликристаллических —— блоков.
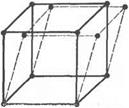
Упругие искажения. Под действием любой силы, независимо от ее природы, атомы кристалла смещаются из своих первоначальных положений. В результате ЭТОГО кристаллическая структура Рнс. 4. Искажение кристал - искажается (рис. 4). лической решетки поддейст-
Упругая деформация металла, вы - вием сил сдвига - званная действием приложенной внешней силы, является результатом суммирования незначительных по абсолютной величине искажений размеров отдельных ячеек кристаллической решетки. Поскольку первоначальное правильное расположение атомов соответствует минимальному значению свободной энергии, а поэтому устойчиво, любое отклонение из этого положения требует дополнительной затраты работы. Работа, израсходованная на упругое деформирование металла, сохраняется им в форме потенциальной энергии атомов до тех пор, пока не сняты усилия. При соответствующих условиях эта энергия может
высвобождаться в виде механической работы, теплоты, химической энергии, электричества и т. п.
Например, сжатая пружина, распрямляясь, совершает механическую работу, равную по величине потенциальной энергии, накопленной атомами в процессе ее сжатия. Известно также, что скрученная напряженная пружина быстрее растворяется в кислоте, чем ненапряженная. Практикой установлено, что сварные соединения, имеющие высокие собственные напряжения, больше подвержены коррозии, особенно на участках концентрации напряжений. В двух последних примерах потенциальная энергия атомов, связанная с искажением кристаллической структуры, проявляется в форме
 тепловой и химической энергии.
тепловой и химической энергии.
Несовершенства структуры вблизи поверхности металла. Атомы на поверхности металла находятся в особых условиях по сравнению с расположенными в глубине. Внутри кристалла каждый атом взаимосвязан с окружающими его соседними атомами. Действующие на него силы симметричны. Поверхностные атомы взаимодействуют с соседними атомами свободной поверхности, а также с атомами, расположенными внутри кристалла. Силы, действующие на поверхностный слой со стороны окружающей среды, обычно незначительны, а в условиях высокого вакуума — близки к нулю.
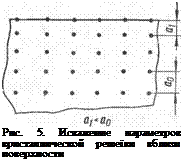
Под действием больших сил притяжения со стороны атомов, расположенных внутри кристалла, атомы слоев, прилегающих к поверхности, сдвинутся из своих нормальных положений (рис. 5). Структура металла в слоях, прилегающих к свободной поверхности, будет искажена. Всякое местное искажение кристаллической решетки связано с приростом энергии, вследствие чего любая свободная поверхность кристалла обладает некоторым запасом поверхностной энергии. Величина последней может быть оценена работой, необходимой для образования единицы новой поверхности, например, при разрушении твердого тела. Поверхностная энергия играет существенную роль в некоторых видах сварки, при адсорбции и дру - 'гих процессах.
Вакантные узлы кристаллической решетки. В результате непрерывных тепловых колебаний атомов некоторые узлы кристаллической решетки могут оказаться временно незанятыми (вакантными). Явление это в определенных условиях имеет массовый характер и может быть объяснено так.
Постоянство температуры всех участков кристалла характеризует только среднюю кинетическую энергию атома. В то же время каждый из них обладает собственным запасом энергии, вообще говоря, не совпадающим со средним ее значением для всего объема.
В результате теплового движения и взаимодействия атомов энергия между ними постоянно перераспределяется Одни атомы теряют кинетическую энергию, и скорость их движения уменьшается, другие приобретают очень высокие скорости движения, преодолевают силы связей с соседними атомами, покидают свое место и перемещаются в кристаллической решетке. Возможно также, что сместившийся из своего положения атом выйдет на поверхность кристалла и вырвется в окружающую среду.
Наличие вакантного узла создает несовершенство кристаллической решетки, изменяет силы взаимосвязей. Вакантное место в узле может быть замещено соседним атомом, за счет чего в свою очередь образуется вакансия.
С повышением температуры вероятность образования вакантных мест в решетке резко возрастает. Возникает цепной процесс перемещения вакансий. Есть области, где вакансии образуются особенно интенсивно. Это поверхностные слои, границы зерен, зоны местных дефектов и т. д. Вакансии оказывают существенное влияние на свойства металлов, в особенности на процессы диффузии (см. § 36).
Удаление' атомов в окружающую среду лежит в основе процесса сублимации и объясняет наличие парциального давления паров металла над кристаллом даже при нормальных температурах.
Искажение кристаллической структуры в сплавах При образовании твердого раствора атомы растворяемого элемента располагаются в решетке растворителя. Они могут замещать атомы последнего в узлах решетки либо находиться в пространстве между узлами. В первом случае получается раствор типа замещения, во втором — типа внедрения. Вид образующегося раствора зависит от соотношения размеров атомных диаметров.
Так как атомы взаимодействующих веществ различны, процесс растворения всегда приводит к искажению формы и параметров первоначальной решетки растворителя. Это искажение тем заметнее, чем сильнее отличаются атомы друг от друга. Естественно, что изменение кристаллической решетки существенно сказывается и на свойствах металла. При разработке новых сплавов в технике широко используют это явление и получают конструкционные материалы, коренным образом отличающиеся по своим свойствам от исходных.
Растворы типа замещения дают те металлы, атомные диаметры которых мало отличаются друг от друга,— не более чем на 15%. Креме того, металлы должны быть близко расположенными в ряду напряжений и иметь сходную кристаллическую структуру. Примерами пар металлов, образующих растворы типа замещения, могут служить Fe—Мп, Au—Ag, Fe—Ni и др. Указанные пары металлов обладают сходными характеристиками межатомных связей и примерно одинаковыми размерами атомов. Большинство пар металлов, удовлетворяющих этим условиям, отличаются хорошей взаимной растворимостью.
Другим типом твердых растворов являются растворы внедрения, где атомы растворенного элемента располагаются в пустотах между атомами растворителя. Приняв сферическую форму атомов, теоретически можно показать, что диаметр растворенного атома должен составлять не более 0,59 диаметра атома растворителя. В обычных металлах мы не встречаем столь большой разницы в диаметрах, поэтому растворы внедрения образуют лишь металлоиды с наименьшим диаметром атома (С, Н, N, В) и некоторые металлы переходных групп. Большая часть остальных металлов дает с указанными металлоидами соединения ионного типа (карбиды, гидриды, бориды и нитриды). Поскольку растворенные атомы имеют малые размеры, то перемещаются они в сплаве очень быстро, не дожидаясь образования вакансий в пустотах между атомами растворителя.
Твердый раствор внедрения обычно имеет структуру растворителя, в значительной мере искаженную влиянием внедренных атомов. Если при образовании сплава типа внедрения соблюдается постоянное соотношение числа атомов растворяемого элемента и растворителя, то принято считать, что мы имеем дело с соединением типа внедрения. К этому типу относятся, например, карбиды (Fe;(C) и нитриды (Fe„N) железа. Вследствие больших искажений кристаллической решетки такие соединения мало пластичны и очень тверды.
Несовершенства, возникающие в процессе кристаллизации металла. Процесс кристаллизации металла можно условно разбить на несколько стадий: образование зародышей кристалла, развитие
отдельных монокристаллов, группировка и объединение последних в поликристаллические блоки.
В начальный период кристаллизации монокристаллы развиваются из зародышей независимо друг от друга. Скорость роста, размеры и расположение их в пространстве различны и зависят от характера теплоотвода, количества жидкой фазы и т. п. В процессе роста отдельно развивающиеся кристаллы сближаются таким образом, что последние атомы жидкой прослойки становятся для них общими. Поскольку кристаллы мешают развиваться друг другу, их форма приобретает случайные очертания, не соответствующие их кристаллографической огранке, а металл представляет собой сросток отдельных зерен — кристаллитов.
На' границе соприкосновения нескольких отдельных кристаллитов никогда не наблюдается правильное расположение атомов, соответствующее параметрам кристаллической решетки. Прежде всего это объясняется тем, что пространственная ориентация кристаллов различна. Атомы последнего слоя жидкой прослойки между соседними зернами занимают какое-то промежуточное положение по отношению к узлам обоих зерен (рис. 6). В результате этого вдоль всей границы их соприкосновения возникают несовершенства структуры, которые распространяются в глубь зерен на несколько атомных слоев. Эти пограничные слои атомов обладают повышенным
запасом энергии и ведут себя несколько иначе, чем точно такие же атомы, расположенные в глубине зерен. Кроме того, при затвердевании последних порций металла примеси и загрязнения оттесняются к границам зерен, где содержание их становится выше, чем внутри зерна.
 Наличие несовершенств и повышенного запаса энергии у атомов вблизи граней кристаллитов определяет химические, физические и механические свойства металлов.
Наличие несовершенств и повышенного запаса энергии у атомов вблизи граней кристаллитов определяет химические, физические и механические свойства металлов.
 |
Например, при погружении в коррозионную среду границы зерен даже самых чистых металлов разрушаются быстрее, чем центральные части кристаллитов. Это явление служит одной из причин межкристаллитной коррозии. Выявление границ зерен при металлографических исследованиях также основано на разной травимости центральной части зерен и их границ. Повышенное значение свободной энергии пограничных атомов приводит к тому, что плавление металла всегда начинается у границ зерен. Важнб также отметить особую склонность атомов с повышенной энергией к диффузии, за счет чего можно объяснить
более интенсивное проникновение в металл чужеродных атомов по межкристаллитным границам.
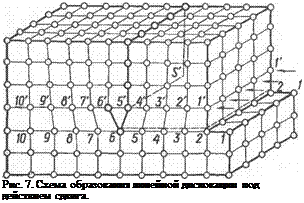
Иногда несовершенства в металлах занимают очень малый объем и имеют точечный характер, но могут располагаться и по определенной линии или плоскости и^ наконец, равномерно распределяться по всему объему кристалла. Примером линейных несовершенств являются дислокации (рис. 7). Если под действием сил
(или различных других причин) один слой атомов сдвигается по отношению к другому, то перемещение рядов 1,2,3,... происходит неодновременно. Сначала, и на большую величину, смещаются атомы первого ряда (считая по направлению действующей силы), затем — атомы следующих рядов 2, 3, 4, ... , причем величина смещения по мере удаления от места приложения усилий снижается до тех пор, пока не исчезнет совсем.
Между атомами нижнего ряда 6 и верхних рядов 5' и 6' образуется неестественная схема связей, при которой с каждым атомом нижнего ряда 6 связаны два атома верхних рядов 5'и б'.Такое несовершенство структуры будет наблюдаться вдоль всего ряда 6—6; оно носит линейный характер и называется линейной дислокацией. Количество дислокаций в каждом реальном кристалле велико — около 10® на 1 см2. Дислокации возникают уже в процессе первичной кристаллизации, и их следует рассматривать как неизбежные дефекты строения кристаллических тел.
Следует учитывать, что искажения решетки и повышенный запас энергии атомов будут во всех рядах, расположенных вблизи плоскости сдвига, хотя под названием «дислокация» обычно подразумевают только несовершенства по линии 6—6'.
В настоящее время установлено, что дислокации — это наиболее важный вид встречающихся в металле несовершенств. Некоторые свойства дислокаций, а также их влияние на показатели механических свойств металлов описаны в гл. II при рассмотрении особенностей пластической деформации металлов.

 Опубликовано в
Опубликовано в