Количественный анализ стирола
 21 декабря, 2012
21 декабря, 2012  admin
admin Определение содержания стирола реактивом Кауфмана. В две конические колбы с пришлифованными пробками емкостью по 250 мл отвешивают на аналитических весах по 0,2 г стирола, приливают из бюретки по 30—35 мл реактива Кауфмана, взбалтывают и оставляют стоять в течение 5—10 мин. После этого в каждую колбу из мерного цилиндра прибавляют по 10—15 мл 10%-ного раствора иодистого калия, разбавляют равным количеством воды, перемешивают и через 10—15 мин оттитровывают выделившийся иод 0,1 н. гипосульфитом, прибавив в качестве индикатора несколько капель раствора крахмала. Параллельно ставят контрольный опыт.
Содержание стирола в процентах (х) вычисляют по формуле
_(д — 6)ft0,0052-100 X— ,
S
Тде а — объем 0,1 н. гипосульфита, израсходованного на титрование контрольной пробы, мл; b — объем 0,1 н. гипосульфита, израсходованно-' то на титрование пробы с навеской, мл; K — поправка к титру 0,1 н. гипосульфита; G — навеска стирола, г; 0,0052 — количество стирола, соответствующее 1 мл 0,1 н. гипосульфита,.г.
Приготовление реактива Кауфмана. Берут 13—14 вес. ч. бромистого калия, предварительно высушенного при 130° С, и растворяют в 100 вес. ч. перегнанного метилового спирта (выполнять в присутствии руководителя). Раствор фильтруют, затем к нему прибавляют 5,1 мл брома на 1 л раствора и оставляют стоять 12—15 дней, после чего устанавливают его титр. Титр устанавливают следующим образом: к 20 мл бромного раствора прибавляют несколько капель концентрированной соляной кислоты и 20 мл 10%-ного иодистого калия. Смесь разбавляют равным количеством воды и оттитровывают выделившийся иод 0,1 н. гипосульфитом. После того как титр реактива Кауфмана практически перестанет изменяться, его используют для анализа.
Определение содержания стирола по методу Вийса. При определеНии стирола по методу Вийса метиловый спирт заменяется четыреххло - ристым углеродом. В основе метода лежит реакция двойных связей с Хлоридом по схеме
С6Н5СН=СН2 + IC1 ->■ СбН5СН1-СН2С1 IC1+KI=I2 + KC1
I2+2Na2S203=2NaI-f Na2S406
Навеску стирола около 1 г (или около 10 г полистирола, если необходимо определить в нем свободный мономер), взвешенную с точностью до 0,0002 г (во втором случае 0,01 г), вносят в мерную колбу, приливают 150—200 мл ССЦ и при помешивании растворяют мономер (или полимер). Затем добавляют ССЦ до метки и взбалтывают. В две конические колбы наливают по 10 мл (во втором случае 50 мл) приготовленного раствора и по 10 мл раствора Вийса. Колбы закрывают пробкой, смоченной раствором KI, и помещают в темное место на 15 мин, затем добавляют 15 мл раствора KI и 100 мл дистиллированной воды. Содержимое колбы тщательно перемешивают и титруют раствором Na2S203, добавляя к концу титрования раствор крахмала.
В аналогичных условиях титруют контрольную пробу.
Содержание стирола (в %) вычисляют по формуле
(а — 6) ft-0,0052-100-250
X— ~ 1
50g
Где а и 6 —количество 0,1 н. раствора Na2S203, пошедшего на титрование контрольной и анализируемой проб, мл; k — поправка к титру 0,1 н. раствора Na2S203; 0,0052 — количество стирола, соответствующее 1 мл точно 0,1 н. раствора Na2S203, г; g— навеска полимера, г.
Приготовление раствора Вийса. В мерной колбе емкостью 1 л растворяют 8 г трех- хлористого или однохлористого иода и 9 г металлического иода в 300 мл СС14 и 700 мл - ледяной уксусной кислоты. Раствор фильтруют в склянку из темного стекла и хранят - в темном месте. Реактивом можно пользоваться через три дня после его приготовления. Все вещества для приготовления реактива должны быть химически чистые.
Определение стирола в дисперсионной среде методом некомпенсационного потенциометрического титрования. В стакан для титрования,, помещенный на магнитную мешалку, вливают 50 мл водно-спиртовой смеси и из капельницы по каплям вносят 1—2 г дисперсионной жидкости, взвешенной с точностью до 0,001 г, после чего титруют 0,1 н. раствором брома в ледяной уксусной кислоте. В аналогичных условиях титруют контрольную пробу (описание метода см. [5]).
|
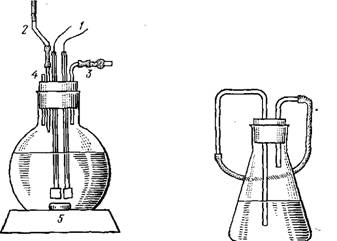
Рис. 14. Колба для титрования воды реактивом Фишера: 1 — платиновые электроды; 2 — микробю - Ретка; 3 — хлоркальциевая трубка; 4 — Пробка; 5 —магнитная мешалка |
|
Рис. 15. Колба для отбора проб |
|
В колбу для титрования (рис. 14), снабженную магнитной мешал - кой, наливают абсолютированный метанол или смесь метанола с мети - ленхлоридом (1:1 по объему) в количестве, необходимом для погружения платиновых электродов. Реактивом Фишера оттитровывают воду, содержащуюся в растворителе, и воду, адсорбированную стенками сосуда и электродами. Сначала реактив приливают быстро (1 каплю в секунду), при этом стрелка микроамперметра очень слабо отклоняется от нулевого положения, при дальнейшем добавлении реактива стрелка амперметра начинает сильно колебаться. В это время подачу реактива производят медленно (1 каплю в 6—7 с). Титрование продолжают до тех пор, пока стрелка амперметра не установится на определенном деле- |
Определение воды. Определение воды в мономере можно осуществить с помощью реактива Фишера на ручной или автоматической электрометрической установке.
Нни шкалы и останется в таком положении в течение 1 мин. Количество реактива, пошедшее на титрование, не фиксируют.
Для определения воды в мономере в колбу с оттитрованным растворителем вносят через отверстие в пробке 4 (рис. 14) навеску анализируемого вещества, которую передавливают сухим инертным газом из колбы (рис. 15) и оттитровывают воду реактивом Фишера по описанному выше методу.
Вычисление водного эквивалента реактива К (г/мл) и содержание воды л; (вес. %) в анализируемой пробе производят по формулам:
„ Ь а/<100
К——; ----------------------------------- .
А 6[
Здесь Ь и Ь; — навески воды (в контрольном опыте) и анализируемой пробы, г; a, ai — количество реактива, затраченное на титрование навески воды и анализируемой пробы.
Приготовление реактива Фишера. В склянку из темного стекла. вносят 85 г металлического иода (предварительно измельченного и высушенного в эксикаторе иад СаСЬ в течение 48 ч), 265 мл абсолютированного пиридина. Склянку закрывают пробкой, оставляют при комнатной температуре и периодически взбалтывают до полного растворения иода. Затем в раствор вносят 665 мл абсолютированного метанола, закрывают пробкой и взбалтывают.
После перемешивания пробку из склянки вынимают и склянку быстро закрывают пробкой с двумя стеклянными трубками (предварительно тщательно высушенными), соединенными предварительно высушенным резиновым шлангом (рис. 15).
Склянку с содержимым помещают в холодную воду со льдом и реактив при охлаждении насыщают SO2, сняв при этом резиновый шланг с наружных концов стеклянных трубок. S02 вводят в склянку через длинную трубку до тех пор, пока вес склянки с содержимым не увеличится на 65—75%.
Определение чистоты стирола криоскопическим методом. Метод основан на зависимости температуры замерзания стирола от содержания в нем примесей и прежде всего воды и этилбензола.
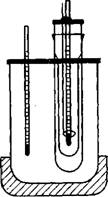
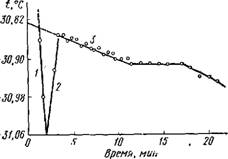
Смесь из ацетона и четыреххлористого углерода в соотношении 1 : 1 помещают в сосуд Дьюара и охлаждают сухим льдом до —42° С. Стирол (10 мл) заливают в чистую и сухую пробирку, помещенную в охлаждающую смесь (рис. 16). В пробирку опускают термометр и следят за понижением температуры. Когда температура понизится до —30° С, начинают перемешивание и фиксируют понижение температуры с точностью до 0,01° С через каждые 30 с. При охлаждении температура падает до минимума, затем быстро поднимается и снова начинает опускаться. Фиксируют несколько точек при падении температуры. В координатах время — температура строят кривую зависимости температуры от времени охлаждения. Температуру замерзания стирола находят по кривым, приведенным на рис. 17. Для этого продолжают кривую охлаждения твердого вещества до пересечения с кривой охлаждения жидкости. Точка пересечения является температурой замерзания.
Содержание стирола х (%) вычисляют по формуле (5) .
Х= 100 + 2,47[ -1 + (- 30,63)],
Где T — температура замерзания анализируемого стирола; —30,63 — температура замерзания 100%-ного стирола; 2,47 — количество примеси этилбензола, понижающее температуру замерзания стирола на 1°, %.
Определение дивинилбензола в стироле спектрофотометрическим методом. Метод основан на различном поглощении света дивиншибензолом и стиролом в ультрафиолетовой области спектра при А,=313 нм [8] [5].
|
Рис. 16. Прибор Для определения температуры замерзания стирола |
Для построения градуировочных графиков приготовляют ряд эталонных растворов стирола с содержанием дивинилбензола 0,001; 0,003; 0,004; 0,005; 0,006; 0,008; 0,01%.
|
Рис. 17. Зависимость температуры замерзания стирола от времени охлаждения: 1 — кривая охлаждения жидкости; 2 — кривая переохлаждения жидкости; 3 — кривая охлаждения твердого вещества |
Оптическая плотность чистого стирола D0=0,215 при Я=313 мкм для толщины слоя 5 мм. Измерения D О производят по отношению к одному кварцевому окошку.
Значения оптической плотности D для дивинилбензола в зависимости от его содержания в эталонных растворах [5] приведены ниже:
Содержание дивинилбензола в стироле, % , .... , 0,001 0,003 0,004 0,005 0,006 0,008 0,010
Оптическая плотность,, , . . „, 0,180 0,500 0,660 0,820 0,980 1,306 1,60»
На основании этих данных строят градуировочный график, откладывая по оси абсцисс содержание дивинилбензола (в %), а по оси ординат оптическую плотность D, измеренную по отношению к чистому стиролу при Я=313 им для толщины слоя 5 мм.
Определение гидрохинона. Стирол не должен содержать гидрохинона. Для проведения пробы к 5 мл стирола добавляют 5 мл раствора NaOH и смесь взбалтывают. При отсутствии гидрохинона нижний слои не дает окраски. Если появляется желтая окраска, то стирол от
мывают от гидрохинона раствором NaOH, как указано выше. При этом: гидрохинон кислородом воздуха окисляется в хинон:
2С6Н4 (ОН)2 + 02 ->■ 2С6Н402 + 2Н20

 Опубликовано в
Опубликовано в