ПРИНЦИП ДЕЙСТВИЯ ЭЛЕКТРОХИМИЧЕСКИХ УСТРОЙСТВ С ИОНООБМЕННЫМИ МЕМБРАНАМИ
 17 октября, 2016
17 октября, 2016  Mihail Maikl
Mihail Maikl В настоящем параграфе будет рассмотрен принцип действия не только ТЭ, но и других электрохимических устройств с использованием ИОМ, либо представляющих самостоятельный интерес, либо используемых при исследованиях ТЭ.
6.1.1. Топливный элемент системы водород — кислород
Схема ТЭ системы водород — кислород представлена на рис. 6.5. К катионообменной мембране 2 с двух сторон присоединены пористые анод 1 и катод 3 с каталитическим покрытием, находящимся в контакте с ИОМ. На аноде водород ионизируется по реакции
2Н2-»-4Н++4е~.
Гидратированные протоны под действием градиента концентрации и электрического поля мигрируют сквозь ИОМ к катоду, где происходит катодная реакция
"iWf' 02 + 4Н+(Н20)„ + 4е--^(Н20)„+2. . , :
6.1.2. Водородный насос
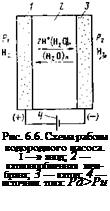
Если к электродам подать разность потенциалов от внешнего источника тока, то можно осуществить перекачку водорода из анодной полости в катодную с повышением давления водорода, т. е. по существу электрохимическое устройство будет работать как водородный насос. Схема такого устройства приведена на рис. 6.6. Устройство его и анодные процессы аналогичны ТЭ, а результирующая реакция на катоде
4Н+ + 4е~-^2Н2.
 |
Теоретически повышение давления водорода, которое можно осуществить в рассматриваемом устройстве, определяется из уравнения
где п—2.
При этом необходимо иметь в виду, что разность потенциалов U, прикладываемая к элементу, не учитывает поляризационных по-
терь на электродах и ИОМ, которые зависят от конкретного исполнения и плотности тока. Во избежание пересушки ИОМ водород, поступающий в анодную полость, необходимо увлажнять. Водородный насос можно использовать и для извлечения водорода из смеси водородсодержащих газов, если, конечно, в ней отсутствуют каталитические яды. .

 Опубликовано в
Опубликовано в