Окисление металла и установление сродства элемента к кислороду
 21 февраля, 2016
21 февраля, 2016  xeil
xeil Кислород особенно интенсивно влияет на ход металлургических процессов при сварке. Окисление металла в сварочной ванне может происходить: при наличии в газовой фазе свободного кислорода или сложных газовых молекул (С02, Н20), способных при диссоциации выделять кислород; при наличии в шлаке оксидов, растворимых в металлической ванне; при химически активных компонентах, вступающих в обменные окислительно-восстановительные реакции с металлом сварочной ванны.
Окисление металла свободным кислородом газовой фазы протекает тем более интенсивно, чем больше сродство металла к кислороду. Оценить степень сродства металла к кислороду можно по прочности образующегося сщсида, которая зависит от его вида, температуры и от давления кислорода, взаимодействующего с оксидом.
С повышением температуры прочность оксида понижается, происходит его диссоциация и выделяется кислород. Однако это будет иметь место только лишь в том случае, когда давление соприкасающегося с оксидом кислорода будет меньше давления кислорода, выделяющегося при диссоциации оксида. Если давления равны, то диссоциация оксида не происходит и наступает равновесие.
Давление кислорода в данной системе при нахождении ее в состоянии равновесия носит название упругости диссоциации данного оксида и обозначается ро2.
Установлено, что положение равновесия реакции окисления данного элемента (реакция диссоциации его оксидов)
всецело определяется величиной упругости кислорода в равновесной системе или иначе упругостью диссоциации оксида ро2- Чтобы судить о направлении реакции окисле^ ния по упругости диссоциации оксида данного элемента, надо упругость диссоциации pos сравнить с парциальным давлением кислорода ро2факт в условиях реакции.
Парциальное давление представляет собой давление, которое оказывал бы газ, если бы он один находился в сосуде, в том количестве, в котором он находится в смеси.
 Тогда парциальное давление кислорода при О °С и 0,1 МПа составит примерно 0,021 МПа.
Тогда парциальное давление кислорода при О °С и 0,1 МПа составит примерно 0,021 МПа.
Если при комнатной температуре упругость диссоциации оксида ро3 меньше парциального давления кислорода в атмосфере Рог факт» ТО состояние оксида устойчиво, и металл на воздухе окисляется. Если ро2 выше Рог факт, то устойчивым CO - стоянием будет чистый металл. Металлы с высокой упругостью диссоциации не окисляются на воздухе, например, золото, платина. ЕСЛИ р02 РО, факт» то состояние равновесия наступило, и реакция приостановится. У большинства металлов упругость диссоциации оксидов меньше парциального давления кислорода в атмосфере, поэтому они окисляются на воздухе.
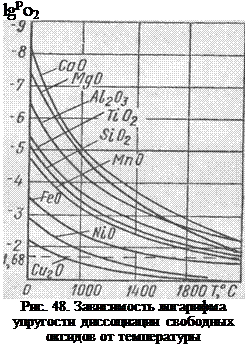
Упругость диссоциации оксида и, следовательно, сродство элементов к кислороду зависит от температуры. Обычно упругость диссоциации оксидов с повышением температуры у всех металлов увеличивается, а сродство к кислороду уменьшается. Зависимость упругости диссоциации оксидов разных металлов от температуры представлена па рис. 48. Чем выше расположена кривая в этой системе координат, тем меньше упругость диссоциации представляемого ею оксида и тем более сильным раскислителем будет рассматриваемый элемент.
Для любого оксида область графика, лежащая выше соответствующей кривой, определяет устойчивое существование данного элемента в свободном состоянии, т. е. в чистом виде, а область графика, находящегося ниже этой кривой, определяет условие устойчивого существования оксида данного элемента. Для удобства сопоставления упругости диссоциации оксида с парциальным давлением кислорода логарифм парциального давления кислорода в воздухе, равный — 1,68, нанесен на график в виде штриховой линии.
Так, при равных концентрациях и температуре 2000 VC наибольшим сродством к кислороду обладает Са, затем Mg, А1, Ті, Si, Мп, Fe, Ni и Си. Последние два элемента обладают меньшим сродством к кислороду, чем железо. Рассмотренное справедливо, если элементы окисляются свободно и независимо друг от друга, находясь в одинаковых внешних условиях.
В реальных условиях сварки последовательность окисления элемента сплава и скорость протекания окисления зависят не только от степени сродства элемента к кислороду, но и от концентрации его в расплаве. При этом установлено, что элемент будет окисляться тем легче, чем больше его концентрация.

 Опубликовано в
Опубликовано в