ФЛЮСОВАЯ ПАЙКА
 16 апреля, 2016
16 апреля, 2016  admin
admin Для защиты от окисления основного металла в процессе пайки флюс должен иметь температуру расплавления ниже температуры солидуса припоя, так как флюс в твердом состоянии не способен защищать паяемый металл и припой от окисления на воздухе. Флюс должен хорошо смачивать поверхность паяемого металла и припоя, растекаться и затекать в зазор между соединяемыми деталями, удалять адсорбированные на них газы, сохранять покровное действие до конца пайки. Флюс должен быть легче припоя и образовывать с ним два несмешивающихся слоя. При нарушении последнего требования в шве образуются флюсовые включения, имеющие выход наружу, ослабляющие паяемый шов, а при высокой коррозионной их активности способствующие развитию коррозии в паяемом соединении после вскрытия пор (например, при механической обработке), заполненных флюсом.
Флюс в условиях неконтролируемого нагрева, например, при газопламенной или индукционной пайке, имеющий температуру плавления на 50 °С ниже температуры плавления припоя, является своеобразным индикатором для определения момента подачи припоя в зазор. Кроме того, только при этом условии он успевает очистить паяемую поверхность от тонкого слоя оксидов до расплавления жидкого припоя. При более высокой температуре плавления флюса, чем температура плавления припоя, поверхность паяемого металла к моменту плавления припоя останется неофлюсованной и сильно окислится.
К важнейшим составляющим паяльных флюсов относятся их активаторы и растворитель. В отдельных случаях в них могут быть введены ингибиторы, понижающие коррозионную активность их остатков и шлаков после пайки и поверхностно-активные вещества (ПАВ), понижающие поверхностное натяжение на границе металла с флюсом и другие вещества. Активаторами флюсов, участвующих в реакциях при пайке, являются, главным образом восстановительные органические и неорганические кислоты.
Согласно ГОСТ 19250—73 флюсы классифицируются по следующим признакам: температурному интервалу их активности, природе растворителя, природе активаторов, по механизму действия, агрегатному состоянию при поставке. По температурному интервалу активности различают флюсы для низко - и высокотемпературной пайки. Температурный интервал активности у флюсов для низкотемпературной пайки находится не выше 450 °С, а у флюсов для высокотемпературной пайки — выше 450 °С.
По характеру взаимодействия на оксиды различают флюсы электрохимического, химического и растворно-химического действия. Флюсы защитного действия предохраняют очищенный предварительно от грязи, жиров и оксидов паяемый металл от окисления при хранении перед пайкой. К флюсам электрохимического действия относятся гигроскопичные хлоридные флюсы ДЛЯ НИЗКО - 140
температурной пайки, хлоридно-фторидные флюсы для высокотемпературной пайки. Как показали исследования, боридно - фторидные флюсы, применяемые для пайки сталей и медных сплавов, относятся к флюсам растворно-химического действия. Вероятно, к этому же классу относятся боратно-хлоридные и боратно-фторидные флюсы, используемые для пайки сталей и никелевых сплавов.
Флюсы для низкотемпературной пайки меди, ее сплавов и сталей. К флюсам для низкотемпературной пайки с выраженным электрохимическим действием относятся неорганические флюсы хлоридного типа, состоящие из слабодиссоциирующего растворителя и активатора. В качестве растворителя для таких флюсов используют воду, спирты, а в качестве активаторов — соляную кислоту и хлориды тяжелых металлов.
К флюсам преимущественно химического действия относятся органические флюсы. Те из них, которые активированы хлоридами, также имеют электрохимическое действие.
По природе растворителей флюсы могут быть полярными (вода) и неполярными (одно - и многоатомные спирты). Активаторами флюсов являются неорганические кислоты (соляная и фосфорная) и некоторые органические кислоты. Эти активаторы можно подразделить на два типа:
1) растворяющиеся в полярных жидкостях (воде); такие активаторы могут ионизировать и приводить к коррозии (соли неорганических кислот, сахара и др.);
2) растворяющиеся в неполярных жидкостях (жирах, канифоли, маслах, этиловом спирте) и не вызывающие коррозии; к ним относятся органические кислоты, например абиетиновая кислота, плавящаяся при 173 °С, которая является основным активатором канифоли. Канифоль не растворяется в воде, а растворяется только в неполярных жидкостях (например, в этиловом спирте). Спиртовой раствор белой канифоли в этиловом спирте с 0,5 % хлоридов тяжелых металлов имеет повышенную активность при пайке.
Главной составной частью канифоли является абиетиновая кислота С20Н30О2, плавящаяся при 173 °С. Расплавленная канифоль может растворить очень тонкий слой оксида меди (оранжевокрасного цвета), т. е. она является очень слабым растворителем оксидов. Слой канифоли, остающийся после пайки, защищает паяный шов от коррозии (в умеренном климате).
При температуре 200 °С канифоль активна; с повышением температуры она начинает испаряться; при 300 °С испаряется 7 % канифоли. При нагреве выше 300 °С канифоль обугливается, что затрудняет процесс пайки. При достаточно быстром нагреве (пайка электросопротивлением, открытыми нагревателями и т. п.) паять с канифольсодержащими флюсами можно и при более высоких температурах (350—370 °С). Для предотвращения обугливания канифольных флюсов и появления пористости в швах нагрев до 350—370 °С можно вести в среде чистого проточного аргона.
Канифольные флюсы пригодны для пайки серебра, кадмия или деталей, покрытых серебром или кадмием, а также меди, латуни и фосфористой бронзы, особенно при пайке погружением в оловянные припои.
Канифоль применяют в виде порошка или раствора в спирте, глицерине, смесях керосина и бензина. Канифольный флюс в смеси керосина и бензина может быть такого состава: 40 % канифоли, 50 % бензина, 10 % керосина.
Недостатком канифольных флюсов является то, что они прочно пристают к металлу и смываются только спиртом, бензином, скипидаром или щелочью. Добавка к 25 %-ному спиртовому раствору канифоли около 50 % стеарина улучшает технологические свойства флюса — он стирается тряпкой.
Рекомендован флюс, содержащий 10 % канифоли, 20 % стеарина, остальное — спирт.
Для усиления флюсующего действия в канифольные флюсы, кроме малоактивных веществ, вводят неорганические или органические соединения — кислоты, галогениды и др. Флюсы этой группы при добавке небольших количеств подобных активирующих веществ могут быть слабо коррозионно-активными, а при больших количествах — коррозионно-активными.
В качестве активирующих компонентов флюсов применяется ортофосфорная кислота. Метафосфорная кислота при нормальной температуре твердая, гигроскопичная и неудобна для пайки. Жидкая ортофосфорная кислота в виде 40—60 %-ных спиртовых растворов эффективна при пайке алюминиевой бронзы и коррозионно-стойкой стали.
Фосфорная кислота, вероятно, может не только влиять на удаление оксидов с поверхности коррозионно-стойкой стали, но и вызывать образование тонкой пленки фосфатов, которые в противоположность оксидам смачиваются оловянно-свинцовыми припоями. Продукты распада ортофосфорной кислоты после пайки вызывают коррозию паяного соединения. Поэтому кислоту смешивают с канифолью, применяя в качестве растворителя этиловый спирт.
Водный раствор соляной кислоты эффективно воздействует при пайке на сталь, монель и сплавы никеля с медью.
Из органических кислот, активизирующих канифольно-спиртовой флюс, применяют водный раствор молочной кислоты СНзСНОН-СООН (15 % молочной кислоты, 84,8 % воды и 0,2 % смачивающей присадки) или смесь ее с канифолью (20 % канифоли, 5 % молочной кислоты и 75 % этилового спирта). Последний флюс слабо коррозионно-стойкий и малоэлектропроводный, применяется для пайки электрической аппаратуры. Молочная кислота плавится при температуре 18 °С.
В качестве компонента флюсов был предложен один из азотоводородов — гидразин N2H4 и его производные (соли). Соли — гидрохлориды гидразина ^Н4*НС1 и ^Н4*2НС1 и другие обладают сильной восстанавливающей способностью и токсичностью.
Наиболее пригодны хлориды и бромиды гидразина. При температуре 200—250 °С происходит медленное разложение этих солей с образованием хлоридов или бромидов аммония, что повышает активность флюсов и исключает коррозионно-активные осадки на изделии. В связи с этим отпадает необходимость промывать изделие после пайки. В качестве флюсов такого типа применяют 5—7 %-ные водные или спиртовые растворы солянокислого, сернокислого или фосфорнокислого гидразина или их смеси с хлоридами олова и аммиака.
Гидразин плавится при температуре 2 °С и кипит при температуре 113,5 °С. Гидразин и его соли гигроскопичны и взрывоопасны. Гидрохлорид гидразина N2H4*2HC1 плавится при температуре 198 °С. Остатки гидразиновых флюсов легко смываются спиртом или водой. В качестве примера приведем состав одного из гидразиновых флюсов: 5—7 % солянокислого гидразина, 15—20% глицерина, остальное — дистиллированная вода. Некоторые флюсы, содержащие производные гидразина, при использовании их для пайки алюминиевых или медных сплавов не вызывают коррозии последних.
Наибольшее распространение среди активаторов флюсов для пайки имеют хлористые соли.
Хлорид цинка — соль белого цвета, легко растворяется в воде и в спирте и присоединяет пары воды из воздуха, образуя при этом жидкий раствор; температура плавления его 283 °С.
Действие хлорида аммония как флюса заключается в том, что он переводит оксиды металлов в их хлориды, которые с хлоридом аммония образуют легкоплавкие, летучие или легко растворяющиеся соединения или эвтектики. С хлоридом железа ГезСІз хлорид аммония, например, образует эвтектику с температурой плавления 220 °С.
Хлорид аммония в твердом состоянии употребляется также для очистки медных паяльников от образующихся на них оксидов меди СигО и СиО. При взаимодействии хлорида аммония с оксидами меди образуются хлорид меди, аммиак и вода:
NH4C1->NH3 + HC1;
CuO + 2HC1-+CuC12 + Н20;
Cu20 + 2HC1^2CuC1 + H20.
Аммиак диссоциирует при нагреве на N2 и ЗН2, и получаемый при этом водород может служить восстановителем и защитной средой. При взаимодействии хлорида меди с хлоридом аммония образуются растворимые двойные соли (CuCl *6NH4C1). Хлорид меди с хлоридом аммония образует эвтектику, плавящуюся при температуре 140 °С.
В результате гидролиза раствора хлорида цинка образуются пары хлористого водорода, которые, воздействуя на оксиды металла, переводят их в более растворимые хлориды.
Продукты гидролиза хлорида цинка вызывают интенсивную коррозию паяного соединения.
Р. С. Ден и Р. В. Вильсон предложили ряд флюсов, не растворимых в воде (не способных к гидролизу) и при нагреве выделяющих хлористый водород, но не образующих продуктов реакции, способных вызвать коррозию паяемых сплавов. Это — наф - тален тетрахлорид, нафтален тетрабромид и др. Однако, как указывают авторы, во влажном воздухе пары хлористого водорода конденсируются на паяном соединении и могут способствовать его коррозии. Смеси хлорида цинка с хлоридом аммония обладают большей активностью, чем каждый из них в отдельности. Температура плавления у смеси ниже, чем у хлорида цинка. При содержании 27 мол. % NH4C1 образуется эвтектика между ZnCb и соединением 2ZnCl2* NTUC1, плавящаяся при температуре 232 °С.
Соединение 2ZnCl2*NH4Cl имеет температуру плавления 249 °С. При содержании 49 мол. % NH4C1 образуется вторая, более легкоплавкая эвтектика с температурой плавления 180 °С. Смеси хлорида цинка и хлорида аммония неустойчивы и при нагреве могут разлагаться с образованием цинкаммонийных хлоридов Zn(NH3)2Cl и 2n(NH4)Cl, являющихся также активными флюсами. Хлорид железа с хлоридом цинка образует эвтектику, плавящуюся при температуре 214 °С.
В качестве флюса рекомендуется эвтектика ZnCb—NH4C1 (28 % NH4C1) или близкая по составу смесь 65—75 % ZnCl2 и 35—25 % NH4C1, а также смесь, состоящая из 50 % ZnCl2 и 50 % NH4C1. Последний флюс пригоден для пайки с легкоплавкими припоями, имеющими повышенную температуру плавления (92 % РЬ и 8 % Sn; 98,5 % Pb и 1,5 % Ag; Zn и т. д.).
Флюсы, содержащие хлориды цинка и аммония, следует хранить в стеклянной, керамической или деревянной таре, но не в металлической. Эти флюсы не должны содержать солей меди, свинца, железа, так как при пайке железа указанные металлы восстанавливаются из солей и образуют на поверхности паяемой детали черный налет. Очистку флюсов от примесей солей тяжелых металлов производят гранулированным цинком, который помещают во флюс на несколько дней. В хорошо очищенном флюсе новая порция гранулированного цинка не должна покрываться черным налетом.
В некоторые флюсы, содержащие хлориды цинка и аммония, добавляют 5—10 % глицерина, который улучшает смачиваемость поверхности металлов флюсом (например, флюс «Прима 1»).
Остатки флюсов, содержащих хлориды цинка, аммония, кадмия, олова, способствуют развитию коррозии в паяном шве и должны быть тщательно удалены после пайки промывкой водой или спиртом. К флюсам (смесь ZnCb и NH4C1), предназначенным для пайки с легкоплавкими припоями, рекомендуется добавлять фториды. Фториды более активны, чем хлориды, но многие из них ядовиты.
Хлоридные флюсы применяют в виде твердой смеси, порошков, водных растворов, пасты. При изготовлении хлоридных флюсов в виде пасты к ним добавляют вазелин (например, смешивается 25 г хлорида и 100 г вазелина при температуре 75 °С), минеральное масло, глицерин, веретенное масло, воск, клейстер и другие безводные смеси (например, 20 ч. хлорида цинка, 12 ч. глицерина и 3 ч. спирта).
Для пайки с легкоплавкими припоями применяют хлориды ZnCh, CdCb, SnCh и др. Хлорид свинца слабо растворим в воде и малоактивен в качестве компонента флюса. Хлорид кадмия повышает температуру плавления хлорида цинка. Смесь хлоридов цинка и алюминия с глицерином рекомендуется для пайки с безоловянными легкоплавкими припоями.
Характерно, что при пайке золотых и позолоченных деталей припоями, богатыми свинцом, с применением активированных флюсов ЛК2, ЛТИ-120, плохое смачивание, вероятно, связано с пассивированием паяемой поверхности. Поэтому пайка таких деталей может быть выполнена качественно с применением слабоактивных флюсов, например с флюсом ВТС.
Все активные флюсы для пайки легкоплавкими припоями позволяют паять металлы без предварительной подготовки; при применении слабоактивных флюсов иногда требуется облужи - вание металла.
Компонент флюсов триэтаноламин N(CH2CH2OH)3, с температурой кипения 279 °С, токсичен, растворим в воде, хранить его нужно в металлической таре.
Флюс 38Н высокоактивен, но вызывает заметную коррозию; наивысшая активность флюса при 350 °С вследствие термического разложения его компонентов и выделения веществ, активно удаляющих оксидную пленку металлов. Остатки флюса легко смываются водой или спиртом.
Остатки флюсов (ФИМ, ЛМ1), содержащих ортофосфорную кислоту, после пайки способствуют коррозии паяного соединения, их необходимо удалять спиртом.
Флюсы, в которых солянокислый анилин (СбН5ІМНз)С1 является основной составляющей, так же эффективны, как и анилинфос - фат. При нагреве таких флюсов выделяется хлористый водород, способствующий удалению оксидов на паяемом шве; он применяется для тех же целей, что и анилинфосфат. Солянокислый анилин плавится при температуре 199 °С, испаряется при температуре 245 °С и легко растворяется в воде и спирте. Остатки анилинофосфатных флюсов после пайки слабо растворимы в воде.
Эти остатки можно и не удалять ввиду их нейтральности при коррозии. Анилинофосфатные флюсы применяют для пайки деталей, покрытых оловом, серебром и кадмием, и при пайке меди, латуни, кремнистой и фосфористой бронзы.
При пайке некоторых токопроводящих деталей — телефонной, радио - и другой электрической аппаратуры — неприемлемы коррозионно-активные флюсы, так как они могут способствовать коррозии паяных швов и разрушению изоляционных материалов или снижению их влагостойкости. Такую аппаратуру паяют почти исключительно с канифольно-спиртовым флюсом.
Солянокислый анилин не растворяется в канифоли и может после испарения спирта осаждаться на паяемой детали и оказывать корродирующее действие.
Для улучшения смачивания поверхности во флюсы вводят иногда смачивающие присадки, например сульфорициновый аммоний.
Среди канифольных флюсов светлая канифоль является в известной степени идеальным флюсом, так как при нормальной температуре она коррозионно-инертна и является электроизолятором, ее остатки, в том числе конденсат, обладают теми же свойствами. После расплавления канифоль активно флюсует золото, серебро, медь и некоторые сплавы. Однако ее активность недостаточна для других металлов. Светлую канифоль применяют для гарантии от коррозии при пайке медных проводов в телефонной и телевизионной связи, в микроэлектронике.
По данным Г. А. Кондратовича и других, активность канифоли повышается при ультразвуковой обработке (/=184-22 кГц) дисперсной смеси канифоли в растворителе в течение 1—20 мин, что сокращает время отмывки остатков флюса и повышает производительность труда.
Следует отметить, что предельная концентрация дыма от канифоли и ее флюсов при пайке составляет 0,1 мг/м3. При больших количествах дыма возможны насморк, слезотечение, раздражение кожи, астма. Астма может быть и от изоцианидов, выделяющихся при нагреве изоляционных эмалей на основе полиуретанов на проводах. Предельная концентрация изоцианидов 2* 10_6 % [32].
Активность при низкотемпературной пайке и коррозионная активность флюсов существенно зависят от степени их кислотности и тем выше, чем ниже кислотность флюса при температуре пайки. Вместе с тем повышение кислотности флюсов до и после пайки способствует развитию коррозии в паяных соединениях и изделиях. Поэтому идеальным был бы флюс с высокой кислотностью при температуре пайки и низкой кислотностью до и после пайки.
Кислотность жидких растворов характеризуется величиной pH. Кислотность флюса зависит от его состава и может изменяться при нагреве по термическому циклу пайки вследствие испарения или окисления, химического взаимодействия его с оксидами или металлом. При значении рН> 7 флюс имеет щелочную реакцию; при pH = 7 — нейтральную; при pH <7 — кислотную. Чем меньше pH, тем выше кислотность флюса. Все это требует правильного выбора температурно-временного режима пайки и строгого дозирования флюса.
Для низкотемпературной пайки меди и ее сплавов применяют четыре типа флюсов [31]. Флюсы первого типа характеризуются неизменностью значений pH до и после пайки [12]. Если при этом pH^7, то флюс достаточно активен при пайке, но его высокая гигроскопичность до и после пайки способствует развитию коррозии паяного соединения. К таким флюсам относится, например, флюс 38Н. При pH, близком к 5—6, флюс слабо активен при пайке, а при температуре 20 °С до и после пайки не вызывает существенной коррозии. К таким флюсам относятся КЭ и ВТС (табл. 29, 30).
К флюсам второго типа отнесены такие, pH которых достаточно высок до пайки, уменьшается при нагреве и остается таким же после пайки при охлаждении до 20 °С (флюсы «Прима 1» и Ф55). Подобный характер изменения pH при нагреве и охлаждении обусловлен слабым испарением НС1, образующейся при разложении солянокислого гидразина (240 °С), хлорида аммония NH4C1 (337 °С), солянокислого диэтиламина в растворе двух - и трехатомных спиртов.
К флюсам третьего типа отнесены такие, у которых pH ^7 до и после пайки и возрастает при пайке и особенно после нее. К таким флюсам относятся КЭЦ, гидразиновый, «Прима 2».
Такой характер изменения кислотности у флюсов для низкотемпературной пайки при нагреве и последующем охлаждении обусловлен тем, что испарение НС1 при нагреве в присутствии воды или одноатомного (этилового) спирта происходит интенсивнее, чем в двух - и трехатомных спиртах (например, в глицерине).
К четвертому типу относятся флюсы с относительно высоким значением pH (4—5) до и после пайки и низким его значением (1—2) при температуре пайки, например, флюсы ЛТИ-120, ЛК2, паста НИСО.
Для низкотемпературной пайки в качестве растворителей паяльных флюсов используют спирты: одноатомные (метанол, этанол, изопропиловый спирт и др.; двухатомные (гликоли); трехатомные (глицерин) или их смеси или полиэфиры на основе спиртов. С увеличением относительной молекулярной массы в гомологическом ряду одноатомных спиртов уменьшается их растворимость в воде и появляется резкий запах, что характерно для высших спиртов.
К спиртам с высокой температурой кипения (разложения), высокими поверхностно-активными свойствами, без запаха, бесцветных и малотоксичных при температуре пайки 150—300 °С и растворимых в воде относятся глицерин, неонол, полиэтилен-
|
Таблица 29. Коррозионно-неактивные или слабоактивные флюсы для пайки металлов легкоплавким припоем ПОС 61
|
|
Флюс |
Состав флюса |
Температурный интервал активности, °С |
Назначение |
|
Ф38Н |
50 % этиленгликоля или глицерина или их смеси 1:1; 25 % солянокислого диэтиламина; 25 % ортофосфорной кислоты |
300 |
Для пайки нихрома, бе - риллиевой и алюминиевой бронз, константана, магнанина, коррозионно - стойких сталей |
|
ФИМ |
200 мл ортофосфорной кислоты; 1 мл этилового спирта; 1 мл воды |
— |
Для пайки алюминиевой и бериллиевой бронз, коррозионно-стойких сталей |
|
ВТС |
100 г вазелина; 10 г салициловой кислоты; 10 г триэтаноламина; 40 г этилового спирта |
240—300 |
Для пайки меди, серебра, золота, платины и их сплавов |
|
Таблица 30. Коррозионно-активные флюсы для пайки легкоплавким припоем ПОС 61
|
гликоль, полиэфир. По данным В. Г. Самойленко, эти растворители флюса не обладают флюсующими свойствами при пайке меди сплавом Розе при 150 °С. Флюсующая активность этих растворителей флюсов оценивается по времени флюсования и увеличивается с повышением температуры до 300 °С. С увеличением относительной молекулярной массы полиэтиленгликолей от 600 до 3500 время смачивания при температуре 240—390 °С (350 °С) снижается. Поэтому для флюсов лучше использовать смеси высококипящих растворителей (например, глицерина или ПЭГ-400, ТУ 6-01-911 — 74), в которые добавляют 5% неонола а для увеличения адгезионных свойств флюсов — до 15—20% полиэфира П2200 (ТУ 6-05-1607—73).
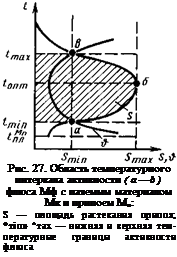 Температурный интервал активности флюса при пайке зависит от состава применяемого припоя, паяемого материала и времени выдержки при температуре пайки. Критерием активности флюса может быть площадь растекшейся дозированной порции припоя или его контактный угол смачивания.
Температурный интервал активности флюса при пайке зависит от состава применяемого припоя, паяемого материала и времени выдержки при температуре пайки. Критерием активности флюса может быть площадь растекшейся дозированной порции припоя или его контактный угол смачивания.
Существующие данные о температурных интервалах активности известных флюсов для различных пар Мк—Мп пока ограничены. В большинстве случаев ограничиваются данными о температуре пайки, ориентировочно определяемыми по испаряемости или термостойкости компонентов флюсов без указания оптимальной температуры пайки и допустимого времени сохранения активности флюса (его «живучести») при этой температуре. Форма области, определяющей температурный интервал активности флюса Мф с паяемым материалом Мк и припоем Мп, имеет в общем виде форму, представленную на рис. 27.
Важными признаками при оценке пригодности флюса, кроме его активности при пайке и коррозионной активности его остатков после пайки, являются его электрическая проводимость и влияние на свойства паяемого материала. Желательно, чтобы флюс, а также его конденсат не вызывали коррозии после пайки, были электропроводными при пайке и являлись изоляторами при температуре 20 °С. Флюс не должен ухудшать свойства паяемого металла и паяных соединений в результате насыщения его, например, бором, развития межзеренной или химической эрозии и др.
Существующие в настоящее время флюсы для низкотемпера
турной пайки меди и стали можно классифицировать на канифольные, органические без канифоли и неорганические.
Флюсы для низкотемпературной пайки алюминия и его сплавов. В табл. 31 приведены состав, температурные интервалы активности и назначение некоторых флюсов, разработанных с 1973 по 1984 г. [23]. По данным В. И. Павлова, среди органических кислот и других веществ, пригодных в качестве активатора флюсов
|
Таблица 31. Некоррозионно-активные и слабокоррозионно-активные флюсы для низкотемпературной пайки и лужения алюминия
|
|
Марка или номер флюса |
Состав флюса, % |
Температурный интервал активности, °С |
Примечание, |
|
8 |
5—8,6 ВіВг2; 23—39,8 капроновой кислоты; канифоль — остальное |
<450 |
|
|
9 |
10—15 тетрафторбората цинка; триэтаноламин остальное |
>350 |
Для пайки алюминиевых проводов с изоляцией (повышает ее стабильность) * |
|
10 |
7.5 фторгидрата анилина; 92.5 канифоли |
<250 |
То же |
|
11 |
83 триэтаноламина; 9 фтор - бората кадмия; 7 кислого фтористого аммония; 1 канифоли |
> 150 |
» |
|
* Пат. 79633 СРР, МКИ3 В23 К 35/22, В 23 К 35/34 |
для пайки алюминия и его сплавов при температуре <300 °С, пригодны только алифатические кислоты, их амиды, а также триэтаноламин, имеющий свойства основания. Среди алифатических кислот наиболее активны одноосновные кислоты: стеариновая, элаидиновая, олеиновая, лауриновая, коприновая, каприловая, капроновая, валериановая, масляная, пропионовая, уксусная, муравьиная. Активность этих кислот повышается с увеличением их относительной молекулярной массы и температуры плавления. При взаимодействии их с оксидом А120з протекают следующие реакции:
А120з + 6RCOOH+2 (RCOO) 3А1 + ЗН20; (15)
2А1 + 6RCOOH+ (RCOO) 3А1 + ЗН2. (16)
Наиболее энергично протекает реакция (14) с муравьиной и уксусной кислотами, менее энергично с капроновой кислотой. Однако введение этих кислот во флюсы мало перспективно вследствие их интенсивного выкипания при температуре пайки и снижения энергии разрыва связи СОО—НС — с возрастанием молекулярной массы кислоты. Соли карбоновых кислот, получаемые по реакциям (15) и (16), термически неустойчивы. Например, уксуснокислый алюминий разлагается при температуре 200 °С.
Среди двуосновных предельных кислот, более сильных, чем одноосновные, первые три члена гомологического ряда кислот (щавелевая, малоновая, янтарная) не обладают активностью при пайке алюминия, что обусловлено декарбоксилированием их при
нагреве. Высшие кислоты имеют во флюсах такую же активность, как и одноосновные кислоты, с тем же числом атомов в радикале.
Ангидриды кислот не активны при пайке. Более высокую активность во флюсах для пайки алюминия имеют галогенза - мещенные кислоты, что объясняется одновременным воздействием на оксид алюминия как карбоксильной группы, так и атома галогена.
Обнаружено, что активны во флюсах некоторые твердые аминокислоты: а-аминопропионовая и фениланитрониловая,
которые обеспечивают хорошее растекание припоя.
С учетом физических свойств, степени токсичности и активности во флюсах среди органических кислот наиболее пригодными можно считать высшие жидкие незамещенные кислоты, их твердые аналоги и аминокислоты. Флюсующая способность смесей кислот в любых соотношениях не превышает активности компонента с наиболее высокой молекулярной массой.
Салициламид и мочевина по активности равноценны действию капроновой или элаидиновой кислоты.
Активность аммонийных солей органических кислот близка к активности исходных одно - и двуосновных кислот. Эти соли имеют преимущества перед амидами — меньшую летучесть при пайке и лучшую растворимость в кислотах. Характерно, что введение органических кислот и их производных в триэтаноламин не повышает его активности при флюсовании алюминиевых сплавов.
Дальнейшее повышение флюсующей активности кислотных органических растворов достигается при добавке в них галлоид - ных солей аминов или металлов. Введение в дециловый спирт (температура кипения 231 °С) LiJ и SnCb или в капроновую кислоту (температура кипения 205 °С) LiBr, LiJ, Nal, SnCL в виде кристаллогидратов активирует раствор.
Введение в кислотные флюсующие растворы солей 95 %-ного этилового спирта дезактивирует их из-за вытеснения воды по реакции:
А1 (OR) з + 3H20-WV1 (ОН) 3 + 3ROH.
Однако присутствие кристаллизационной воды в спиртовом растворе хлорида олова не влияет на активность его при пайке.
Для пайки алюминия легкоплавкими припоями М. А. Макси - михиным, В. Д. Нестеровой, В. Д. Орловой были предложены реактивные органические флюсы. Основой этих флюсов является органический аминоспирт триэтаноламин, а активаторами фтор - бораты тяжелых металлов и аммония. В местах контакта фторбо - ратов с алюминием через несплошности в оксидной пленке А120з высаживаются металлы: кадмий и цинк. Остатки триэтаноламина в процессе нагрева переходят в инертное вещество смолообразного вида, не вызывающее коррозии паяных соединений. Эти флюсы и их остатки после пайки имеют pH = 8, что также подтверждает их некоррозионно-активность. Все эти флюсы не отличаются по коррозионной активности при пайке алюминия, но при пайке его со сплавом АМц, медью и ее сплавами наиболее эффективным является флюс Ф59А. Температурный интервал активности этих флюсов 150—300 °С. Флюсы этого типа непригодны для пайки в нахлестку с укладкой припоя у зазора деформируемых сплавов АМг, Д1, Діб, В95 и литейных алюминиевых сплавов. Ими можно пользоваться только при облуживании паяемой поверхности алюминия с последующей пайкой, например с флюсом ЛТИ-120. При этом температура между паяемыми деталями при пайке не должна отличаться более чем на 10 °С. Остатки флюсов легко смываются водой или протираются влажной салфеткой, смоченной водой или этиловым спиртом, и не вызывают сколько-нибудь заметной коррозии в течение более 1000 ч. Исследования показали, что по сравнению с флюсами, содержащими в качестве растворителя уксусную, капроновую, олеиновую, лауриновую кислоты, а в качестве активатора хлорид висмута, флюс Ф54А обеспечивает большую площадь растекания припоя П250А по алюминию АД1; но он менее активен при пайке коррозионно-стойкой стали, латуни и меди, чем флюсы, содержащие хлорид висмута.
Флюсы Ф54А, Ф59А и Ф61А пригодны для пайки в указанном интервале температур припоями П200А, П250А, П300А, П170А и П150А. Для этого используют терморегулирующие электропаяльники, индукционный нагрев, а также пайку погружением в расплавленный припой. Недопустима пайка с этими флюсами при нагреве открытым пламенем из-за возможности их сгорания. При температуре выше 350 °С в паяных швах соприкасающихся соединений, выполненных этими флюсами, образуются непропаи. При быстром нагреве (электроконтактным, индукционным способами) в среде чистого аргона пайка с этими флюсами возможна при температуре 320 °С.
Есть данные о применении для пайки алюминиевых сплавов легкоплавкого припоя Sn— (8—15)% Zn— (2—5) % Pb с температурой плавления 190 °С с флюсом в виде раствора борнофтористого и фтористого аммония в моноэтаноламине. Во флюсах для низкотемпературной пайки алюминия и его сплавов вместо канифоли предложено использовать пентаэритрит бензоата, который более термостоек, чем канифоль, а остатки его некорро- зионно-активны и в виде эластичной пленки предохраняют паяные швы от окисления. В качестве активатора флюса используют карбоновые кислоты. Паяные соединения (припой П250) не разрушаются в солевом растворе в течение 200 суток. Припой из проволоки (Sn—Pb—Ag) с сердцевиной из указанного флюса пригоден для пайки всех алюминиевых материалов, в которых содержится менее 3 % Mg и 3 % Si.
Флюсы для высокотемпературной пайки меди, ее сплавов и сталей. Для успешного выполнения важнейшей функции паяльных флюсов — удаления оксидов с поверхности меди и сталей при высокотемпературной пайке необходимо их химическое взаимодействие с оксидной пленкой на поверхности паяемого материала и припоя. Для этого среди компонентов флюса должны быть более сильные окислители, чем кислород. По окислительной способности активнее кислорода являются хлор и фтор. Поэтому высокоактивные флюсы, как правило, содержат хлориды и (или) фториды. При этом состав флюсов должен обеспечивать их температуру плавления ниже температуры плавления припоя.
При пайке меди, медных сплавов и сталей в качестве других компонентов флюсов применяют боридные соединения, например буру Na2B407* IOH2O, борную кислоту Н3ВО3 и борный ангидрид В2О3.
Борная кислота растворима в спирте, воде и минеральном масле; ее плотность 1,5 г/см3. При нагреве до 100 °С из нее удаляется часть воды и борная кислота превращается в НВО2. При более высоком нагреве из нее удаляется вся вода и образуется борный ангидрид В2О3, застывающий в виде стеклообразной массы, имеющей температуру плавления 580 °С и испаряющийся при относительно невысокой температуре. Основное свойство В2О3 как компонента флюса в том, что он образует с оксидами меди, цинка, никеля, железа сравнительно легкоплавкие бораты, метабораты и другие сложные соединения.
Бораты имеют хорошие раскисляющее и защитные свойства и длительно защищают паяемый металл и припой от окисления. Большинство боратов плавятся и эффективны при температурах вблизи 760 °С. Для них характерна относительно высокая вязкость в расплавленном состоянии, и поэтому их обычно смешивают с другими солями. Бораты малорастворимы в В2О3 и при избытке образуют два жидких слоя, что снижает активность таких флюсов. Борный ангидрид В2О3 — компонент флюсов для пайки при температуре от 900 °С и выше. Однако в нем мало растворимы оксиды хрома, цинка, кремния и алюминия, и поэтому он не пригоден в качестве компонента флюсов для пайки сталей и сплавов, на поверхности которых образуются оксиды этих металлов.
Бура образует бесцветные прозрачные кристаллы моноклинной структуры. Ее плотность 1,75 г/см3. Бура растворима в воде. При нагреве из буры удаляется кристаллизационная вода: при 100 °С — 5 молей, при 130 °С — 7 — 8 молей; при 150 °С — 9 молей; выше 200 °С — вся вода. Поэтому, чтобы при нагреве бура не кипела, ее необходимо использовать во флюсах в прокаленном виде. Она плавится при температуре 743 °С, а в жидком состоянии распадается на натрийметаборат и борный ангидрид Na2B407 ^ 2NaB02 + B203. Бура используется во флюсах для пайки при относительно невысоких температурах, например, серебряными припоями.
Фториды более жидкотекучи, но хуже защищают паяемый металл от окисления, чем бораты. Фториды имеют и более высокие раскисляющие (флюсующие) свойства. Их используют во флюсах вместе с боратами или щелочными соединениями, такими, как например карбонаты.
В качестве составляющих флюсов наибольшее распространение получили смеси буры и борной кислоты (ВгОз* Na20*2B203), которые образуют два соединения: ЫагО-ЗЕЬОз и ЫагО^ВгОз. Продукты взаимодействия буры с оксидами образуют твердую стеклообразную корку, трудноудалимую с поверхности паяного соединения механическим путем и плохо растворимую в воде.
Соли борной кислоты К4В4О7 и Na2B407 образуют непрерывный ряд твердых растворов с минимумом при 660 °С и при содержании 35 молей К2В4О7. Соли KF и К2В4О7 образуют эвтектику с температурой плавления 680 °С и содержащую 80 молей К2В4О7. Соли Na2F и К2В4О7 образуют эвтектику с температурой плавления 712 °С при содержании 44 моля К2В4О7.
Некоторые смеси солей системы KF—NaF—В2О3, пригодные в качестве флюсов и содержащие гигроскопичные компоненты KF и В203, совершенно негигроскопичны [12].
Смеси борного ангидрида и буры оказывают слабое флюсующее действие при пайке сталей, легированных большими количествами хрома. Для их активирования добавляют разные соли. Наиболее активны добавки фторидов щелочных металлов или фторборатов. Фториды металлов добавляются во флюсы, предназначенные для пайки при температурах 850—1200 °С, а фтор - бораты — для пайки при температурах ниже 850 °С (табл. 32, 33). Стеклообразные остатки флюса ПВ200 (табл. 33) наиболее надежно и быстро удаляют при погружении паяных соединений в водный раствор кислого сернокислого калия KHS04 (100 мл KHSO4 на 900 мл воды); промывку ведут при 20 или 60 °С в течение 60 и 10 мин соответственно. После чего паяное соединение промывают в проточной воде и сушат на воздухе.
При использовании пасты из флюсов ПВ200 или ПВ201 (табл. 33), замешанной на воде или спирте, шов может получиться пористым. Этот дефект отсутствует при замешивании пасты на специальных растворителях — многоатомных спиртах: глицерине и этиленгликоле. Такая паста однородна и хорошо прилипает к паяемому металлу, растворители хорошо испаряются и не вызывают коррозии.
Бораты слабо растворимы в жидком борном ангидриде, поэтому при нагреве до температуры 900 °С в их смесях образуются два жидких несмешивающихся слоя: борного ангидрида и боратов. Активность борного ангидрида, несмотря на то, что его температура плавления равна 580 °С, проявляется только при температуре выше 900 °С. Образующийся в таких флюсах метаборат NaB04 активизирует процесс растворения оксидов, поэтому активность буры как компонента флюса проявляется при температурах немного выше ее температуры плавления и ниже температуры активного действия борного ангидрида.
Борный ангидрид, бура и их смеси непригодны для пайки
|
Флюс |
Состав флюса, % |
Температурный интервал активности, °С |
Назначение |
|
ПВ209* |
41—43 KF; 34—36 В203; 22—24 KBF4 |
500—750 |
Для пайки коррозионно-стойких сталей (по данным С. Н. Лоцманова) |
|
ПВ209Х* |
34,8—36,8 НзВ04; 27,9—29,9 КОН; 34,3— 36,3 KF |
600—750 |
То же |
|
ПВ284* |
25-1-2 В20з; 35-1-2 KF (обезвоженный); 40+2 KBF4 |
500—750 |
Для пайки коррозионно-стойких сталей (по данным С. Н. Лоцманова, В. М. Гостениной) |
|
ПВ284Х* |
29—31 Н3В04; 25—27 КОН; 43—45 KF |
500—750 |
Для пайки коррозионно-стойких сталей |
|
«Салют 1» (ТУ 48-0537—78) |
39 Н3ВО3; 3,5 KN03; 40 KF-2H20; 6,0 KBF4; 4,5 КС1; 7,0 KHF2 |
550—750 |
Для пайки латуней (по данным Б. С. Шеера С. В. Лашко, Г. А. Асиновской и др ) |
|
— |
52—58 KBF4; 26—28 ZnCl2; 8—10 ВаС12; 8—10 LiF |
450 |
Для пайки алюминиевых бронз (по данным В. Р. Бойко) |
|
— |
55 KI1F2; 12,5 CdCl2; 32,5 H3BO3 |
450 |
Для пайки алюминиевых бронз (по данным В. Р. Бойко, С. В. Лашко) |
|
15—22 KBF4; 8—10 криолит; 5—8 ZnCl; 8—10 CaF2; 9—11 MgCl2; тетраборнокислый натрий остальное |
450 |
Для пайки алюминиевых бронз (по данным М. Р. Леписко и др.) |
|
Флюс |
Состав флюса, % |
Температурный интервал активности, °С |
Назначение |
|
ПВ200 * |
65—67 В203; 18—20 Na2B407; 14—16 CaF |
850—1200 |
Для пайки сталей, медных и алюминиевых сплавов. Образует стеклообразные шлаки (по данным С. Н. Лоцманова) |
|
ПВ201 * |
76—78 В203; 11 — 13 Na2B207-10 Н20; 0,9— 1,1 CaF2; 0,9—1,1 лигатура (4 Mg, 48 Си, 48 AI) |
850—1200 |
То же |
|
5—15 НзВОз; 20—25 LiF; 20—55 NH4F; 5—10 марганцовистого калия; 10—22 азотнокислого никеля; 5—8 кремниевокислого натрия |
1050—1150 |
Для пайки коррозионно-стойких сталей. Не образует стеклообразных шлаков |
|
|
Бура |
100 буры |
880—1150 |
Для пайки углеродистых сталей, чугуна, меди, латуни, бронзы, твердых сплавов с припоями системы Си — Zn, Ag — Си |
|
— |
80—50 буры; 20—50 борной кислоты |
850—1150 |
То же при помощи систем Си — Zn, Ag — Си, Си — Ni |
|
18В |
40 KF (обезвоженного); 60 борной кислоты |
650—850 |
Для пайки коррозионно-стойких, конструкционных жаропрочных сталей, а также никелевых, медных, серебряных, латунных припоев (по данным С. Н. Лоцманова) |
|
АНГЛ |
62 В203; 16 Na2B407; 10 KF; 9 КВ507; 3 K2ZrF6 |
850—1260 |
Для пайки высоколегированных сталей. Температура плавления 720 °С (по данным Ю. И. Людвига) |
|
АНП2 |
68 В2Оэ; 20 Na2B407; 9 КВ508; 3 K2ZrC6 |
800—1100 |
Для пайки высоколегированных сталей. Температура плавления 650 °С (по данным Ю. И. Людвига) |
|
— |
90 буры; 2,2—2,8 NaF; 7,2—7,4 NaCl |
800—1150 |
Для пайки чугуна и латунных припоев |
|
Ф100 |
46,5 KBF4; 36,5 Na2B07; 13,5 W03; 3,5 Co203 |
900—1100 (/П„ = 500°С) |
Для твердосплавного инструмента (по данным Н. А. Клочко и др.) |
металлов и сплавов серебряными припоями с температурой плавления 600—850 °С. Для этого используют смеси борного ангидрида с фторидами или смеси тетраборатов с борным ангидридом и бурой.
Фториды взаимодействуют с большинством оксидов металлов при высокотемпературной пайке и потому используются как активный компонент, особенно если на поверхности паяемого металла присутствуют оксиды хрома и алюминия. Фториды часто добавляют во флюсы для увеличения жидкотекучести жидких боратов и улучшения заполняемости жидким припоем капиллярных зазоров.
Более активны флюсы из смесей борного ангидрида, буры, фторидов и фторборатов (особенно тетраборатов МЄ2В4О7; R20*2B203 и фторборатов [(BF4„Me]. При этом достигается высокая флюсующая способность и относительно слабое коррозионное воздействие остатков флюсов на паяное соединение. В качестве компонентов для флюсов пригодны следующие фтор - бораты:
1) BF4Me' или BF3*MeT, где Me' = Li, Na, К, Cs, Rb, NR4;
2) (BF4)2Me// или ^ВРз-Ме'Тг, где Me" = Cu, Са, Ва, Mg, Zn, Со, Pb;
3) (BF4)3A1 или BF3-A1F3.
Тетрабораты калия и натрия хорошо смачивают поверхность металлов и активно влияют на разложение их оксидов. Тетра- фторборат калия как компонент флюсов труднее диссоциирует, чем фторборат натрия, и потому он менее желателен в качестве компонента паяльных флюсов. Тетрафторборат калия был предложен как компонент флюсов для пайки хромистых коррозионно - стойких и жаропрочных сталей еще в 1976 г. Он пригоден также для пайки золотых и серебряных изделий. Нашли применение только некоторые смеси, содержащие борный ангидрид, буру, бораты и фториды, подобранные опытным путем (см. табл. 32, флюсы ПВ209 и ПВ284). Эти флюсы не образуют стекловидных шлаков и легко удаляются кипячением в воде или в 10 %-ном водном растворе лимонной кислоты. Флюс ПВ209 можно наносить перед пайкой в виде сухого порошка или пасты, замешанной на воде или спирте. При изготовлении пасты флюс вводят небольшими порциями в воду, так как при его растворении выделяется сравнительно большое количество теплоты. Нанесение сухого флюса ПВ209 на паяемый металл перед пайкой иногда приводит к его пригоранню. Поэтому лучше наносить свежий флюс непосредственно при пайке. Остатки флюса 209 после пайки способствуют коррозии паяных соединений, и их необходимо тщательно смывать в холодной, а затем в горячей проточной воде. Пайку с флюсами ПВ209 и ПВ284 необходимо проводить под приточно-вытяжной вентиляцией, так как тетрафторборат калия при нагреве до 750 °С распадается с образованием ядовитого газообразного фтористого бора BF3.
Фторид калия образует с 33 % NaF простую эвтектику с температурой плавления 700 °С. Флюс из смеси таких компонентов может быть изготовлен в виде пасты, замешанной на воде, спирте и четыреххлористом углероде.
Хлориды действуют аналогично фторидам, но имеют более узкий интервал действия и при более низких температурах, чем фториды.
Введение хлоридов во флюсы на фторидной основе понижает их температуру плавления. Хлориды имеют тенденцию окислять паяемый металл.
Щелочи — поташ и гидроокись натрия — используют для повышения температурного интервала активности флюсов; при этом даже следы влаги могут существенно уменьшать продолжительность действия флюса (его «живучесть»).
Среди высокотемпературных различают флюсы:
1) галогенидные (хлоридно-фторидные с температурными интервалами активности 400—625 °С и 600—1000°С);
2) с простыми и комплексными фторидами (с температурными интервалами активности 550—860 °С и 750—11 000 °С);
3) из фосфатов и силикатов с соединениями бора (с температурным интервалом активности выше 1000°С);
4) без соединений бора с фторидами и хлоридами; время действия флюсов обычно менее или равно 5 мин.
Составы важнейших флюсов и их ориентировочные температуры активности приведены в табл. 43, 44.
Флюсы ПВ209 и ПВ284 (ГОСТ 23178—78) первоначально были разработаны для пайки коррозионно-стойких сталей серебряными припоями, содержащими 40—45 %Ag при температуре 620—750 °С. Обнаружено, что при газопламенной пайке крупногабаритных изделий из латуней серебряными припоями с этими флюсами в паяных швах возникает значительное число пор и непропаев, снижающих герметичность соединений, а после удаления галтельных участков — ухудшающих микрогеометрию их поверхности. Подпайка дефектных мест увеличивает трудоемкость изготовления и снижает эксплуатационные характеристики изделий. В связи с этим разработан флюс «Салют 1» для газопламенной пайки латунных, в том числе крупногабаритных изделий [16].
Термографические, рентгеноструктурные и химические исследования флюсов ПВ209, «Салют 1» и их шлаков после переплава, после растекания их по латуни и меди, а также после пайки серебряными припоями показали, что в процессе нагрева флюсач ПВ209 происходят реакции между его компонентами с расплавлением образующихся продуктов:
2В204 + KF = KF • 2В20з, /Пл > 290310 °С;
KBF4 + 2В20з = BF3 + KF • 2В20з, /пл > 580 °С.
2KBF4 = BF4 + KBF5, /пл>580 °С.
При температуре 400—445 °С плавятся KF и KBF4. При температуре 500 °С во флюсе образуются простые и комплексные соединения фторидов, которые при дальнейшем повышении температуры растворяются в жидком флюсе. При нагревании до 750 °С и выше образуются комплексные соединения боратов.
Растекание жидкого флюса по поверхности латуни происходит с образованием четырех зон, различающихся по фазовому составу. Во второй зоне содержится больше соединений бора, чем в первой, центральной зоне. В результате окислительно-восстановительных реакций и обесцинкования поверхностных слоев латуни на них появляется слой чистой меди.
Как показали рентгенограммы шлаков, образовавшихся на поверхности латуни, подвергнутой предварительно флюсованию, и оксидов, образовавшихся на неофлюсованной поверхности, окисление металла под слоем флюса происходит более интенсивно, чем без него. Медь в контакте с флюсом окисляется в 2 раза быстрее, чем латунь.
Взаимодействие жидкого припоя с паяемым металлом, флюсом и компонентов флюса между собой способствует увеличению продуктов реакции. Изменение состава флюса в процессе его растекания и затекания в зазор между деталями ухудшает условия смачивания паяемого металла жидким припоем, а выделение газообразных составляющих BF3, Н2 и других в зазоре при недостаточно быстром их дрейфе в галтельные участки паяных швов способствует образованию газовых пор в шве.
Процесс флюсования при газопламенной пайке, таким образом, является сложным: при повышении температуры происходят различные электрохимические и химические процессы взаимодействия компонентов флюсов между собой и с парами воды, с оксидами и паяемым металлом, продуктов реакции между собой.
В начале нагрева на поверхности паяемого металла оксиды, образовавшиеся под действием паров воды из пасты флюса и газового пламени, переходят в гидрооксиды меди и цинка: Zn(OH)2 и Си (ОН) 2. При нагреве выше 80°С гидрооксиды разлагаются, что приводит к нарушению сплошности оксидной пленки на металле:
МеО + Н20(г) =Ме(ОН)2.
Расплав флюса через несплошности в оксидной пленке растворяет под ней паяемый металл вследствие преимущественного протекания процесса по термодинамически менее равновесным местам. В результате этого, как и при растворении паяемого металла в жидком припое, оксидная пленка диспергирует и переходит в расплав флюса с образованием комплексных соединений фторидов цинка в результате обмена катионами между фторидами щелочных металлов и диссоциированными оксидами цинка. Дальнейшее повышение температуры ускоряет этот процесс; медь и цинк восстанавливаются, взаимодействуют с компонентами флюса и при температуре 600 °С образуют соединения, растворимые во флюсе.
При дальнейшем повышении температуры до 700 °С из расплава флюса испаряются борный ангидрид и соединения BF3(BOF2), что приводит к выпадению избыточных комплексных соединений меди и цинка, диссоциирующих вслед за этим с образованием простых фторидов. Эти фториды взаимодействуют с парами воды, гидролизуются с образованием оксидов и фтористого водорода. При 700—800 °С появляются комплексные соединения боратов типа КгВзОіз, а ионы О2- и катионы К+ образуют высокоактивный оксид, который далее соединяется с борным ангидридом, а последний взаимодействует с оксидами меди и цинка, образуя с ними комплексные соединения. Все эти процессы активизируются в присутствии жидкого припоя. В результате этих процессов активность флюса понижается.
Состав шлаков после газопламенной пайки латуни с флюсом ПВ209 зависит от массы паяемых узлов вследствие ее влияния на продолжительность нагрева, степень завершенности процесса флюсования и снижения активности флюса. В шлаках этого флюса при пайке мелких деталей содержатся соединения KZn4F7 и Кз2гі2р7, которые отсутствуют в шлаках, образующихся при пайке более крупных и массивных изделий. Вместе с тем в шлаках появляются новые фториды K3C11F4, ZnF2, что характерно для более длительного процесса флюсования. Независимо от массы деталей в шлаках флюса ПВ209 после пайки латуни Л63 присутствуют оксиды ZnO и следы С112О.
Различие процессов флюсования меди и латуни состоит в том, что в последнем случае комплексные соединения фторидов не образуются: при более высоких температурах получаются простые бораты цинка и меди, которые гидролизуются парами воды.
Таким образом, непропаи при газопламенной пайке массивных изделий из латуни обусловлены большей продолжительностью процесса их нагрева и окисления, после чего активность флюса оказывается недостаточной и окисленные участки препятствуют равномерному смачиванию паяемого материала жидким припоем.
При газопламенном нагреве газовая пористость в шве возникает главным образом вследствие воздействия BF3, а также водорода и частично азота, попадающих в зону пайки из газового пламени. При этом применение слабовосстановительного пламени способствует некоторому снижению пористости в швах.
Флюс «Салют 1», основу которого составляют соединения Н3ВО3—KF -2Н20 с отношением 0,9, содержит также компоненты, препятствующие скоплению газов в зазоре, более эффективно4 защищающие паяемый металл от окисления и способствующие растворению оксидной пленки. Введение KNO3 во флюс «Салют 1» защищает металл от окисления и понижает число непропаев в шве. Установлено, что KNO3 защищает латунь в интервале температур 400—700 °С, но окисляет медь, начиная от 500 °С, и поэтому для высокотемпературной пайки меди флюс «Салют 1» не рекомендуется.
В процессе растекания состав флюса «Салют 1» не изменяется, газовые включения не образуются, что способствует затеканию припоя в зазор ровным фронтом; флюс имеет больший интервал температурно-временной активности, чем флюс ВП209.
При пайке с флюсом «Салют 1» величины зазора (0,01—0,5 мм) и нахлестки (2—5 мм) существенно не влияют на качество паяного соединения. Это обусловлено отсутствием в шлаках оксидов металлов. Температурный интервал активности флюса «Салют 1» при пайке с серебряными припоями составляет 650— 750 °С.
Остатки и шлаки коррозионно-активных флюсов-электролитов, имеющих pH <7, удаляют с поверхности паяного изделия путем тщательного промывания его в растворителях, например воде.
Введение во флюсы для пайки серебряных припоев 5 % Si02 в виде очень мелких частиц избавляет от необходимости просушки флюса перед пайкой.
Флюсы для высокотемпературной пайки алюминия. При высокотемпературной пайке алюминия используют флюсы следующих систем: 1) КС1—LiCl—NaCl—ZnCL2 (с добавкой фторидов); 2) КС1—LiCl—NaCl—ZnCl2 (CdCl2); 3) KC1—LiCl—NaCl (c криолитом или KF и A1F3); 4) KC1—NaCl—BaCl2.
Флюсы систем 1 и 2 относятся к реактивным; они нашли применение при пайке в печах (система 2), газопламенным нагревом и погружением (система /). Флюсы систем 3 и 4 — нереактивные — применяют в основном для пайки во флюсовых ваннах.
В процессе флюсования алюминия и его сплавов в расплавах систем 3 и 4 имеет место механизм электрохимического разрушения оксидной пленки на паяемом металле и твердом припое [24]. Поверхность окисленного алюминия в расплавах хлоридных и хлоридно-фтористых солей заряжена положительно. Поэтому на первой стадии флюсования на межфазной границе оксид — расплав флюса адсорбируются поверхностно-активные ионы — преимущественно анионы. Ионы А13+ из металла мигрируют через несплошности в слое оксида, обусловленные нестехиометрич - ностью его состава, к границе раздела его с флюсом под действием поля напряжением ~ 100 В при толщине пленки 100 нм. Оксидная пленка разрушается, когда стационарный потенциал алюминия Ест в расплаве флюса становится более положительным, чем потенциал активации Еа. При потенциале Еа галогениды вытесняют ионы гидрооксида с поверхности алюминия, препятствуя его электрохимическому окислению. При этом химическое сродство алюминия к кислороду уменьшается и становится меньше, чем сродство алюминия к иону С1“.
Условие Ест > Еа возможно при образовании в расплаве флюса аниона (ион F-), активно разрушающего оксид алюминия, и деполяризатора катодного процесса (комплексный катион
(A1F)2+). Последний возникает при термической диссоциации криолитовой группировки (A1F6)3~.
При пайке алюминия реактивными флюсами 1 и 2 (табл. 34) деполяризатором катодного процесса, по мнению Е. И. Сторчая, служат катионы солей тяжелых металлов, разряжаемые в дефектных местах оксидной пленки. Дефектные места образуются в оксидной пленке при нагреве (в условиях защиты ее от воздуха) вследствие разницы коэффициентов линейного расширения пленки и металла, присутствия в металле включений других фаз, скопления дислокаций на границе пленки с металлом из-за несоответствия параметров и структур кристаллических решеток оксидной пленки и металла. Нарушение сплошности оксидной пленки при флюсовой пайке происходит также под действием галогенидов, особенно ионов F~. Дальнейшее удаление оксидной пленки с алюминиевых сплавов интенсифицируется в результате ее диспергирования при твердожидком плавлении алюминия под ней в контакте с жидким припоем или с вытесненным из флюса тяжелым металлом.
Термическая стойкость флюсов системы КС1—LiCl—NaCl— AIF3 относительно мала вследствие образования легко гидролизующегося и летучего AICI3. По данным Е. И. Сторчая, такие флюсы могут быть стабилизированы при введении в них KF, подавляющего образование А1С1з. Наиболее термостойкие солевые системы, содержащие 4 % (п—KF—AIF3), с мольным отношением KF: AIF3 >► 2. Все флюсы для пайки алюминиевых сплавов коррозионно-активны.
Составы флюсов для пайки алюминиевых сплавов приведены в табл. 34.
Механизм действия флюсов реактивного класса, используемых для газопламенной и печной пайки алюминия и его сплавов, электрохимический; в данном случае деполяризатором катодного процесса являются катионы солей тяжелых металлов, которые разряжаются в дефектных местах оксидной пленки: Ме2+ +2е~ = = Ме. Возникновению дефектов в оксидной пленке алюминия способствуют ионы фтора, поэтому флюсы, кроме хлоридов, должны содержать некоторое количество фторидов металлов. При этом высаживающийся из солей легкоплавкий тяжелый металл на поверхности алюминия приводит к контактному твердожидкому плавлению паяемого материала, развивающемуся прежде всего по межфазной границе металла со слоем оксидной пленки, и отделению последней от подложки в местах нарушения ее сплошности (диспергация). Такой механизм активирования металла реактивными флюсами возможен при условии, если тяжелый металл, входящий в компоненты флюса, образует с алюминием монотек - тическую или эвтектическую диаграмму состояния с малой растворимостью алюминия в высаженном тяжелом жидком металле. Учитывая, что большинство флюсов в жидком состоянии являются электролитами, были развиты новые представления о механизме 164
|
Марка или номер флюса |
Состав флюса, % |
Температурный интервал активности, °С |
|||||||
|
NaF |
NaCl |
KF |
ZnCl2 |
LiCl |
ксі |
Другие компоненты |
Назначение |
||
|
Ф34А |
9—11 |
8—12 |
29—30 |
54—56 |
420—620 |
Для газопламенной пайки * |
|||
|
ФЗ |
10 |
— |
— |
— |
38 |
47 |
5 SnCl2 |
420—620 |
Для пайки в печи |
|
Ф5 |
10 |
— |
— |
— |
38 |
45 |
3 SnCl2; 4 CdCl2 |
420—620 |
То же |
|
ФВЗ |
8 |
— |
— |
— |
36 |
40 |
— |
450 |
Для пайки в печи с припоями на основе цинка |
|
1 |
12 |
4,6 |
0,1 ** |
34 |
44 |
5,3 A1F |
450 |
Для пайки в печи или погружением с припоями на основе А1 —Si |
|
|
2 |
60 |
ЗО |
610—620 |
Для пайки крупногабаритных конструкций с вертикальным зазором по замкнутому контуру |
|||||
|
Ф320 |
6 |
24 |
42 |
28 |
420—620 |
Для пайки нагружением во флюсовую ванну |
|||
|
Ф320 |
5 |
— |
— |
10 |
38 |
47 |
— |
560—620 |
То же |
|
17 |
— |
— |
— |
— |
41 |
51 |
8 карналлита |
560—620 |
» |
|
44—55 |
55—57 |
1 —10 фтор - цирконата калия или фтор- титаната калия |
480—615 |
» |
|||||
|
Ф435АП |
3—5 |
15—17 |
3—5 |
— |
23—25 |
49—51 |
3-5 A1F3 |
>570 |
Для пайки с погружением с припоем силумин |
|
— |
— |
8—12 |
4,6 |
— |
30—40 |
40—50 |
Si02 0,5—5 |
580—590 |
То же |
|
— |
5,4 |
12 |
4,5 |
0,1 |
34 |
44 |
A1F 5,4 |
580—590 |
|
|
20—40 |
60—80 дихлорида меди |
500—600 |
Для реактивно-флюсовой пайки при 500—600 °С |
|
* За исключением кислородно-ацетиленового пламени. ** ZnCl2 или CdCl2. |
флюсования алюминиевых сплавов при высокотемпературной пайке погружением в их расплавы.
При соприкосновении металла с электролитом происходит электрохимическое его растворение, т. е. переход положительных ионов металла в электролит. По мере накопления ионов металла в растворе начинается обратная реакция, обусловленная образованием отрицательно заряженной поверхности на паяемом металле по мере ухода с нее положительных ионов в электролит. При этом возникает разность потенциалов между металлом и электролитом, которая препятствует дальнейшему растворению металла. Такой двойной слой образуется практически мгновенно. Когда взаимодействие отрицательно заряженного металла и положительных ионов в электролите станет таким, что процесс ионизации (растворения) прекратится, наступит равновесие. Тем не менее, образование равновесного состояния на границе металл — электролит не означает прекращения процесса ионизации: при нем скорости реакции ионизации и обратного процесса лишь равны. При этом устанавливается равновесный потенциал между слоем свободных зарядов на поверхности металла и слоем заряженных ионов в растворе. Если при этом не протекает других реакций на границе металл — электролит, скачок равновесного потенциала зависит от концентрации ионов и температуры, определяется по уравнению Нернста (для обычной реакции элемента):
, RT, CcDd Ф = фо + -^1п-^г,
где R — газовая постоянная; a, b, с, d — концентрации реагирующих веществ и продуктов реакции; п — число электронов на один атом металла; F — число Фарадея.
При погружении металла в электролит, содержащий ионы и молекулы других веществ, последние могут также адсорбироваться на поверхности металла; при этом может протекать электрохимическая реакция, соответствующая данному равновесному потенциалу. Протекание этой реакции при условии, что ее равновесный потенциал отрицательнее водородного потенциала, может привести к расходу электронов и сдвинет потенциал металла в положительную сторону, т. е. поляризует его. Возврат в равновесное состояние может быть достигнут вновь при последующем растворении металла в электролите по реакции Ме-^Ме+ + е. При свободном протекании процесса растворения металла освобожденные электроны могут снова поглощаться при реакции восстановления водорода, т. е. процесс будет проходить непрерывно. При прекращении одной из этих электрохимических реакций процесс прекратится. Потенциал, который устанавливается на границе металл — электролит при непрерывном протекании процесса растворения металла и ассимиляции электронов деполяризатором, называют стационарным.
Деполяризация может быть обусловлена не только образовать
ниєм молекулы водорода, но и другими реакциями, протекающими на границе металл — электролит. В этом случае на этой границе могут накапливаться продукты реакции (коррозии), например оксиды металла.
По современным представлениям поверхность металла состоит обычно из непрерывно перемещающихся анодных участков, на которых происходит процесс окисления (потеря электронов) и переход металла в раствор по соответствующей реакции, например
А1 — 3 электрона->А13+ 3 электрона,
(металл) (ионы в растворе)
Для протекания этой реакции на катодном участке должен одновременно происходить процесс восстановления (приобретения электронов).
Выдвинуто положение [24], что активность флюса может быть оценена по значению стационарного потенциала и анодной поляризационной кривой. Поляризационная кривая представляет собой зависимость между значением равновесного потенциала для металла, погруженного в электролит, и соответствующим значением его поляризации і (рис. 28).
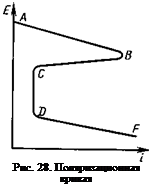 Эта кривая может иметь следующие характерные участки: АВ — участок активного растворения погруженного в электролит металла, ВС — неустойчивого и CD — устойчивого пассивного состояния металла и DF — участок нарушения пассивного состояния металла (пассивность торможения или предотвращение реакции). Разрушение оксидной пленки А120з ионами галлоидов в электролите происходит при увеличении скорости анодного процесса на участке DF. Таким образом, оксидная пленка на алюминии при погружении его в расплав электролита отсутствует или не защищает его на участках анодного растворения АВ и DF, а электролит при этом может играть роль флюса, если значение анодного разрушения оксидной пленки достигается при введении в солевой расплав активного иона, разрушающего оксидную пленку А1202, и при существовании во флюсе деполяризатора, достаточно активного для того, чтобы обеспечить условие £ст>
Эта кривая может иметь следующие характерные участки: АВ — участок активного растворения погруженного в электролит металла, ВС — неустойчивого и CD — устойчивого пассивного состояния металла и DF — участок нарушения пассивного состояния металла (пассивность торможения или предотвращение реакции). Разрушение оксидной пленки А120з ионами галлоидов в электролите происходит при увеличении скорости анодного процесса на участке DF. Таким образом, оксидная пленка на алюминии при погружении его в расплав электролита отсутствует или не защищает его на участках анодного растворения АВ и DF, а электролит при этом может играть роль флюса, если значение анодного разрушения оксидной пленки достигается при введении в солевой расплав активного иона, разрушающего оксидную пленку А1202, и при существовании во флюсе деполяризатора, достаточно активного для того, чтобы обеспечить условие £ст>
> Еа. Для большинства алюминиевых сплавов деполяризатором катодного процесса является растворенный в расплаве флюса кислород, а активным ионом — ион фтора F~.
Введение в расплавы хлоридов добавок KF и A1F способствует смещению стационарного потенциала сплава систе
мы А1 — Мп вследствие облегчения анодного процесса. Самопроизвольное разрушение оксида алюминия на поверхности паяемого алюминиевого сплава при добавках A1F3 происходит активнее, чем при введении KF. Активизирующее действие ионов фторидов обусловлено их способностью при определенном значении потенциала вытеснять кислород из оксида металла, вступая с ним в реакцию
Me-f-ttF_->MeFn
Термическая устойчивость расплавов флюсов, используемых для пайки погружением алюминия и его сплавов, является важной характеристикой, так как от нее зависят качество паяемых изделий и необходимая частота корректировки солевых (флюсовых) ванн. Как показали исследования [24], это, в частности, зависит от реактивной способности добавляемых в ванну фторидов. Так, например, в системе КС1—LiCl—A1F3 значительная часть A1F3 при нагреве до 620 °С в течение 60 ч переходит в другие соединения. Это обусловлено протеканием процесса гидролиза в расплаве флюса, приводящего к повышению температуры ванны и ее загрязнению. Поэтому в такую систему флюса необходимо введение стабилизаторов. Таким стабилизирующим компонентом, например, является KF, образующий с A1F3 криолит K3AIF6. Процесс гидролиза в расплаве КС1—LiCl—KF—A1F3 происходит главным образом благодаря наличию влаги солей. Для предотвращения потерь фторидов при гидролизе расплавы предварительно обезвоживают. Расплавы, содержащие криолит с модулем М = 2,4, имеют наибольшую термическую устойчивость.
В расплавах флюсов, содержащих фториды щелочных и щелочно-земельных элементов, оксидная пленка не растворяется. Удаление пленки А1203 определяется содержанием во флюсе химически связанной (в солях) воды. При взаимодействии алюминия с водой происходит реакция
2А1 + ЗН20 = А1203 + ЗН2.
Часть водорода сгорает на поверхности ванны, а часть реагирует с фтором по реакции
H2 + 2F = 2HF.
Этот газ через трещины в оксидной пленке проникает к поверхности алюминия, отделяя при этом оксидную пленку от металла, после чего она переходит в расплав. Экспериментально показано, что отсутствие влаги в расплаве флюса и образование HF предотвращают флюсование алюминия в расплавах нереактивных флюсов.
Для повышения термической стойкости нереактивного флюса при пайке погружением предложен его состав с повышенным содержанием KF (%): 23—25 LiCl, 15—17 NaCl, 3—5 KF, 3— 5 A1F3, 49—51 KC1 (см. табл. 34, флюс Ф435АП). Этот флюс отличается более низкой температурой начала активного действия (560 °С) и технологичен при длительной эксплуатации. При пайке с припоем, содержащим 6—8 % Si, временное сопротивление разрыву паяных соединений при 20 °С и при — 196 °С составляет соответственно 137 и 245 МПа.
Для сохранения активности флюсовой ванны в режиме холостого нагрева рекомендовано снижать ее температуру до —500 °С, а корректировку ванны производить путем введения недостающих компонентов после удаления из нее гидрооксидных соединений алюминия, образующихся при гидролизе и флюсовании.
Флюсовые расплавы системы КС1—LiCl—NaCl—A1F3 обладают малой термической устойчивостью, так как при их эксплуатации образуется летучее и легко гидролизующееся соединение A1F3. Для стабилизации термической устойчивости флюсов такой системы в них предложено вводить KF. Оптимальная термическая устойчивость такого флюса имеет место при содержании KF— A1F3 свыше 4% и при мольном соотношении KF/A1F3;>2. Содержание KF в аналогичных флюсах увеличивают до 6,3 % при следующем содержании других компонентов (%): 22—25 LiCl, 15—17 NaCl, 5,1—6,3 KF, 3—3,79 A1F3. Флюс технологичен при длительной эксплуатации и рекомендован к применению с припоем, содержащим 6,8—8 % Si; временное сопротивление разрыву паяных соединений, выполненных с указанным флюсом и припоем при температуре 26 °С и —196 °С, равно соответственно 137 и 245 МПа.
Для уменьшения расхода дорогостоящего и дефицитного компонента флюса для пайки погружением — соли лития — Е. И. Сторчаем и Н. С. Барановым предложен другой состав флюса (%): 39—42 СаС1, 39—46 КС1, 12—17 NaCl и 2—3 (NaF + + A1F3) или (LiF + AlF3). Температура плавления флюса свыше 530 °С. Он становится жидкотекучим при температуре 560 °С и почти не испаряется при нагреве вплоть до 700 °С. Введение СаС12 в расплав компонентов флюса обеспечивает более длительное поддержание необходимой концентрации ионов фтора в соляной ванне. При последующем взаимодействии кальция и фтора в расплаве, которое может происходить в течение одного — семи дней, флюс теряет свою активность. Добавки других фторидов обычно обеспечивают активность флюсовой ванны примерно в течение одного дня. Флюсы для высокотемпературной пайки алюминия погружением, содержащие СаС12, могут иметь составы (%): 1 (3,5— 3,2 NaCl; 34,2—51 CaCl 2; 27,5—32 LiCl; 2) 17—20 NaCl; 40— 45 КС1; 17—20 СаС12; 6—7 A1F3. Эти флюсы являются сплавами в области концентрационного треугольника КС1—СаС12—NaCl и пригодны для пайки металлов с припоями А1 —Si (в виде готовых форм или плакирующего слоя на паяемом металле).
В последние годы разработаны новые флюсы для высокотемпературной пайки алюминия и его сплавов; такие флюсы состоят из смеси фторидов с температурой плавления 562—600 °С. Пайка с этими флюсами возможна в среде чистого азота; в чистом водороде или диссоциированном аммиаке (с предварительным
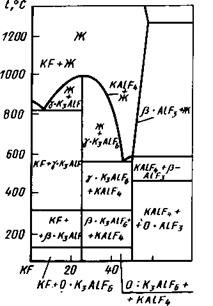
вакуумированием пространства печи до 9,806 Па). Основой флюсов является наиболее легкоплавкая эвтектика системы KF — A1F3 (рис. 29), состоящая из уКзАІРб и KAIF4. Флюс получил название «Ноколок» и применяется в виде пасты [33].
 Остатки флюса этого типа прочно сцепляются с паяемым материалом, но не вызывают коррозии паяного соединения, и на них могут быть нанесены лакокрасочные покрытия. Температура пайки с такими флюсами
Остатки флюса этого типа прочно сцепляются с паяемым материалом, но не вызывают коррозии паяного соединения, и на них могут быть нанесены лакокрасочные покрытия. Температура пайки с такими флюсами
_______ составляет 590—620 °С при-
60 ALFJfMon.% поем состава А1—8Si. Введение во флюсы до 4—20 % LiF позволяет паять с такими Рис. 29. Диаграмма состояния солевых флюсами Припоем, СОДержа-
расплавов системы KF—A1F3 ЩИМ более 50 % Zn.
Один из подобных флюсов содержит (мол. %) 30—55 A1F3; 35—60 KF; 20 фторида металла, например ZnF2, обладающего способностью высаживаться на паяемом металле (Заявка 58-159995 Япония, МКИ3 В 23 К 35/362). Кроме того, флюс может содержать до 25 % (мол.) одного или нескольких фторидов из группы LiF, NaF, PbF, CsF, MgF2, CoF, например ~ 1—5 % NaF,0,l —10 % LiF, 0,1—5 % CaF2 и <10% (NaFLiF + CaF). В подобные флюсы могут быть введены сложные фториды металлов K2LiAlF4, KA1F4, K2Zn2F2 как источники фторидов металлов KF—AIF3 или ZnF2. Флюсы могут содержать смесь нерастворимых в воде фторидно - алюминатных комплексов из А1, К, F, Li или их смеси с фторидом алюминия в форме простых соединений: 53—62 % A1F3, 35—44 % KF, 2—7 % LiF2 и 2 % примесей. Такие флюсы приготовляют путем сплавления исходных продуктов. Флюсы применяют в виде водной суспензии с 5—50 % сухого порошка флюса. Смывка остатков флюса не нужна, так как они не вызывают коррозии паяного соединения. Водная суспензия с 10 % сухого измельченного флюса наносится на паяемую поверхность предварительным распылением (Заявка 2119407 Англия, МКИ3 В23 К 35/362,ч В 23 К 1/04, НКИ С7М). Флюс этого типа в расплавленном состоянии хорошо смачивает алюминий. Состав флюса такого типа (мол. %): 32—35 A1F3, 42—65 KF и кроме KF еще один фторид щелочного металла из группы LiCl, NaF, PbF, CsF или MgF2, CaF2 в количестве 20 % (лучше 3—15 %) [71, 72].
Дозирование флюса и нанесение его перед пайкой. Во многих случаях дозирование флюса при пайке облегчает процесс последующего удаления остатков флюса и улучшает качество изделия (предотвращает попадание флюса на участки изделия, не подвергаемые пайке). При избытке флюса его остатки мешают затеканию припоя в зазор, а при недостатке флюса ухудшается процесс флюсования и могут измениться свойства флюса. Флюс при пайке дозируют различными способами: введением его в виде водного раствора, в смеси с порошком, зернами или стружкой припоя, иногда в виде таблетированной смеси с зернами припоя, в виде трубки припоя, заполненной флюсом-порошком. В трубчатых припоях весьма важно соотношение масс припоя и флюса. В трубчатых припоях ПОС 40 и ПОС 61, например, количество флюса составляет «2—2,5 % массы припоя. При пайке трубчатым легкоплавким припоем флюс и припой подводят при пайке одновременно, что облегчает процесс, особенно в труднодоступных местах конструкции, уменьшает потери флюса на 50 % и припоя на 20 % по сравнению с процессом пайки, при котором припой и флюс вводятся порознь. Применение трубчатых припоев во внутренней полости фасонного сечения или в нескольких каналах круглого сечения обеспечивает более равномерную подачу флюса. Внутренний диаметр трубчатого припоя обычно в 2 раза меньше наружного диаметра. Трубчатые припои изготавливают прессованием.
По данным Иозима Имира, для улучшения смачивания припоем поверхности периферийные каналы трубчатых припоев Sn—Pb иногда заполняют кристаллической канифолью, смешанной с 5—7 % хлоргидрата толуидина или другого активатора. Центральный канал заполняют жидкой канифолью, смешанной в равных долях с одним или несколькими активаторами: гликолевой, молочной, глутаминовой кислотами.
Проволока припоя может иметь вместо сквозных внутренних продольных каналов сплошные или прерывистые углубления с поверхности вглубь, заполненные флюсом. Такие углубления обычно направлены поперек оси проволоки и могут располагаться по спирали. Использование таких углублений для закрепления флюса на поверхности проволоки припоя предотвращает его выкрашивание при изгибе припоя (рис. 30). Длина углублений
|
Рис. 30. Варианты расположения флюса на прутке или проволоке припоя: 1 — припой; 2 — флюс (по данным С. Бернсдорфа и В. Рубела) |
^2 мм. Их наносят режущим инструментом или путем накатки. Подготовленную таким образом проволоку припоя погружают в жидкий флюс, заполняющий внутреннюю полость углублений, после чего снаружи проволоки стирают излишки флюса, затвердевающие в углублении. Для улучшения затекания флюса в углубления на поверхности проволоки перед погружением в жидкий флюс их заполняют быстро испаряющейся, хорошо смачивающей металл жидкостью, например спиртом.
Дозирование флюса почти полностью устраняет необходимость в трудоемкой операции удаления остатков продуктов флюсования после пайки.
По данным Утихаси Хисао, нашло применение дозированное флюсовое покрытие, наносимое с двух сторон ленты припоя. Наносимый флюс состоит из канифоли и синтетической смолы типа полихлорвинила, эпоксидной или фенольных смол, органических составляющих — аминосоляной кислотой и других органических кислот. В качестве связующего флюса служит смесь раствора канифоли в воде и натурального каучука.
По данным Тамада Минору, применение мелких зерен припоя с охлажденной на них тонкой пленкой флюса предотвращает окисление их поверхности в течение длительного времени.
Флюс может быть нанесен на места, подвергаемые пайке, также с помощью кисти или погружением в суспензию или эмульсию жидкой составляющей, в которой флюс нерастворим. Флюс может быть нанесен и в виде нестабильной пены (Пат. 4419146 США, МКИ3 В 23 К 35/36, НКИ 148/23) в аэрозольной упаковке.
Покрытие прутков или проволоки припоя может быть осуществлено в гидравлическом электрообмазочном прессе при пропускании их через фильтр, в котором происходит соосное соединение прутков и флюса в виде порошка, смешанного со связующим веществом. В качестве связующего в последнее время используют термопласты (этилен, пропилен, изобутилизопрен и др.). Опрессовку смеси производят при температуре термопластичного состояния, смесь выдавливается в кольцеобразное пространство между фильерой пресса и прутком. Термопласт при этом является и клеем и пластификатором; он может быть использован в виде крошек, гранул, порошка. Электрически заряженный порошок посредством электростатического поля наносят на паяемые кромки, предварительно смоченные водой или минеральным клеем. Деталь предварительно нагревают до 120 °С.
Флюс перед пайкой может быть нанесен путем распыления с помощью ультразвуковой установки [41]. Установка состоит из бачка с флюсом, вентилятора и раструба. Флюс из бачка поступает по трубке в наконечник, установленный в трубе. Выходя из торцовой поверхности наконечника, флюс распыляется, сбоку к трубе крепится вентилятор, воздушный поток которого подхва - тывет распыленные частицы флюса и через раструб направляет их к месту пайки. Размер частиц распыленного флюса ~ 10 мкм.
При автоматической пайке плат волной припоя для предварительного флюсования нашли применение флюсы в виде пены, состоящие из сосновой канифоли и высокомолекулярной синтетической смолы. Для этого жидкую канифоль под давлением сжатого воздуха пропускают через поропласт из синтетической смолы, имеющей поры диаметром 50—500 мкм. По другому способу вспенивающийся флюс, состоящий из флюсующей составляющей и испарителя (например, изопропилового спирта), пропускают через специальный пористый материал, в котором нагнетают воздух. Над насадкой образуется пенистая подушка, через которую пропускают собранные под пайку узлы. Устройство для получения пенистого флюса состоит из ванны с флюсом, установленного под ней, насоса и насадка. Флюс нагнетается в ванну через насадку с пористым материалом (Заявка 2042957 Англия, МКИ3 кл. ВЗР (В 23 К 3/00, В 23 К1/20)). Флюсовое покрытие может быть нанесено в виде эластичного опрессованного слоя, содержащего, кроме флюса, специальные компоненты, улучшающие смачивание, и компоненты, обедненные кислородом и повышающие прочность соединения. Такое покрытие применено на серебряных припоях. Для дуговой пайки сталей и медных сплавов в электротехнической промышленности использованы припои, помещаемые вместе с флюсом в трубку.
Применение серебряных припоев систем Ag—Си—Zn, Ag— Си—Zn—Cd, Ag—Си—Zn—Sn в виде прутков, заполненных флюсом, позволило понизить требования к точности подгонки и сборки под пайку.
 Опубликовано в Пайка металлов
Опубликовано в Пайка металлов Комментарии закрыты.