ЭЛЕКТРИЧЕСКИЙ ТОК В РАСТВОРАХ
 13 марта, 2013
13 марта, 2013  admin
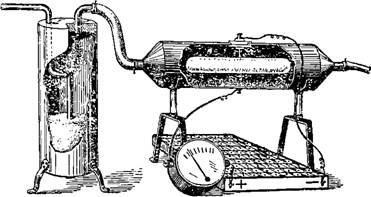
admin На рисунке 9 электроды аккумулятора были соединены, или, как говорят, замкнуты металлами — медными проводами и вольфрамовой спиральной проволочкой электрической лампочки. Присоединим провода, идущие от аккумулятора, к двум металлическим или угольным пластинам, опущенным в воду. В цепь включим амперметр—прибор, показывающий ток. Его стрелка будет стоять на нуле. Цепь разорвана, так как между пластинами находится изолятор — вода.
Так будет, если в сосуд, куда погружены пластины, налита химически чистая, то-есть не содержащая растворённых примесей вода. Но стоит прибавить к ней несколько капель соляной кислоты или щепотку соли, как стрелка амперметра отклонится. В цепи пойдёт ток. Вода, в которой растворена кислота, соль или щёлочь, уже не изолятор, а проводник.
Однако это совсем иной проводник, нежели металлы. В растворах движутся не электроны, а ионы.
Мы уже знаем, что молекула соляной кислоты состоит из двух ионов — водорода и хлора, связанных силой электрического притяжения. При растворении молекулы воды разрывают молекулу соляной кислоты на составляющие её ионы. Таким образом, в водном растворе соляной кислоты появляются положительные ионы водорода и отрицательные ионы хлора.
Такой распад молекул на ионы при растворении называется электролитической диссоциацией.
В чистой воде нет свободных зарядов. Поэтому электрическое поле не вызывает в ней тока. Но в воде, где растворена соляная кислота, находятся ничем не связанные ионы водорода и хлора. Под действием поля они приходят в движение. При этом отрицательные ионы хлора устремляются к положительно заряженной пластине — аноду, а положительные ионы водорода поле гонит к катоду. В растворе возникает упорядоченное движение зарядов — электрический ток.
Однако ток в растворе не похож на ток в металле. Вместо лёгких электронов здесь движутся в тысячи и десятки тысяч раз более тяжёлые ионы. Не один, а два потока зарядов образуют ток: поток положительных ионов, идущих к катоду, и поток отрицательных ионов, идущих к аноду.
Подходя к катоду, ионы водорода забирают у него недостающие им электроны и превращаются в атомы водорода. Ионы хлора отдают аноду свои лишние электроны и превращаются в атомы хлора.
В результате электроны, приходящие на катод из генератора электрического тока, уходят в раствор, а на анод выделяются электроны из раствора. В цепи идёт ток.
Таким образом, ионы как бы «перевозят» электроны через раствор, где электроны не могут двигаться самостоятельно. Правда, на аноде «высаживается» совсем не тот «пассажир», который «сел на ион» с катода. Но пассажиры эти все одинаковы. Сколько электронов приходит в секунду на катод от генератора, столько же уходит с анода обратно в генератор. Так поддерживается в цепи постоянный ток.
Образующиеся на катоде атомы водорода соединяются в молекулы водорода. Из молекул образуются пузырьки водорода, всплывающие и улетающие из раствора. Точно так же на аноде выделяется газ — хлор. Таким образом, в результате прохождения гока через раствор в растворе происходят химические процессы. Соляная кислота, которую мы растворили в воде, превращается в два газа — водород и хлор.
Электрический ток в растворах всегда сопровождается химическими превращениями. Здесь вместе с зарядами перемещаются и ионы растворённых веществ. Под действием электрического поля ионы, на которые распадаются молекулы, уходят: одни — к катоду, другие — к аноду. Поэтому вещества, входившие в состав молекул, разделяются полем и выделяются на различных электродах.
Тот же механизм прохождения тока можно наглядно показать на опыте, где носителем электрических зарядов служат не ионы, а хорошо видимые глазом частицы.
К двум металлическим цилиндрам, заключённым один в другой (рис. 10), подведены провода от аккумуляторной
|
Рис. 10. Электропроводность с применением пылинок в качестве носителей электричества. Внутренний металлический цилиндр служит катодом, внешний металлический цилиндр — анодом. |
Батареи; в пространстве между цилиндрами создано электрическое поле. Но тока в цепи нет, так как, подобно чистой воде, воздух, находящийся между цилиндрами, — изолятор; в нём нет свободных зарядов.
Начнём теперь вдувать в пространство между цилиндрами смесь пшеничной муки и порошка серы. Крупинки муки вследствие трения о металл заряжаются положительно, а крупинки серы — отрицательно. Попадая в поле, они ведут себя так же, как ионы в растворе. Крупинки муки притягиваются к катоду и забирают с него электроны. Крупинки серы идут к аноду и отдают ему электроны. Таким образом, электроны уходят с катода и появляются на аноде. Амперметр показывает, что в цепи идёт ток.
Раскроем установку. Внутренний цилиндр, служивший катодом, оказывается покрытым слоем муки. На внутренней поверхности внешнего цилиндра (анода) лежит слой серы. Ток разделил смесь муки и серы подобно тому, как он разделяет вещества в растворах.
Ионы могут перемещаться не только в растворах, но и в расплавах, а также в твёрдых телах. Однако движение ионов в твёрдом теле очень затруднено; заметные ионные токи возникают лишь при высоких температурах.
Выше мы говорили об электронах в твёрдых телах, отрывающихся от атомов благодаря тепловому движению. Такие тела являются электронными полупроводниками. По той же причине в некоторых твёрдых телах при высокой температуре отрываются от своих мест и ионы. Такие тела являются ионными полупроводниками. Обыкновенная каменная соль — типичный ионный полупроводник. Большинство твёрдых полупроводников имеет смешанную проводимость — и электронную и ионную.
Возьмём платиновую чашку, в которой находится иодистое серебро. Йодистое серебро было залито в чашку в расплавленном состоянии, а затем при охлаждении закристаллизовалось. Ещё до того, как оно затвердело, в него была опущена серебряная игла.
Подведём теперь к игле и к чашке провода от батареи. Амперметр покажет, что через кристаллическое иодистое серебро идёт ток. При этом игла служит анодом, а платиновая чашка — катодом.
Вытащим через некоторое время иглу и взвесим. Она оказывается легче, чем была до опыта. Внутри платиновой чашки мы обнаружим кристаллы металлического серебра. При прохождении тока часть серебра перешла с анода на катод. Это значит, что через иодистое серебро шёл не электронный, а ионный ток, перемещались ионы серебра.
Отрицательные ионы иода в иодистом серебре связаны гораздо прочнее, чем положительные ионы серебра. Поэтому перемещения их и выделения иода на аноде не обнаруживается.
В металлах электрические токи создаются только электронами, в растворах — только ионами. Твёрдые неметаллические тела ведут себя при низких температурах как изоляторы, а при достаточном повышении температуры приобретают некоторую проводимость, обусловленную высвобождаемыми теплом электронами и ионами.

 Опубликовано в
Опубликовано в