ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ СОСТАВА СМЕСИ ПРИ ПОСТОЯННЫХ ДАВЛЕНИИ И ТЕМПЕРАТУРЕ
 7 апреля, 2013
7 апреля, 2013  admin
admin Рассмотрим изотермическую реакцию в газовой смеси, представляя <ее состоящей из горючего А и окислителя В, объемные доли которых соответственно составляют Са и Св вне зависимости от состава этих двух частей.
Представляя такую реакцию бимолекулярной типа А + В и имея в виду, что Св=1—С а, согласно (5-18) скорость ее можно выразить следующим образом:
(5 21)
Заменив сомножитель р/ЯТ, представляющий собой согласно уравнению (4-11) число молей в единице объема, значением последнего, определенным как частное р/х, получим:
^ = *^С,(1-СЛ), (5-22)
Где (а, — молекулярная масса смеси, кг/моль; р — плотность смеси, кг/м3.
В процессе реагирования газов величина (а, изменяется сравнительно мало. Скорость реакции_ зависит в основном от сомножителей С_А (1 — С_а) . При изменении С А от нуля до единицы произведение Са(1—С а) увеличивается от нуля до некоторого максимума и снова 64
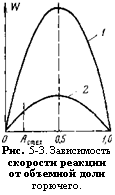
Стремится к нулю, обусловливая аналогичное изменение скорости реакции (рис. 5-3, кривая 1). Максимум скорости такой условной бимолекулярной реакции достигается при одинаковых концентрациях СА = СВ=0,5, т. е. в смеси стехиометрического состава.
|
Рис. 5-3. Зависимость скорости реакции от объемной доли горючего. |
 Рассмотрим теперь эту условную бимолекулярную реакцию при наличии инертного компонента, представляя его в качестве примеси к окислителю. Это имеет место, в частности, при использовании в качестве окислителя воздуха, который наряду с кислородом содержит азот, являющийся инертной примесью. Обозначим долю окислителя в смеси его с инертным газом через е, тогда доля окислителя в реагирующей смеси будет:
Рассмотрим теперь эту условную бимолекулярную реакцию при наличии инертного компонента, представляя его в качестве примеси к окислителю. Это имеет место, в частности, при использовании в качестве окислителя воздуха, который наряду с кислородом содержит азот, являющийся инертной примесью. Обозначим долю окислителя в смеси его с инертным газом через е, тогда доля окислителя в реагирующей смеси будет:
ЕСв = е(1 —СА).
Поэтому выражение для скорости реакции примет вид:
|
ЙС |
![]()
|
М |
![]() (5-23)
(5-23)
Т. е. скорость реакции в 1/е раз меньше, чем при отсутствии инертной примеси (рис. 5-3, кривая 2).
И в этом случае максимальная скорость реакции соответствует содержанию горючего вещества Са=0,5, концентрация же окислителя будет равна е (1—Са)=0,58.
Концентрация горючих в стехиометрическом составе смеси, определенная из следующих двух уравнений:
|
С |
![]() Составляет:
Составляет:
(5-24)
При наличии инертной примеси е<1 и поэтому САстех <0,5. С уменьшением е, т. е. с увеличением содержания инертной примеси, СаСТ(?х уменьшается. Это также приводит к уменьшению скорости реагирования в стехиометрической смеси, г. е. в смеси, которая требуется для полного выгорания горючих.
Таким образом, при постоянной температуре наличие инертной примеси не изменяет относительного содержания горючих, при котором скорость рассмотренной бимолекулярной реакции достигнет максимума, но уменьшает концентрацию реагирующих веществ, а следовательно, и скорость реакции. Наибольшая скорость реагирования получается не в стехиометрической смеси, необходимой для полного выгорания, а в смеси, обогащенной горючим веществом, что также приводит к уменьшению скорости реакции.
Аналогично изменяется скорость при изменении состава смеси и для тримолекулярных реакций.
Скорость тримолекулярной реакции типа 2А+В=М в случае, когда в окислительной части доля кислорода составляет е, согласно (5-19)
5— 541 65
|
|
|
Равняется: |
Скорость реакции достигает максимума при Са=2/3 вне зависимости от количества инертных газов.
Стехиометрический состав можно определить из уравнений
|
|
Совместным решением получаем, что концентрация горючих в стехиометрической смеси *
Так как е<1, Слстех <'2/3, т. е. стехиометрическая концентрация горючего в смеси с инертной примесью меньше, чем концентрация, при которой скорость реакции максимальна. Следовательно, и в этом случае наибольшая скорость соответствует обогащенной смеси.
Таким образом, при наличии инертной примеси скорость реакции уменьшается в результате уменьшения концентрации реагирующих веществ и вследствие того, что максимальная скорость горения отвечает обогащенной, а не стехиометрической сме - с и, которую для обеспечения полного выгорания горючих необходима иметь в процессе горения жидких и газообразных топлив с самого начала, а твердых — после обеспечения устойчивого зажигания.
В результате рассмотрения влияния инертной примеси на скорость изотермической реакции можно сделать два важных вывода.
В камерных топках парогенераторов подогрев потока горючей смеси, обеспечивающий ее воспламенение, осуществляется посредством рециркуляции горячих продуктов сгорания. Исходя из вышеизложенного, следует иметь в виду, что чрезмерная рециркуляция может ухудшить условия воспламенения в результате существенного понижения концентрации окислителя — кислорода и горючих компонентов. Поэтому зажигание горючей смеси целесообразно осуществлять посредством рециркуляции умеренного количества продуктов сгорания с возможно высокой температурой.
Из выражений (5-23) и (5-25) для скоростей реакции выше первого порядка следует, что если в смеси содержится небольшое количество одного из реагирующих веществ, то изменение концентраций других веществ в ходе реакции может быть относительно небольшим. Поэтому в этом случае реагирование можно рассматривать как процесс первого порядка относительно вещества, находящегося в недостатке.

 Опубликовано в
Опубликовано в