ГЕМИЦЕЛЛЮЛОЗЫ
 24 апреля, 2013
24 апреля, 2013  admin
admin Под гемицеллюлозами обычно подразумевают ту углеводную часть растительной ткани, которая в отличие от целлюлозы является более доступной воздействию разбавленных кислот и слабых растворов щелочей. Несмотря на явное несоответствие между понятием «гемицеллюлозы» и свойствами полисахаридов, объединенных этим названием, обладающих самыми различными свойствами и составом, термин «гемицеллюлозы» не только не утратил своего значения, но находит все более широкое распространение.
В понятие гемицеллюлоз входят полимерные углеводы с пятью и шестью углеродными атомами в основном звене. Общие формулы их (С5Н804)я и (С6Н10ОБ)я, где п — степень полимеризации. Первые называются пеню- з а н а м и, вторые — гексозанами. Пентозаны при гидролизе в присутствии минеральных кислот дают пентозы
(С5Н804)я+иН20 иСБН10О5
Гексозаны при гидролизе дают гексозы
(C6H10Os)„H-nH2O гаС6111206.
Пентозаны и гексозаны являются, следовательно, полимерными ангидридами пентоз и гексоз и носят родственные им названия. Так, например, пентозан, дающий при гидролизе ксилозу, называется ксиланом, дающий арабинозу—арабаном. Аналогично гексозан, дающий нри гидролизе ман - нозу, называется маннаном, дающий галактозу, галактаном и т. д. Существуют и комбинированные полисахариды. Так, например, полисахарид, при гидролизе которого одновременно получаются арабиноза и галактоза, называют арабогалактаном. В природе найден целый ряд различных комбинированных полисахаридов, таких как: арабоксилан, глю - команнан, галактоманнан, глюкофруктан и др.
Содержание гемицеллюлоз в спелой древесине довольно значительно и для различных пород колеблется в широких пределах (табл. 116) Г1].
Лиственные породы обычно содержат примерно в 1.5 раза больше гемицеллюлоз, чем хвойные. Больше гемицеллюлоз находят также в ветвях и вершине.
Гемицеллюлозы по количеству занимают значительное место в составе древесины (до 43%), однако биологическая роль их в жизни дерева еще окончательно не выяснена. Некоторые авторы [2] делят гемицеллюлозы по из назначению в растениях на конструктивные, входящие в состав клеточных стенок как склеивающий и строительный элемент, и резервные,
|
Таблица 116 Содержание гемицеллюлоз в древесине
|
Представляющие собой запасные вещества живого растения наряду с крахмалом. К сожалению, нельзя провести в настоящее время четкой границы между гемицеллюлозами и другими полисахаридами, в связи с чем понятие гемицеллюлоз приобретает известную условность.
Большая часть углеводов этой группы характеризуется меньшей по сравнению с целлюлозой устойчивостью к разбавленным кислотам. При нагревании с разбавленными щелочами гемицеллюлозы переходят из древесины в раствор; растворяются они и в холодной 4°/0 щелочи, но процесс идет медленнее. После извлечения гемицеллюлоз из древесины щелочью и осаждения из раствора спиртом, они становятся частично или даже полностью растворимыми в холодной или горячей воде.
Однако некоторую часть гемицеллюлоз очень трудно извлечь из древесины. Каким бы методом ни выделяли целлюлозу из древесины, в ней всегда содержится некоторое количество прочно связанных гемицеллюлоз. Таким образом, не все гемицеллюлозы легко гидролизуются; не все они легко и до конца извлекаются щелочью. Наиболее частыми спутниками древесной целлюлозы являются ксилан и маннан. В одной из сульфитных еловых целлюлоз, после ее полного гидролиза с помощью крепкой кислоты с последующей инверсией гидролизата, было найдено 13% гемицеллюлоз, в том числе 6% маннана, 4.5% ксилана и 2.5% фруктана (левулана). Прочно связанная часть гемицеллюлоз, остающаяся в сульфитной целлюлозе, оказывается так же устойчива к гидролизу разбавленными минеральными кислотами, как и сама целлюлоза. Причины того, что одна часть гемицеллюлоз способна легко удаляться из клеточных стенок, другая же оказывается более прочно связанной, исчерпывающе пока не разъяснены. Возможно, что часть гемицеллюлоз более доступна воздействию различных реагентов — более открыта и легко переводится в раствор, тогда как другая часть, по-видимому, вследствие более глубокого залегания ее или другого коллоидно-химического состояния, лучше защищена, и действие реагентов оказывается недостаточным для того, чтобы перевести ее в раствор. Кроме того, степень полимеризации гемицеллюлоз значительно меньше, чем целлюлозы, и составляет в среднем 100—200. Если эти короткие цепочки гемицеллюлоз попадают в ориентированные участки целлюлозного волокна, то эта часть гемицеллюлоз оказывается трудно гидроли - зуемой. Легко гидролизуемы, по-видимому, те гемицеллюлозы, которые находятся либо отдельно от целлюлозы, либо в аморфной ее части. Трудно гидролизуемые гемицеллюлозы, прочно связанные с целлюлозой, получили название целлюлозанов [48]. Целлюлозаны, как считают, состоят из коротких цепей гемицеллюлоз, совместно ориентированных с длинными цепями целлюлозы, в состав которых входят главным образом ксилан и маннан. При гидролизе древесины целлюлозаны могут гидролизоваться лишь совместно с целлюлозой, так как трудногидролизуемая целлюлоза защищает от гидролиза и цепи целлюлозанов. Имеются указания на то, что целлюлозаны представляют ту часть фракции технической целлюлозы, которую обычно называют |3- и у-целлюлозой PJ, и состав которой, помимо ксилана и маннана, входят и другие гемицеллюлозы. Так, при исследовании щелочерастворимых фракций сульфитной и сульфатной целлюлоз содержание (3-целлюлозы составило 3—7 % от исходной целлюлозы, в которой было найдено 20—54% ксилана, 12—15% маннана, 7% арабана и 2% галактана (от веса фракции) [4].
В другой работе [41] методом хроматографии на бумаге было показано что а-целлюлоза из сосновой вискозной сульфатной целлюлозы содержит 2% гемицеллюлоз и 98% целлюлозы, |3-целлюлоза — 4% гемицеллюлоз и 96% целлюлозы, а у-целлюлоза — 49% ксилана, 46% маннана и только 5% целлюлозы.
Методом фракционного диализа [42] через полупроницаемую мембрану с ионообменной смолой из щелочных экстрактов целлюлозы была выделена р-целлюлоза с СП в интервале 20—200 и у-целлюлоза с СП 4.
При этом ксилан был главным углеводом, найденным в выделенных гемицеллюлозах. Определено, что холодная щелочная экстракция более эффективна (при облагораживании целлюлозы) для удаления ксилана, чем маннана.
Установлено I44], что общий выход гемицеллюлоз для сульфатных целлюлоз (из березовой древесины) выше, чем у сульфитных. Наиболее высокий общий выход гемицеллюлоз из сульфатных целлюлоз получается при экстракции 10%-м NaOH; для сульфитных — при экстракции 10 и 18% NaOH — одинаковый. В среднем величины СП сульфатных гемицеллюлоз (130—160) примерно в 2 раза выше, чем у сульфитных гемицеллюлоз (60-90).
Природные гемицеллюлозы березы имеют СП около 200.
Многие исследователи [®] указывают, что гемицеллюлозы состоят не только из полимерных ангидридов пентоз и гексоз, но что кислотный гидролиз гемицеллюлоз, помимо моносахаров, дает еще некоторое количество уроновых кислот типа
СНОН—СНОН—СНОН—СНОП—СН—СООН
Такие уроновые кислоты образуются за счет той части гемицеллюлоз, цепи которых содержат звенья с карбоксильными группами. Важнейшими уроновыми кислотами являются гексуроновые кислоты (с 6 атомами углерода): p-D - глюку р оновая, |3-/)-маннуроновая и a-D-галактуроновая.1
Г Принадлежность моносахарида [6] к £>- или Л-ряду обычно устанавливают, сравнивая расположение атома водорода и гидроксила у последнего асимметрического атома углерода с расположением их у правовращающего и левовращающего
I--------
НО—С—Н I
Н—С—ОН
I
Но—с—н I
Н—С - I
Соон
|
О |
Р-О-глюкуроновая кислота
Соон
-V -маннуроновая кислота
НО—С—н
I
|
О |
НО—С—н I
Н—С--------
СООН a-D-галактуроновая кислота
Приводятся доказательства [7], что гексуроновые кислоты являются продуктами окисления гексоз в результате образования промежуточного альдегида — 6-альдо-гексозы по схеме
Сно соон
|
6-альдогексоза |
Гексуроновая кислота
Глицеринового альдегида — простейшего оксиальдегида с одним асимметрическим атомом углерода
|
И—С—ОН |
СНО СНО
НО—CI_H I
|
СНоОН |
|
Сно |
—I 1
|
СН2ОН |
|
СН2ОН I-глицериновый альдегид |
|
D-глицериновый альдегид/ |
О форме связи 1 и р судят по расположению полуацетального гидроксила при первом углеродном атоме и гидроксила у последнего асимметрического углеродного атома. В а-форме расположение полуацетального гидроксила такое же, как гидроксила у асимметрического углеродного атома, определяющего принадлежность к D- или к L-ряду. В p-форме — обратное. При обозначении а-формы моносахаридов D-ряда полуацетальный гидроксил обычно пишут справа, а у (з-формы D-ряда слева. Б случае Z-ряда, наоборот, у ct-формы полуацетальный гидроксил пишут слева, а у (3-формы — справа
|
"но-с£н_ н-с-он но-с-н I и _Н-с-он I ~~ Н-"с---------------------- Сн^он-~ Р - D - глюкоза |
|
I_ н-с-рн_ н—с-он но-с-н |
|
О |
|
Н-С-ОН I 1—-I-------- ] — LH-CzrZ-- снгон Et-D - глюкоза |
Таким образом, из (3-.0-глюкозы может образоваться (З-О-глюкуроно - вая кислота, из р-£)-маниозы р-/)-маннуроновая кислота и т. д. Однако вопрос этот еще окончательно не разрешен.
|
Таблица 117 Содержание уроновых кислот в древесине европейских пород (в % от веса древесины)
|
|
СООН Н X--------- Ом |
|
Н, со |
|
СООН T /--- Он |
|
Нчсо |
|
Н Но -о- |
|
Л" �Н НА Ч------ /н |
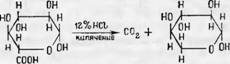
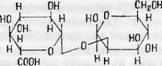
Одной из важнейших реакций уроновых кислот является их декар - боксилирование, протекающее легко при нагревании с минеральными кислотами и приводящее к образованию углеводов с меньшим числом углеродных атомов, например
|
|
|
P-D-глюкуроновап кислота |
|
P-D-ксилоза |
Количество отщепляемой С02 пересчитывается на уроновые кислоты по эквивалентным весам.
Н. И. Никитин и Авидон [г] получили следующие данные о содержании уроновых кислот в некоторых породах древесины (табл. 117). Как видно из табл. 117, исследованные лиственные породы содержат примерно в два раза больше уроновых кислот, чем хвойные.
Несмотря на малое содержание в древесине уроновых кислот, они имеют важное значение. Благодаря содержанию карбоксильных групп уроновые кислоты обладают большой ли - офильностью и, присутствуя в целлюлозных волокнах в небольших количествах, оказывают положительное влияние на размол массы.
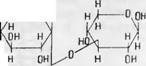
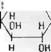
Более тщательные исследования состава уроновых кислот показывают, что почти все они содержат метокеиль - ные группы, большей частью связанные сложно-эфирной связью. Имеются, однако, указания на существование метоксильных групп, находящихся в простой эфирной связи. Большим шагом вперед в этой области явились работы Джонса с сотрудниками [8], которые идентифицировали 4-метил-/)-глюкуроновую кислоту в гидролизате осиновой древесины (подробно об этом см. в главе «Пентозаны»), Это соединение было найдено раньше в некоторых древесных камедях [9] и недавно в гидролизатах древесины ели, эвкалипта, березы и других пород I10]. Найденная 4-метил-/)-глюкуроновая кислота является составной частью альдобиуроновой кислоты и оказалась связанной с ксиланом по приведенной конфигурации[46]
Гемицеллюлозы камеди сливы, например, состоят из остатков L-араби- нозы, D галактозы, D-маннозы и />-глюкуроновой кислоты в соотношении 3:2:1 : 1 и дополнительно содержат около 3% ксилозы. В одной из фракций гидролизатов этих гемицеллюлоз были выделены галактоза и альдо - биуроновая кислота, состоящая из остатков D-глюкуроновой кислоты и D маннозы со связью 1—2
|
|
Нельсон и Шюрх I"] показали, что основная часть уроновых кислот березы образована галактуроновой кислотой, бариевая соль которой осаждается спиртом. Глюкуроновая кислота в свободном виде не обнаружена. Ее присутствие было обнаружено в вид< 4-метил-/)-глюкуроновой кислоты в соединении с />-ксилозой: Тимелл I12] исследовал состав гемицеллюлоз целого ряда древесин лиственных и хвойных пород. В древесине лиственных пород аш найдено (от веса древесины): 1% галактана, 2—3% маннана, 0.5% арабана и 16—25% ксилана. В древесине хвойных: 1—2%- галактана, Ь—13% маннана, 1 — 1.5% арабана и 4—7% ксилана. В гидролизатах из всех пород древесины идентифицированы моно - и биуроновые кислоты и следы метилированных кислот. Общее содержание уроновых кислот, по данным этого автора, у всех пород оказалось почти одинаковое (3—4%). Другим автором [13] было показано, что уроновые кислоты почти полностью извлекаются при сульфитной варке древесины сосны, ели, березы и осины, Предполагают [1в], что имеется связь между способностью гемицеллюлоз к растворению и содержанием в них уроновых кислот. Однако считают [15], что 4-метилглюкуроновая кислота сопутствует как технической, так отчасти и беленой целлюлозе в виде так называемых кислых ксиланов и относится в большинстве случаев к трудногидролизуемым гемицеллюлозам.
Природными источниками уроновых кислот являются также некоторые полисахариды, в которые уроновые кислоты входят как структурные элементы. Например, глюкуроновая кислота является структурной единицей многих слизей (мукополисахарицов), всех камедей за исключением камеди трагаканта (в которой содержится а-£>-галактуроновая кислота), специфических полисахаридов микроорганизмов, природных глюкозидов, сапонинов и т. д. [16]. Галактуроновая кислота является структурной единицей пектиновых веществ, содержащихся в растительных соках, в плодах яблок, груш, лимонов, в мясистых корнях свеклы, моркови и т. д. Маннуроновая кислота является составной частью альгиновых кислот, содержащихся в больших количествах в бурых океанских водорослях [17]. Некоторые уроновые кислоты, в частности глюкуроновая кислота, играют важную роль в «защитных функциях» животного организма: многие ядовитые вещества, попадающие в организм, образуют глюко - зиды глюкуроновой кислоты или сложные эфиры и выводятся с мочой.
Все вещества, в структурные единицы которых входят уроновые кислоты, являются аморфными веществами, нерастворимыми в крепком спирте. Многие из них растворяются в воде или в едких щелочах, аммиаке, соде. При смачивании и набухании эти вещества делаются клейкими, скользкими или желатинообразными. Все дают окрашивание с рутениевой красной и положительную пробу с нафторезорципом на уроновые кислоты Большим достижением в области методов исследования ряда сложных полисахаридов, особенно в выяснении их строения, необходимо признать применение методов качественной и особенно количественной хроматографии [1в]. С успехом применена хроматография для анализа гемицеллюлоз - ных гидролизатов, для разделения продуктов расщепления метилированных полисахаридов (с применением селективных растворителей). Широко используется метод фракционирования гемицеллюлоз путем последовательного растворения холоцеллюлозы в едких щелочах или медноаммиачных растворах постепенно увеличивающейся концентрации, раство рами соды, водой и другими растворителями.
Холоцеллюлозой называют весь углеводный комплекс древесины, за исключением лигнина. В холицеллюлозу входят — целлюлоза, пентозаны, гексозаны и уроновые кислоты. Было замечено, что, если подвергать древесину попеременной - обработке влажным хлором и смесью спирта с пиридином, лигнин хлорируется, окисляется и переходит в раствор, в результате чего в остатке получается вся углеводная часть древесины почти в неизмененном состоянии, которую и назвали холоцеллюлозой. Холоцеллюлозу в дальнейшем стали получать и другими методами: удаляла-лигнин из неизмельченной древесины чередующимися обработками слабыми растворами двуокиси хлора и сульфита натрия, попеременной обработкой опилок влажным хлором и 3%-м раствором моноэтанол шина в 95%-м спирте. В настоящее время чаще применяют метод делигнификации растительной ткани хлоритом натрия в уксуснокислой среде и делигнификации древесины с перуксусной кислотой, СН3—СО—О—ОН (которая в свою очередь получается из уксусного ангидрида и перекиси водорода), а также метод удаления хлорированного лигнина диоксаном [1S]. Выход холоцеллюлозы составляет в среднем для древесины хвойных пород — 70—73 %, для древесины лиственных —- 72—79 %. Холоцеллюлоза является хорошим объектом для фракционирования и изучения состава отдельных фракций гемицеллюлоз. Гемицеллюлозы из древесины, где они присутствуют вместе с лигнином, удаляются щелочью труднее и более загрязненными, чем из холоцеллюлозы [20]. Так, например, холоцеллюлоза, выделенная из древесины дуба (действием хлорита натрия), с выходом 67% от веса древесины, содержала пентозанов 29.2% (от веса холоцеллю лозы), уроновых кислот 8.6%; холоцеллюлоза из пихты белокорой с выходом 66%, содержала пентозанов 7.1%, уроновых кислот 4.8%, маннана 14.4%; из пихты сахалинской — с выходом 70%, содержала пентозанов 8.8%, уроновых кислот 3.8%, маннана 12.7% и, наконец, холоцеллюлоза из ели аянской, с выходом 71%^ содержала пентозанов 6.1%, уроновых кислот 3.0%, маннана 8.7%. Содержание лигпина во всех полученных холоцеллюлозах составляло 0.2%- (от веса холоцеллюлозы) [21]. Однако имеются указания [22], что в некоторых случаях лучше проводить извлечение гемицеллюлоз непосредственно из растительного материала щелочью во избежание деструкции полисахаридов.
При выделении гемицеллюлоз без использования щелочи (путем водных экстракций предварительно размолотой холоцеллюлозы на вибромельнице) исследователи [47J исключают потери ацетильных групп. С помощью этого метода удалось выделить из ели и березы в среднем 12—15% гемицеллюлоз содеря:ащих связанные ацетильные группы. Выделенные отдельные фракции гемицеллюлоз из ели содержали при этом около 4.7—4.8% связанных ацетильных групп, а отдельные фракции гемицеллюлоз из березы — 12.7—12.9%.
Изучение холоцеллюлозы приводит к интересным выводам, имеющим юлыное практическое значение. Было показано t1], что холоцеллюлоза «держит на 2.6% больше а-целлюлозы, чем целлюлоза, полученная по кроссу и Бивену, и на 13.4% больше, чем соответствующая целлюлозная пасса. Таким образом, холоцеллюлоза является источником для получения Зольших количеств а-целлюлозы высокой вязкости, пригодной для производственных целей. Специально приготовленные листы из осиновой холоцеллюлозы, полученной с выходом свыше 70% (тогда как выход сульфитной или сульфатной целлюлозы составляет лишь 40—45%), дали хорошие показатели механических испытаний.
Холоцеллюлоза, выделенная из соломы, картофельной ботвы, травы эспарто, стеблей подсолнечника, табака и других растений, дает выход целлюлозы примерно на 10% выше, чем при получении ее другими способами. Поэтому в последнее время встает вопрос о получении холоцеллюлозы в промышленности I28].
Как известно, одним из наиболее распространенных углеводов в растительном мире является крахмал, относящийся к основным резервным питательным веществам I24]. Он содержится в семенах и плодах в виде постоянного запаса, за счет которого питается зародыш растущей ткани наряду с другими питательными веществами, такими как протеины, яшры и органические фосфаты. Крахмал содержится в вегетативных частях растений, в клубнях, живых клетках сердцевины, коры корней и стволов, а также в млечном соке некоторых растений и — в переходной форме — в зеленых листьях.
В частях растений, где крахмал отлагается как постоянное запасное вещество, количество его может быть достаточно велико. Для некоторых видов семян или зерен содержание крахмала доходит до 70%. В клубнях орхидей, корнях и сердцевине стволов некоторых пальм содержание крахмала определено в 25—30%. Оналичии крахмала в древесине имеется чрезвычайно мало данных. Для определения крахмала пользуются его способностью извлекаться горячей водой, гидролизоваться под влиянием некоторых ферментов: диастаза, такадиастаза и амилазы слюны. Зерна крахмала, окрашенные раствором йода в синий цвет, можно видеть под микроскопом в живых клетках древесной паренхимы и сердцевинных лучей. Найденное в исследуемой древесине содержание крахмала приведено в табл. 118.
Было показано, что крахмал, выделенный из древесины дуба и орешника, осахаривается такадиастазой медленнее, чем крахмал картофеля. Этот крахмал состоит на 90% из остатков глюкозы, остальные 10% представляют смесь глюкозы, ксилозы и глюкуроновой кислоты, частично метилированной. Крахмал был также обнаружен в древесине тоноля, лимона и заболони акации. При апализе выделенных из этих древесин гемицеллюлоз была получена монометилглюкуроновая кислота в сочетании с £>-ксилозой. Кроме того, было определено, что в цепи выделенного кислого ксилана имеются ангидроглюкозные группы. Возможно, что последний продукт обязан происхождением крахмалу, примешанному к гемицеллюлозам. Содержание крахмала в древесине зимой и летом не одинаковое. Считают, что содержание крахмала достигает дважды максимума и дважды минимума, а именно, откладываясь в течение лета, он достигает первого максимума осенью перед опаданием листьев; позже от начала сентября и до ноября происходит убыль крахмала, вместо которого появляется сахар. У одних пород эта смена идет полностью — крахмал зимой совсем исчезает, так что в плазме можно видеть только масло: это породы маслянистые, к которым принадлежат — липа, береза, наши хвойные. У других крахмалистых
пород (дуб, клен, вяз, ясень) содержание крахмала зимой в древесине только несколько уменьшается и он совсем исчезает лишь из коры, переходя в сахар. Вследствие этого у всех деревьев зимою наступает в древесине первый минимум крахмала.
Ранней весной, перед распусканием почек, наступает второй крахмальный максимум. Второй минимум крахмала наступает поздней весной с момента начала роста побегов, когда крахмал, превращаясь в глюкозу, транспортируется к тронувшимся в рост побегам. Отложение крахмала начинается у основания ствола, спускается вниз в корень к более молодым его
|
Таблица 118 Содержание крахмала п древесине разных пород
|
Частям, а затем поднимается
Вверх к ветвям. Так i;ai крахмал образуется из сахара, притекающего из листьев по лубу, то сначала им заполняются клетки луба, затем по клеткам сердцевинных лучей заполнение распространяется на живые клетки древесины и сердцевины.
Крахмал является одним из важнейших продуктов фотосинтеза, образующегося на весьма ранних стадиях этого процесса.
С физиологической[47] точки зрения, фотосинтез!25]— это процесс углеродного питания растений с первичным образованием органических веществ из С02 и Н20 и с накоплением в них энергии солнечного света, поглощаемого хлорофиллом.1 Непосредственный фотосинтетический ап парат растений, т. е. место, где протекают основные реакции фотосинтеза, где образуются продукты фотосинтеза, —- это хлоропласт.[48] Именно в хдо - ропластах или на их поверхности образуются первично при фотосинтезе такие вещества как углеводы и крахмал, которые, согласно классическому представлению, и являются прямыми продуктами фотосинтеза. Между основной фотохимической реакцией фотосинтеза и реакцией образования нервого продукта восстановления С02 (например, глицеринового альдегида), а тем более углеводов, лежит сложная цепь энзиматических реакций, которые могут совершаться в растениях и в процессе вторичных превращении углеводов, без участия фотосинтетического аппарата. Тем не менее
углеводы и крахмал считаются прямыми продуктами тогда, когда они первично образуются в хлоропластах. Фотосинтетический аппарат— это прежде всего аппарат для снабжения растений универсальным и однообразным питательным материалом — углеводами. Помимо образования углеводов (играющих первенствующую роль), фотосинтетический аппарат образует и другие важные продукты, меняя их состав и качество в зависимости от вида растений, их состояния и условий роста.
Как оказалось, в фотосинтезе исключительно важную роль играют фосфаты Сахаров.
На синтез сахарозы
|
НгС- 0Р03н2 |
|
С=0 |
|
НС-ОН (I) |
|
(Ш) НгС-0Р03Нг |
|
НгС-0Р03Нг/ |
|
С=о / / |
|
Н„С—ОН |
|
Нгс-он; с=о J |
|
НгС-0РО3Н |
|
L нс-он 05) v0h |
|
(X) |
|
Но |
|
0Р03нг |
|
НгС-ОР03Н2 (vrai |
|
0Р0,Н« |
|
НС-ОН I НгС-0РО3Нг |
|
Нс=о I Нс-он I Нс-он нс-он I HjjC-OPOjHg Нгс-0Р03Н2 |
|
НС = 0 I Нс-он I Нс-он I Н2с-оро3нг |
|
С=о I -с—н I Нс-он I Нс-он нс-он |
|
С=о I |
|
Но-сн I Нс-он I Не-он I Нс-он I Н„с |
|
(К) |
/
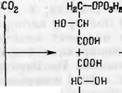
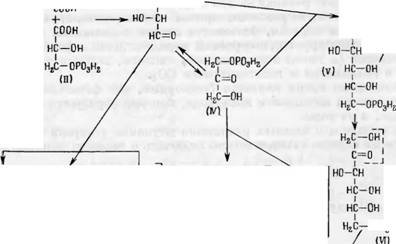
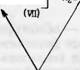
Ассимиляция углекислоты и углеродный фотосинтетический цикл представлены на схеме (по Кельвину) [26]. Акцептором С02 является ри- булезо-1,5-дифосфат (I), который при действии карбоксидисмутозы (через гипотетический промежуточный продукт R—Н + С02 -> R — СООН) дает 2 молекулы 3-фосфороглицериновой кислоты (II). Восстановление последней (II) дает 3-фосфороглицериновые альдегиды (III), (IV), которые под влиянием альдолазы дают фруктозо-1,6-дифосфат (V), частично гид- ролизующийся в фруктозо-6-фосфат (VI), на который действует транске - толаза. Остаток гликолевого альдегида переносится на (III) с образованием рибулезо-5-фосфата (XI). Остаток (VI) в виде фосфата тетрозы (VII) конденсируется с диоксиацетонофосфатом (IV), образуя седогептулезо-1,7- дифосфат (VIII). Последний частично дефосфорилируется в седогептулезо-7- фосфат (IX), который путем транскетолазной реакции ( с III) превращается в смесь рибозо - и рибулезо-5-фосфатов (X, XI). Фосфорилирование (XI) дает (I), вступающий в следующий цикл, ассимилируя С02. Из 11 промежуточных продуктов этого цикла 10 являются фосфатами Сахаров, из которых многие в значительной степени дециклизованы. Акцептор С02- 1,5-рибу - 25 П. и. Никитин
лезо-дифосфат обладает строением, полностью исключающим циклизацию.
Реакция восстановления фосфороглицериновой кислоты до триозы с образованием рибулезодифосфата, как полагают, требует наличия света, а превращение рибулезодифосфата в фосфороглицериновую кислоту через реакцию карбоксилирования света не требует.
Каждая стадия в этой схеме, как показано, контролируется определенной ферментативной системой. Согласно этим представлениям, Я-фосфорогли - цериновая кислота, первый доказанный продукт реакции, образуется при взаимодействии 1,5-дифосфата рубулезы, С02 и воды.
Иные представления о фотосинтезе развивает Варбург [40]. По его мнению, фотосинтез включает световую и темновую реакции; в первой из них каждая молекула хлорофилла образует одну молекулу кислорода, при темновой же реакции —-2/3 образовавшегося на свету. кислорода вступают в обратную реакцию, причем вновь регенерируются «входные вещества. Таким образом, фотосинтез связан с дыханием. По Варбургу, углекислота фиксируется, по крайней мере, частично в виде а карбоксила глутаминовой (а также аспарагиновой) кислоты, которая тем самым участвует в связывании и восстановлении С02-
В настоящее время является бесспорным, что фотосинтез у растении сопровождается выделением кислорода, который образуется не из двуокиси углерода, а из воды.
Все процессы с момента вхождения двуокиси углерода в растение до завершения синтеза Сахаров можно включить в валовую реакцию фотосинтеза
6С02 + 6Н20 С6Н1206 + 6 02.
Часто пользуются сокращенным уравнением
С02 + Н20 { СН20 } + 02,
Где {CH2U} — обобщенное звено углеводной цепи [27].
В процессе фотосинтеза в атмосферу поступает кислород, обеспечивающий дыхание всего живого на земле, с другой стороны — синтезируются углеводы, которые сами по себе являются пищей, а кроме того, в переработанном состоянии дают белки, жиры, витамины i; другие питательные вещества, возникающие в растительном организме при длительном превращении углеводов в общем обмене веществ уже без участия света, исключительно в результате «темновых» ферментативных реакций.
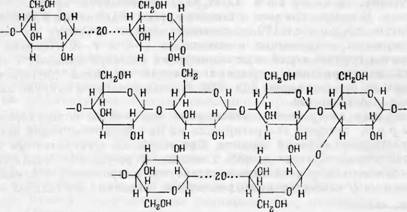
Крахмал не является химически индивидуальным веществом [4С].. По своим свойствам и химическому составу он различается как в одном и том же растении, так особенно в различных растениях. Удельный вес крахмала в среднем 1.5. Углеводная часть крахмала (96—97-%) состоит из двух полисахаридов, различающихся по своим физиррским и химическим свойствам, — амилозы и амилопектина. Амилоза легко растворяется в теплой воде и дает растворы со сравнительно невысокой вязкостью. Амилопектин растворяется в воде лишь при нагревании под давлением и дает очень вязкие растворы. Амилоза различного происхождения имеет молекулярный вес в пределах 32 ООО—160 ООО и даже выше, что соответствует наличию, в молекуле от 100 до 980 глюкозных остатков. Молекулярный вес амилопектина равен 100 000—1 000 000, что соответствует степени ролимериза - ции 600—6000. В настоящее время большинство исследователей, считает [25], что амилоза и амилопектин равномерно распределены во внутренних а внешних участках крахмальных зерен. Амилоза дает интенсивно синее окрашивание с раствором йода, амилопектин с йодом дает желто-бурый цвет. Содержание фосфора (который в виде остатков фосфорной кислоты связан в крахмале с некоторыми глюкозными остатками) в амилозе очень мало — до 0.03%, в амилопектине значительно выше — 0.20—0.22%. В молекуле амилозы остатки a-D-глюкопиранозы связаны глюкозидными связями в положении 1—4 по типу непрерывной цепи
Н он н он н он
|
|
Снгон сн2он снгон
В молекуле амилопектина a-Z^-глюкоииранозные остатки соединены глюкозидными связями не только в положении 1—4, но периодически в положении 1—3 и 1—6, образуя разветвленную структуру
|
|
Содержание фракций амилозы и амилопектина в крахмале, выделенном из различных растений, различно: от 15 до 25°/0 амилозы и от 75 до 85% амилопектина [28J.
Вещество, родственное крахмалу, содержащееся в печени и других тканях высших позвоночных как запасной углевод, называется гликогеном или животным крахмалом. Гликоген отличается от крахмала тем, что в его молекуле отсутствует линейная фракция. Он еще более разветвлен, чем амилопектин, не образует зерен, .D-глюкопиранозные остатки соединены в положении 1—4, 1—3 и 1,6 глюкозидными связями. Недавно гликоген был найден в тканях растений: маисе, синезеленых водорослях, в грибах, дрожжах, в зернах сахарной кукурузы и др.
В некоторых растениях крахмал заменяет инулин. Инулин представляет собой полимер фруктозы, растворимый в воде и высаживающийся спиртом из водных растворов. При гидролизе инулин образует фруктозу. Молекула инулина построена примерно из 30 (j-D-фру ктофу рано злых остатков,[49] связанных глюкозидной связью в положении 1—2. Приводятся
доказательства, что в инулине имеются также a-D-глюко пир анозные остатки [2В|.
Строение инулина может быть схематически изображено следующим образом [39, стр. 458]
О—...
..—О—СН2 О-
V
/
СНОН о
СНОН О СНОН о
I I II II
|
-СН2 О- V |
|
-СП, |
СНОН—СН—СИ2ОН СНОН—СН—СН2ОН СНОН—СН—СН.-ОН
Инулин содержится в больших количествах в клубнях земляной груши и георгина, в корнях одуванчика, кок-сагыза и цикория, в артишоках, в корнях, листьях и стеблях каучуконосного растения гваюлы (Parthenium Argent Alum). В этих растениях инулин является запасным питательным веществом, заменяющим крахмал. В отличие от инулина (состоящего примерно из 30 фруктофуранозных остатков) в стеблях ржи был найден дифруктозид, р-л е в у л и н С12Н22Ои, являющийся кристаллическим веществом. В исландском мхе, а также в других видах мхов и в лишайниках содержится л и х е и и н [80], состоящий подобно крахмалу из остатков глюкопиранозы, соединенных в положении 1—4 и 1—3. Лихенин легко извлекается горячей водой, при охлаждении раствора выпадает в осадок. Степень полимеризации отдельных фракций лихенина достигает 500, в среднем же она составляет 265—365. При нагревании в вакууме лихенин образует левоглюкозан.
В морских водорослях — ламинариях был найден полисахарид л а - м и н а р и н, который экстрагируется из них баритовой водой или слабыми растворами соляной кислоты. При гидролизе минеральными кислотами ламинарии образует до 98% глюкозы. В результате метилирования и последующего гидролиза было показано, что макромолекула ламинарина построена из D-глюкопиранозных остатков, связанных ацетальной связью
|
Многоатомных Л |
|
Альдегидо - или кетояоспир- |
Полуацетали С=0
Альдегидная
|
Римолекулярные тов [6] |
|
С^-ОН | ОН Н—С—ОН |
|
Н—С—ОН I I По—С—Н +ЩО НО—С—н I I Н—с—он |
|
II—с—он I Сн2он Гидрат (промешут< >чная форма) |
Форма (D-гдюкоза)
Но- I
-н2о но—С—Н
Окисные формы моносахаридов обычно рассматриваются как производные гетероциклических соединений: шестичленные — как производные пирана, а пяти - членные — как производные фурана. Таким образом, фруктофуранозой будет называться пятичленное окисное кольцо фруктозы, а глюкопиранозой — шестичленное окисное кольцо глюкозы.
|
П |
Степень полимеризации ламинарина составляет в среднем 73. Приводятся доказательства, что в молекуле ламинарина имеются также связи в положении 1—6, образующие боковые цепи с разветвленным строением [31], а также, что в ламинарине присутствуют остатки. D-маннозы [32].
За последние годы наметился значительный прогресс в промышленном использовании гемицеллюлоз. Как известно, в настоящее время целые отрасли промышленности основаны на химической переработке гемицел- люлозных компонентов растительной ткани. К их числу могут быть отнесены: производство фурфурола, этилового спирта, кормовых дрожжей, производство кристаллической ксилозы, триоксиглутаровой кислоты, пятиатомного спирта ксилита. Осуществлено получение из гемицеллюлоз (при помощи окислительных и восстановительных реакций) таких органических соединений, как метилглиоксаль, эритроновая и глицериновая кислоты, глицерин, гликоль, пропиленгликоль, а также ряда других продуктов. При использовании щелоков вискозного производства (содержащих гемицеллюлозы) была получена «алюмогемицеллюлоза», обладающая противокоррозийным свойством [33].
Интересно отметить положительное влияние легко набухающих гемицеллюлоз на размол бумажной массы и формование листа. Гидратация, например, холоцеллюлозы происходит много быстрее, чем целлюлозной массы, содержащей меньшее количество гемицеллюлоз. Механическая прочность бумаги, полученной из холоцеллюлозы, оказывается весьма большой. Однако холоцеллюлоза, содержащая большое число низкополимерных гемицеллюлоз, оказывается менее прочной, так как низкополимерные продукты обладают меньшей клейкостью. При удалении только низкополимерных гемицеллюлоз прочность листа значительно повышается. Приводятся экспериментальные данные, подтверждающие положительное влияние гемицеллюлоз на повышение прочности бумаги, особенно в мокром состоянии [34].
Влияние гемицеллюлоз на прочные свойства бумаги, полученной из древесно-целлюлозного волокна, было темой серьезного изучения многих лет ряда авторов [43].
|
В положении 1—3. Сильное отрицательное удельное вращение в щелочных растворах указывает на наличие р-связи |
Было исследовано влияние прибавления различных гемицеллюлоз к отбеленной еловой сульфитной целлюлозе с высоким содержанием а - целлюлозы [35]. Например, гемицеллюлозы осины, изолированные из холоцеллюлозы щелочью, ксилан, полученный из шелухи овса, галакто - маннан из гумми белой акации (рожкового дерева) и альгинаты Na — все оказывают на свойства бумаги сходное действие. Прочность бумаги повышается до максимума при добавлении в пределах 10% вышеуказанных гемицеллюлоз. Наиболее ясно выражено влияние галактоманнана и ксилана. Добавление 10% ксилана увеличивало разрывную длину на 47%, продавли - вание на 58%, удлинение на 55%. При небольших добавках галактоманнана (~1%) действие было более эффективно, чем при добавках такого же
количества ксилана. Ксилан оказывает больший эффект при добавках выше 2.5%. Гемицеллюлозы осины уступают ксилану по величине эффекта, по-видимому, из-за сильно разветвленной их структуры и высокого содержания уроновых кислот. Ксилан и гемицеллюлозы осины благоприятно действуют на размол, а галактоманнан и альгинаты натрия ухудшают его. Особое внимание обращено также на использование гемицеллюлоз из отходов древесины (получаемых с лесозаготовок и всех видов механической переработки древесины) [36]; отходов сельского хозяйства: хлопковой шелухи, подсолнечной лузги, кукурузной кочерыжки и другого непищевого сырья [37].

 Опубликовано в
Опубликовано в