ХИМИЧЕСКАЯ КОРРОЗИЯ МЕТАЛЛОВ
 13 апреля, 2013
13 апреля, 2013  admin
admin Химическая коррозия - самопроизвольное взаимодействие металла с коррозионной средой, при котором окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Как и любая химическая реакция, этот вид коррозии носит временной характер. Окислителями (корродирующими агентами) могут быть сухие газы (02, С02, S02, HCl, оксиды азота и др.), перегретый водяной пар, жидкости, не являющиеся электролитами, а также расплавы органических и неорганических веществ, в том числе металлов. Наиболее часто химической коррозии подвергается металлургическое оборудование, сопла реактивных двигателей, детали газовых турбин и двигателей внутреннего сгорания, оболочки ракет и космических кораблей, т. е. изделия, работающие при высоких температурах.
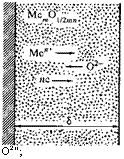
Из разновидностей химической коррозии обстоятельно изучена газовая коррозия. Механизм ее сводится к росту оксидных пленок на поверхности металла. Выделяют ряд стадий, протекающих последовательно и параллельно (рис. 5.2). Например, в случае двухвалентного металла такими стадиями являются:
1) ионизация металла и переход его ионов и электронов из металлической фазы в оксид:
Ме —► Ме2+ + 2е;
Рис. 5.2. Схема роста оксидного слоя на металле при газовой коррозии
2)
|
О2"; |
 Перемещение ионов Ме2+ и электронов в слое оксида;
Перемещение ионов Ме2+ и электронов в слое оксида;
3) адсорбция кислорода на поверхности пассивного оксидного слоя:
МеО + 02 —► МеО 120адс;
4) ионизация адсорбированного кислорода и перемещение образующихся ионов в слое оксида:
Оад с + 2е ►
5) рост оксидного слоя:
|
МеО. |
![]() Ме2+ + О2"
Ме2+ + О2"
Скорость роста оксида лимитируется скоростью диффузии реагирующих компонентов в слое, причем процесс идет с автоторможением. Последнее объясняется увеличением толщины диффузионного слоя и меньшей проницаемостью образующихся при окислении высших оксидов по сравнению с низшими.
Если металл образует с окисляющим компонентом среды несколько устойчивых соединений, то получаются многослойные оксидные пленки с размытой границей между слоями. Меньшая степень окисления, естественно, приходится на слои, непосредственно примыкающие к металлу. В целом оксидный слой можно рассматривать как комплекс слоев последовательно расположенных соединений металла и компонентов внешней среды. Например:
Для железа Бе I БеО I Ре304 I Ре203 I 02
Для марганца Мп I МпО I Мп304 I Мп203 I 02
Различные металлы обладают разной стойкостью к химической коррозии; большое влияние оказывает и состав среды (рис. 5.3).
Хром проявляет высокую стойкость ко многим средам, в том числе и окисляющим; напротив, химическая стойкость железа при высоких температурах (800 °С и более) низка. Константа скорости коррозии, как и любой реакции, определяется уравнением Аррениуса:
К = АеШк1
Где Е- энергия активации (теплота) химической реакции.
Продукты химической коррозии (окалина и другие соединения) обладают повышенной хрупкостью и склонны к растрескиванию вслед-
Рис. 5.3. Диаграмма газовой коррозии металлов при 700 °С за 24 ч
Ствие возникающих внутренних (в основном, термических) напряжений. В процессе разрушения металла при химической коррозии наблюдается также образование газовых пузырей в окисленном и граничащем с металлом слое.
Защита металлов от химической коррозии в основном заключается в их легировании добавками элементов, более стойких к окислению. Защита легированием основана на образовании соединений: а) с малой дефектностью кристаллической решетки, обладающих низкими коэффициентами диффузии по отношению к корродирующему агенту; 6) с кристаллической решеткой шпинелей (типа двойных оксидов), обладающих повышенной химической стойкостью. Наиболее эффективными легирующими добавками, сообщающими железу жаростойкость, являются хром, титан, молибден, вольфрам, алюминий, тантал, ниобий. Благодаря их применению созданы коррозионностойкие стали для реактивной, ракетной, атомной и другой техники.
Эффективность лакокрасочных покрытий в борьбе с химической коррозией ограничена их низкой термостойкостью. При невысоких температурах (300-500 °С) они, однако, могут защищать металлы за счет теплоэкранирования или химического (восстановительного) действия. Так, если нагревать изделия из стали с полиамидным или по - лиакрилонитрильным покрытием, пигментированным алюминиевой пудрой, то сталь под пленкой остается блестящей, пока полностью не разрушится покрытие; непокрытый металл в этих условиях заметно окисляется.

 Опубликовано в
Опубликовано в