ОСОБЕННОСТИ НАПЛАВКИ МЕДИ И БРОНЗ НА СТАЛЬ
 10 марта, 2014
10 марта, 2014  admin
admin По данным Г17], в системе Fe—Си, как следует из диаграммы Fe—Си (рис. 34), установлено наличие двух перитектических реакций: 1) б-твердый раствор (6,7% Си) + жидкость (10,3% Си)"^. ^.у-твердый раствор (8,3% Си) при 1478°; 2) у-твердый раствор (~8% Си) + жидкость (97,2% Си) X є-твердьга раствор (96% Си) при 1094° С, и одного эвтектоидного процесса: у-твердый раствор (4% Си) a-твердый раствор (-—-1,4 % Си) + е-твердый раствор (—98,5% Си) при 850° С.
При комнатной температуре в равновесном состоянии сплавы меди с железом представляют собой твердый раствор меди в железе (а); твердый раствор железа в меди (е) и смесь твердых растворов (а + є). Следует отметить, что хотя теоретически растворимость меди в железе при температуре ниже 650° С очень небольшая в действительности при комнатной температуре в твердом растворе с a-железом могут находиться значительные количества меди. Максимальная растворимость меди в у-железе составляет: 8,3% при 1478° С; 7,5% при 1484° С; —8,0% при 1430° С и —7,5—
8,5 % при 1094° С. Растворимость меди в a-железе составляет —0,9% при 800° С; 0,5% при 750° С и 0,3% при 700° С. С дальнейшим понижением температуры растворимость меди в железе снижается и составляет при 450° С 0,15 ± 0,02% [17]. Растворимость железа в меди почти линейно уменьшается от 3,8% при 1094° С до 0,3% при 800° С. При температуре 200° С следует ожидать растворимости порядка 1,27-10_5% [17].
В указанной работе отмечается, что в железо-медных сплавах при таких низких температурах равновесного состояния достичь невозможно. Этому способствуют высокие скорости охлаждения, получаемые как при термообработке медистой стали, так и при
сварке, которые не обеспечивают состояние равновесия. Согласно [60], благодаря инертному выделению. меди из твердого раствора а в структуре нормализованной и отожженной медистой стали, содержащей медь даже в количестве 1 — 1,5%, включения структурно-свободной меди не наблюдаются, так как при свободном охлаждении на воздухе (или даже в печи) медь не успевает выделиться из твердого раствора с a-железом, в результате чего фиксируются структуры, отвечающие пересыщенному медью твердому раствору без следов свободной меди.
Г. А. Кащенко [38] считает, что в практических условиях выделение железа из твердого раствора не обнаруживается даже Т.°С г -
|
L |
"Г —1 / |
і528° /Л 77° -9 |
|||||||
|
Г |
ж. р) |
> |
-ч |
||||||
|
/ |
/ |
||||||||
|
/ |
|||||||||
|
'I |
|||||||||
|
109< |
|||||||||
|
V |
|||||||||
|
V |
|||||||||
|
833°------ |
|||||||||
|
Г |
759° |
|
1509 1400 1300 1200 1100 Си W00 900 800 W0 |
|
906° ■Р 759° |
|
10 20 30 40 50 50 70 80 90 100 fe, % Рис. 34. Диаграмма состояния бинарной системы железо—медь |
при содержании его в меди до 2% и объясняет это медленным распадом и исключительной дисперсностью выделений. Наличие высокодисперсных частиц железа в меди подтверждается и в работах Е. С. Шпичинецкого и И. JI. Рогельберга, изучавших влияние небольшого содержания железа на свойства меди и «-латуней. В работе [104] указывается, что причина торможения роста зерна железосодержащих сплавов вызвана именно высокой дисперсностью частиц второй фазы, которые, оттесняясь в процессе рекристаллизации к границам зерен, механически препятствуют их росту.
В условиях сварки процесс кристаллизации протекает настолько быстро, что растворившееся в жидкой меди железо может не успеть выделиться из твердого раствора с медью и останется в виде пересыщенного твердого раствора с медью. Поэтому, как показали проведенные исследования, даже при наличии в металле наплавки до 2—2,5% железа включения структурно-свободного железа не наблюдаются. Это очень важно, так как коррозионная стойкость и другие физико-механические свойства металла наплавки существенно зависят от наличия в нем структурно-свободного железа.
На растворимость меди в железе и железа в меди оказывают влияние находящиеся в них легирующие элементы и примеси.
Углерод не растворяется в меди. Примесь углерода, находящаяся в стали, несколько уменьшает растворимость меди в твердом железе и создает ограниченную растворимость в жидком состоянии.
Марганец, образующий с медью непрерывный ряд твердых растворов, увеличивает растворимость меди в железе [20]. Это объясняется тем, что марганец увеличивает внутрикристаллит - ную растворимость меди в железе. Образуя с железом твердый раствор замещения, марганец снижает критическую точку А3, расширяет область у-твердого раствора. Растворимость же меди в у-твердом растворе выше, чем в a-твердом растворе. Кроме того, медь с марганцем имеют значительную взаимную растворимость, что способствует внутрикристаллитной диффузии.
Кремний хорошо растворяется в меди. Максимальная растворимость кремния в меди составляет 6,7% при температуре 726° С. С понижением температуры растворимость кремния в меди падает, составляя при комнатной температуре 3—4%. Железо в медно-кремниевых сплавах растворяется ограниченно [20]. Кремний оказывает существенное влияние на механические свойства сплава. Основное влияние кремния на механические свойства обусловлено, по-видимому, упрочнением зерен твердого раствора, а также его раскислительным действием ввиду высокого сродства к кислороду.
Сера и фосфор несколько увеличивают растворимость меди в железе, так как увеличивают межкристаллитную диффузию. Помимо растворимости железа в меди и меди в железе образованию прочной металлической связи между медью и железом способствует ряд близких физико-химических СВОЙСТВ меди и железа, особенно таких, как радиус атома, параметр кристаллической решетки, тип решетки и др. В табл. 11 сопоставлены важнейшие физико-химические свойства меди и железа.
Вместе с тем целый ряд факторов затрудняют наплавку меди и ее сплавов на сталь. Основными из них являются [96]: 1) значительное сродство жидкой меди к кислороду; 2) большая растворимость газов, особенно водорода, в жидкой меди; 3) высокая тепло - и электропроводность меди и др. Тем не менее процесс соединения меди и ее сплавов со сталью протекает успешно.
В ряде работ показана возможность электродуговой сварки меди со сталью и наплавки меди и ее сплавов на сталь [9, 13, 27, 74, 89, 108 и др.]. В зависимости от требований, предъявляемых к соединению, могут применяться те или иные способы сварки или наплавки.
|
Важнейшие физико-химические свойства меди и железа
|
Металл наплавки должен быть без дефектов, снижающих прочность изделия, а иногда и плотность. Такими дефектами могут быть поры, раковины, трещины. Поры в меди и ее сплавах при наплавке на сталь могут образоваться в результате взаимодействия жидкого наплавляемого металла с газами. Газы, особенно водород, обладают большой растворимостью в жидкой “меди [96]. Растворившийся в жидкой] меди водород взаимодействует с'кисло - родом меди:
Н2 - f- Cu20 = 2Cu - f - H20.
Аналогично взаимодействует с кислородом меди и окись углерода:
СО + Cu20 = 2Си + С02.
Водяные пары и углекислый газ не растворяются в меди, а стремятся выделиться из нее, образуя в ней при выходе поры, а иногда и трещины [96].
Водород может образовывать в меди поры, не вступая в реакцию с кислородом. На образование пор влияет не столько абсолютная величина растворимости водорода в меди, сколько значение коэффициента диффузии водорода в твердой меди - По данным [96], коэффициент диффузии водорода в твердой меди составляет при 1000° С 3,9-10‘6 мл Н21мм-см*-сек, тогда как коэффициент диффузии водорода в твердом железе составляет при 1500° С 1,22-10мл Н2/мм-см2-сек. В результате такой малой скорости диффузии в меди остающийся после затвердевания жидкого металла водород может покинуть металл путем диффузии и де-' сорбции через поверхность наплавки.
Как указывалось выше, жидкая медь обладает значительным сродством к кислороду. В процессе наплавки образуются растворы закиси меди в жидкой ванне, благодаря чему активность жидкой меди по отношению к кислороду увеличивается. Твердая медь почти не растворяет закиси меди. Поэтому в процессе кристаллизации активность меди по отношению к кислороду, а следовательно, и стойкость соединений кислорода резко снижается. Закись меди выделяется в виде самостоятельной фазы в составе эвтектики Си—Си20. Образующаяся эвтектика обволакивает кристаллы меди, вызывая хрупкость и трещины в металле наплавки.
По данным [88], стойкость металла наплавки против образования трещин снижается и при высоком содержании железа в металле наплавки. Поэтому способ и режим наплавки должны обеспечивать отсутствие попадания в металл наплавки кислорода, водорода и других газов, а также минимальный переход железа из основного металла в металл наплавки.
Во многих случаях металл наплавки должен обладать высокой коррозионной стойкостью, которая зависит как от количества железа в нем, так и от того, в каком виде железо находится в этом
металле. Когда железо находится в сплаве в твердом растворе либо распределено в нем в виде мелкодисперсных частиц, коррозионные свойства сплава не нарушаются. По данным [104], коррозионная стойкость меди и латуней при содержании в них железа до 0,5% не нарушается, т. е. остается такой же, как и у чистого сплава.
Наличие в металле наплавки участков с обособившимися включениями железа приводит к резкому понижению его коррозионной стойкости, коррозия в таких местах протекает наиболее интенсивно.
|
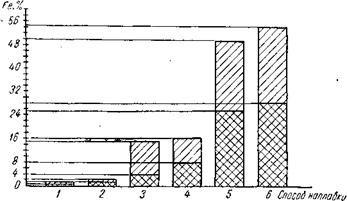
Рис. 35. Содержание железа в первом слое металла наплавки в зависимости от способа и режима наплавки: 1 — наплавка плазменной струей с токоведущей присадочной проволокой; 2 — наплавка расплавлением облицовок; 3 — автоматическая наплавка под слоем флюса ленточным электродом; 4 — наплавка лежачий электродом под слоем флюса; 5 — ручная наплавка электродами «Комсомолец»; 6 — автоматическая наплавка под слоем флюса электродной проволокой; S — минимальное содержание Fe; S — максимальное содержание Fe |
Таким образом, для получения металла наплавки с высокой коррозионной стойкостью необходимо свести содержание железа в нем до минимума и, главное, не допустить получения в металле наплавки структурно-свободного железа. Содержание железа и то, в каком состоянии оно находится в металле наплавки, определяются способами и режимами наплавки (рис. 35).
В случае применения способов наплавки, при которых основной металл расплавляется, происходит перемешивание расплавленной стали с жидкой медью, а также протекают физико-химические процессы на межфазной границе, вследствие чего в металл наплавки переходит большое количество железа (как указывалось выше, от 4 до 55—60%) и, естественно, оно будет находиться в структурно-свободном состоянии в виде отдельной фазы. Такая наплавка, как будет показано ниже, обладает низкими эксплуатационными свойствами.
В случае наплавки плазменной струей основной металл в процессе наплавки не расплавляется. Переход железа в металл наплавки при отсутствии расплавления стали осуществляется только в результате физико-химических процессов, протекающих на межфазной границе. Поэтому для получения металла наплавки с низким содержанием железа необходимо уметь управлять физико-химическими процессами, которые протекают на межфазной границе.
 Опубликовано в Плазменная наплавка металлов
Опубликовано в Плазменная наплавка металлов Комментарии закрыты.