ГЕКСОЗАНЫ
 25 апреля, 2013
25 апреля, 2013  admin
admin Главнейшими представителями гексозанов являются маннан, дающий при гидролизе маннозу, и галактан, дающий галактозу. Менее изучен левулан (фруктан) и глюкан. Распространены в растительном мире также гексозаны смешанного типа: глюкоманнан, фруктоманнан, арабогалактан, галактоманнан, глюкофруктан, манногалактан, манно - арабогалактан, гдюкоарабан и др.
Гексозаны являются ангидридами гексоз, молекулы которых химически связаны между собой в виде цепей (более коротких, чем цепи целлюлозы); иногда такие цепи имеют разветвленную структуру. Пространственное расположение водородных атомов и гидроксильных групп в цепях гексозанов обусловливается конфигурацией простейших Сахаров, входящих в состав данного полисахарида
С—п I
Н— С—ОН I
Но—С—II I
Б-глюкоза
НО—с—н
НО—С—н I
Н—с---------
Р - D - глюкопираноза
С—н I
НО—С—н I
НО—с— н I
D-манноза но—с—И I
НО—с—н I
НО—с—н I
Н—с---------
СН2ОН P-D-маннопираноза
|
/О С—н I Н—с—он I Но—с—н I Но—с—н I Н—с—он СН2ОН D-галактоза |
|
НО-С—н I Н—С—он I Но—с—н I Но—с—Н I Н—с_____ |
|
О |
|
Сн2он 0- D-галаитопираноза |
СН2ОН СИ2ОН СН2ОН
I I I
|
Но—с--------- I НО—С—н I О Н-с—он |
|
I О I И—с- |
|
Н—с—он н - ;—он I I D-фруктоза L |
С=0 НО—с-------
Но—с—н но—с—н н—с—он <~ Н—Г—он
<_Н2ОН
Р D-фрукто - P-D-фрукто - фураноза
Шраноза
О содержании гексозанов в том или ином материале судят по получаемым при гидролизе соответствующим сахарам, которые в свою очередь - определяются или в виде их характерных производных [*], или хрома- тографически.
Для маннозы характерен ее фенилгидразон, нерастворимый в ацетоне, с т. пл. 204—205°, а также м-бромфенилгидразон с т. пл. 208°. Галактоза часто определяется в кристаллическом виде, в виде (З-нафтилгидразона с т. пл. 190 —191° или путем окисления до слизевой кислоты с т. пл. 213 Фруктозу определяют в виде а-метилфенилгидразона с т. пл. 158—160" или и-нитрофепилгидразоиа с т. пл. 180—181°. Если при гидролизе получается только один вид сахара, то из этого можно заключить, что исходный'полисахарид состоял из однородных монозных остатков. Если же - при гидролизе получаются различные сахара, то источником их могли служить или смесь однородно построенных полисахаридов, или полисахариды, состоящие из различных ангидридов Сахаров, химически связанных между собой. Многообразие комбинаций, в которых могут группироваться ангидриды Сахаров в полисахаридах, указывает на невозможность ограничиваться исследованием одних только продуктов гидролиза.. Необходимо выделять полисахариды как таковые и изучать их уже - в чистом виде, хотя это и является чрезвычайно трудной задачей.
Общего метода определёйия всех гексозанов подобно методу определения иентозан^в-йет. Гексозаны при нагревании с 12°/0 НС1 гидро - лизуются до пексоз, из которых образ^тся оксиметилфу рфурол; последний в условиях этой реакции оказывается нестойким и в большей; своей части превращается в муравьиную и левуЖЯовую кислоты,, присоединяя две частицы воды
СН—ОН
II II
СН, ОН—СНОН—СНОН—СНОН—СНОН—C<f H0H2C—Сч о—с 7 +зн2о
н V и
СН—СН II II 'О
НОН2С—С ^С—С<^ - г 2 Н20 ^ НСООН -)- СН3—СО—СН2—СН2—СООН
От оксиметилфурфурола при нагревании может частично отщепляться формальдегид с образованием фурфурола
TOC o "1-3" h z СН—СН СН—СН
II II /Р II II /Р
НОН2С—Сч уС—с, —> СН20 - I - СН с—С^ >/ н ч/ н
И о
l/'j
Поэтому по оксиметилфурфуролу нельзя определить ка-че&тщдо сумму гексозанов. Общее содержание гексозанов в древесине определяют или по количеству сбраживаемых Сахаров в гидролизатах, или по сумме маннана и галактана, определенных по их частным реакциям.
Обычно в древесине хвойных содержится значительно больше гексозанов, чем в древесине лиственных. Для иллюстрации приводим данные о содержании легко гидро - лизуемых гексозанов в некоторых древесных породах (табл. 119) [2].
Маннан встречается во всех исследованных до настоящего времени хвойных породах, входит в состав многих растений и наряду с другими гемицеллюлозами часто сопровождает целлюлозу. В лиственных же породах его находят реже и в меньших количествах.
Маннан в древесине определяют в виде двух частей: легко гидролизуемого (кипячением опилок 5°/0-й НС1, с последующим высаживанием маннозы фенилгидразином) и трудно гидролизуемого (обработкой 72-й H2S04).
Общее содержание маннана в древесине хвойных [3] в среднем составляет 8—12°/0, в древесине лиственных [4] около 1%. Подробное обследование древесины разных пород, проведенное Шарковым с сотрудниками [5], показало, что содержание маннана меняется как по высоте,
|
Таблица 120 Содержание маннана в древесине хвойных [Е]
|
Так и по диаметру ствола; оно растет в хвойных от центра к периферии и убывает от основания к вершине, независимо от степени освещенности (табл. 120).
В целлюлозе, полученной из древесины бука и красной японской сосны, содержание маннана обнаружено главным образом в аморфных участках молекулы [6].
Маннан впервые был извлечен из сульфитной целлюлозы ели многократными обработками 8'/0-й NaOH и последующим высаживанием из подкисленных растворов спиртом.
|
Таблица 119 Содержание гексозанов в некоторых древесных породах
|
Для очистки маннана от примесей выделившийся осадок растворяют в медноаммиачном растворе, из которого маннан выделяют в виде медно-
щелочного соединения, формула которого, возможно близка к формуле меднощелочного соединения целлюлозы [3< стр. 202].
О
СбИ7°2<Г ^Си Cu(NH3)M + 2NaOH —>
П/ - I*
2 CctI702^0/CU + [Cn(NH3)K] (ОН)2 ^О Na
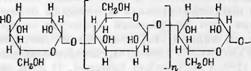
Из этого соединения очищенный маннан высаживают после подкисле - ния уксусной кислотой метанолом. Контролем чистоты продукта служит постоянство удельного вращения плоскости поляризации в нормальном •едком натре: [а]л18=—44.58°—42°. Маннан, выделенный подобными методами, имеет СП = 130—160 и линейную форму макромолекулы, в которой р-/)-маннопиранозные остатки соединены друг с другом глюкозид - ной связью в положении 1—4
|
|
В маннане древесины было найдено некоторое количество метокисль - ных групп. Предполагают, что метоксильные группы ослабляют силы ассоциации между отдельными цепями молекул, что содействует доступу растворителя. Маннан из древесины сосны, как было найдено, содержал •одну метоксильную группу на 8 остатков маннозы СвН10О6. Кроме того, в этом маннане определено около одной группы СООН в среднем на 20 ман - дозных остатков,
В одной из последних работ [47] для извлечения маннана сосновую холоцеллюлозу обрабатывали 24°/0-м раствором NaOH. Гемицеллюлозы •осаждали из раствора метанолом (после нейтрализации ледяной уксусной кислотой), нромывалп 80°/о-м раствором метанола и растворяли в го - рячей воде с получением примерно 1°/0-го раствора. К раствору добавляли 28%-й раствор аммиака и гидрат окиси меди в количестве, необходимом для получения раствора, содержащего 25% NH3 и 1.0% Си(ОН)2. Для полного растворения гемицеллюлоз в смеси вводили С02. Затем добавляли концентрированный раствор NaOH до получения 0.1N концентрации и смесь оставляли стоять на 3 часа. Осадок комплексного соединения меди с маннаном центрифугировали и очищали переосаждением. Хроматография показала, что полученный препарат содержал 82°/0 маннана с СП около 70, т. е. маннан был значительно деструктирован при выделении. Уроновые кислоты в данном препарате маннана не были найдены, остальную часть (18%) составляла глюкоза. В этой же работе был получен препарат маннана из слонового ореха. Как указывают авторы, маннан из слонового ореха был чистым маннаном. Кристалличность у соснового маннана (определена при помощи рентгенографического анализа) выражена слабее, чем у маннана слонового ореха, вероятно вследствие более сложного состава маннана сосны.
Выделенный из древесины маннан обладает лучшей растворимостью, чем маннан, находящийся в древесине. Замечено также, что маннан ели гидролизуется легче маннапа сосны.
Были получены производные маннана, например азотные эфиры маннана, частично растворимые в ацетоне, и бензоилацетилманнан - полностью растворимый в хлороформе. Этот смешанный эфир содержал две бензоильных и одну ацетильную группы на каждый остаток маннозы. Получен также бензиловый эфир маннана по реакции
CfiH8Os(OH)2 2C6H5CH2C1-f 2NaOH С6Нч03(0СН2С6Н6)2 -f 2NaCl + 2Н20
Бензиловый эфир хорошо растворим в спирто-бензоле (1 : 1), однако пленки получаются очень хрупкие.
Кроме древесины, маннан содержится в значительных количествах в клеточных стенках семян бобов, клубнях некоторых растений, дрожжах. Довольно подробно исследован маннан каменного ореха. Оказалось, что. он имеет такую же рентгенограмму и такую же величину удельного вращения, как и маннан. выделенный из древесины ели. В каменном орехе, кроме маннана, извлекаемого щелочью, с СП= = 71—86 (маннан А), был обнаружен еще другой маннан, нерастворимый в щелочи, обладающий большей длиной цепей. Общее содержание маннана в скорлупе каменного ореха доходит цо 65°/0.
В последнее время появились работы [7], указывающие, что маннан ореха состоит не только из остатков |3-£)-маннопиранозы, связанных в положении 1—4, но что в состав маннана входят также цепочки, у которых остаток манноттранозы имеет «-конфигурацию. Маннан подвергали ацетолизу при 20^ затем дезацетилировали (СН30)2Ва, хроматографи - ровали на угле, затем на целлюлозе, в результате чего была выделена смесь полимергомологов
Ман.1 — 4(3 (Ман. 1 — 4р)и Ман. 1 — 4|з, (1)
Ман. 1—4а (Ман. 1 — Щ,„ Ман. 1 — 40, (2>
|
1 Как известно, существуют различные способы условного перспективного изображения стр^тур, показывакщих взаимное пространственное расположение идрокс^гльны'х гр. упл в звене и характер ^вязи между звеньями в макромолейуле. Приведенная упрощенная структурная схема маннана ореха может быть представлена и в виде формул
|
|
Н Н Н Н Н Н |
|
СНг0Н снгон снгон В последнее время все чаще пользуются упрощенными структурными схемами |
Где Ман — маннопираноза.1
Маннан, извлеченный из клубней семейства орхидейных Tubera Sa- Iep, получил название салепманнана. Он легко извлекается из клубней путем экстракции водой и осаждается спиртом. Выход его доходит до 34°/0. При исчерпывающем его метилировании и последующем гидролизе было получено 84% 2,3,6-триметил-£>-маннозы и 1.7% 2,3,4,6-тетраметил-/)-маннозы, из чего следует, что молекула салепманнана состоит исключительно из маннопиранозных остатков, соединенных 1—4 глюкозидной связью. Специфическое вращение салепманнана в воде {а)л18=—35°. Путем фракционирования нитросалепманнана показано, что природный салепманнан является смесью салепманнанов с различной длиной цепей, что по мнению ряда авторов, характерно для резервных полисахаридов, находящихся в подвижном равновесии созидания и разрушения под влиянием ферментов. Легкая растворимость салепманнана ш воде утрачивается после обработки его кислотой или щелочью. Это объясняется отщеплением ацетильных групп, связанных в нем эфирной «вязью. Причем, как было найдено, на каждые 11 маннозных остатков в среднем приходится одна ацетильная группа.
В пекарских дрожжах, как показали исследования [4], ■содержится маннан, сильно отличающийся своим строением, со степенью полимеризации около 500. При кислотном гидролизе полностью метилированного маннана были получены 2,3,4,6-тетраметил-_0-манноза, ■3,4,6-триметил-С-манноза, 3,4-Диметил-£)-манноза в соотношении 2 :1 : 1 : 2 и небольшое количество 2,4,6-триметил-0-маннозы. Таким образом, между элементарными звеньями маннана дрожжей имеется главным ■образом три типа связей: 1—2, 1—3 и 1—6. Причем полагают, что на каждые 6 маннопиранозных остатков основной цепи два образуют боковую депь
... 2 Ман. 1------ 3 Ман. 1------- 2 Ман. 1------- 2 Ман. 1 . . .
6 6
I |
1 Man. 1 Man.
Где Ман. — остаток. D-маннопирансзы.-
Кроме того, выделенный из дрожжей маннан состоит только из D-маннопиранозных остатков и не содержит пентоз и уроновых кислот.
Водные растворы маннана имеют положительное вращение (а) в24 = 89°, что говорит об а-связи между маннопиранозными звеньями. Выход маннана (при обработке дрожжей горячим раствором 6%-го NaOH) составляет около 2%.
Весьма сходен с маннаном, изолированным из хлебных дрожжей, маннан, производимый дрожжами Saccharomyces Rouxu [8], в котором предположено три типа структуры: линейная цепь из чередующихся 1—2 и 1—6 связей (1); чередующиеся 1—2 и 1—6 связи в главной ■цепи и одного остатка со связью 1—2 в боковой цепи (2) и 1—6 связи ■в главной цепи и боковые ветви из двух остатков маннопиранозы со ■связями 1—2 (3)
Май. 1------ 2 Ман. 1------- -2 Man. 1------- 6 .Ман. (1)
Ман. 1 Мая. 1 (2)
2 2 .6 Ман. 1-------- 2 Ман. 1------- б Man. 1 2 Ман. 1.
|
(3) |
|
Ман. |
Ман. 1
|
2 Ман. |
|
2 Ман. |
2
|
-6 Ман. 1. |
|
Таблица 121 Содержание галактана в древесине
|
. 6 Ман 1-
Предположение об а-конфигурации 1—-2 связей в маннопиранозе основано на продуктах ацетолиза и положительном вращении в воде (аЬ27 = 58°.
Маннан из красных океанских водорослей (Red Algea Porphyra Umbilicalis) в отличие от маннана дрожжей построен из (3-/)-маннопиранозных остатков со связями 1—4, кроме того, в нем содержатся единицы маннуроновой кислоты [9]. Маннан был найден также в гидролизатах различных сельскохозяйственных отходов. Так, в соломе
И кукурузных кочерыжках маннана найдено до 6% к весу редуцирующих веществ.
Галактан сравнительно широко распространен в природе. Он содержится в больших количествах в морских водорослях, в пектиновых веществах различного происхождения и значительно меньше его находят в древесине и других растительных материалах.
В табл. 121 приводятся данные о содержании галактана в древесине некоторых пород.
Строение галактана чрезвычайно разнообразно и завист от вида растительного материала, в котором он содержится. Известны галактаны как с линейной, так и с разветвленной формой строения макромолекулы. В одних из них между элементарными звеньями имеются глюкозидные связи в положении 1—4, в других — в положении 1—3; в некоторых га - лактанах одновременно содержится несколько типов связей.
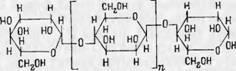
Наиболее хорошо изучен галактан, выделенный из семян белого люпина (Lupinus Albus), который построен из остатков [3-.0-галактопи - ранозы, соединенных в положении 1—4 глюкозидной связью. Количество полученной тетраметилгалактозы соответствует примерно одной концевой группе на 100 галактопиранозных остатков. Тип структуры следующий
|
|
|
-ООН |
Галактан легко растворяется в воде. Не вполне очищенный от примесей (пектина и арабана) галактан имел (а)г20 =38° в воде. После метилирования и удаления примесей (экстракцией эфиром) галактан имел (а)л20=—12° в уксусной кислоте. По данным Виноградовой, Конкина и Роговина [10], следует, что скорость гидролиза галактана в гомогенной среде в 2.6 раза больше скорости гидролиза целлюлозы, а в гетерогенной среде — в 300 раз. Это явление авторы объясняют различием структуры этих полисахаридов. Показано также, что при одинаковом молекулярном весе препараты галактана в отличие от целлюлозы полностью растворимы в воде. Процесс ацетилирования у галактана идет быстрее, чем у целлюлозы. Указанными авторами был впервые получен препарат тринит - рогалактана.
Из бурых водорослей (Rodophyceae) путем гидролизата 2°/0-й H2S04 при 108° и 0.34 атм. (с последующей очисткой гидролизата углем и упариванием в вакууме) получена кристаллическая галактоза с выходом около 23°/0 (от веса водорослей) [и].
Небольшое количество галактана было изолировано из а - целлюлозы белой и желтой березы и сахарного клена I12], построенного из A-D-та - Лактопиранозных остатков в положении 1—4.
В древесине хвойных пород, таких как лиственница, сосна Джеффри, белая ель, содержится сильно разветвленный галактан со связями 1—3. и 1—6. Однако считают, что галактан хвойных обязан своим происхождением водорастворимому полисахариду — арабогалактану (об этом см. ниже). Имеются указания [13], что в тяговой и креневой древесине эвкалипта и сосны содержание галактана увеличивается почти вдвое по сравнению с нормальной древесиной.
Шведские исследователи Бувен и Мейер [46] выделили из креневой древесины норвежской сосны водорастворимый галактан, содержащий 13% уроновых кислот. Высказано предположение, что сам галактан состоит из линейных цепей P-D-галактопиранозы, соединенных в положении 1—4.
JI е в у л а и (или фруктан) при гидролизе образует Z)-фруктозу, которую благодаря сильному вращению плоскости поляризации влево, называют еще левулезой. Фруктоза была обнаружена в продуктах гидролиза сульфитной целлюлозы (около 2.5%), в древесине ели (1.9%), в продуктах гидролиза инулина (см. выше). Вместе с 2)-глюкозой. D-фрук - тоза содержится во многих сладких плодах, в тростниковом сахаре, является составной частью меда; содержится в различных однолетних и двулетних травах [14] и других растениях [16]. В полимеры D-фрук- тоза чаще входит в виде пятичленного фуранозного кольца [16]. Типы связей в макромолекуле фруктана бывают различные: 2—1 (например, в инулине); 2—6 (фруктан корней райграса) [17], бывают одновременно - два типа связей 2—1 и 2—6 или 2—1 и 2—4 (в иризине и тритизине из, клубней ириса). Встречаются фруктаны и с циклической формой строения I18].
Г л ю к а н дает в качестве конечного продукта гидролиза, так ж& как и целлюлоза, jQ-глюкозу, однако, физические и химические свойства глюкана резко отличаются от целлюлозы [1в]. Во-первых, он не растворяется ни в горячей воде, как крахмал, ни в медноаммиачном растворе, как целлюлоза, но растворяется в 40—42% НС1 и выпадает из такого, раствора при разбавлении. Вторая его особенность та, что при частичном гидролизе глюкана можно получить в кристаллическом виде дисахарид,. не идентичный ни с целлобиозой, имеющей (3-глюкозидную связь,.
Ни с мальтозой, в которой два остатка глюкозы связаны а-глюкозидной •связью. При гидролизе метилированного глюкана, выделенного из клеточных стенок пивных дрожжей, была выделена 2,4,6-триметилглю - коза, на основании чего следует, что в глюкане дрожжей имеется 1—Зглю - козидная связь, а не связь 1—4, как в целлюлозе. В глюкане ячменя [20] ■структурная молекула состоит из (3-£)-глюкопиранозных остатков, со - •единенных в положении 1—4, с промежуточными связями в положении 1—3. На основании результатов мягкого ступенчатого гидролиза показано, что содержание глюкана в древесине ели составляет 7—8%, в древесине сосны 5.0%, в древесине березы 11.5%. Однако для точного предоставления о природе глюкана недостаточно только получить продукты гидролиза, необходимо также выделить сам полисахарид. К сожалению, .до настоящего времени из древесины не выделены полимеры глюкозы, •отличающиеся по строению и свойствам от целлюлозы, поэтому вопрос о существовании глюкана в древесине остается нерешенным.
Как уже указывалось, весьма распространены в растительном мире тексозаны смешанного типа, из которых в первую очередь заслуживает внимания арабогалактан.
Арабогалактан представляет собой водорастворимый по - •лисахарид, содержащийся в значительных количествах главным образом в древесине лиственницы. Так, в древесине даурской лиственницы ■содержится в среднем 10—12% арабогалактана (от веса древесины), но количество его может колебаться в широких пределах от 5 до
Различные авторы выделили и исследовали арабогалактан древесины западноамериканской, восточноамериканской и европейской лиственниц. Было найдено, что указанный полисахарид содержит 84.6% ангид- рогалактозы и 11.95% ангидроарабинозы, т. е. на каждые 6 молекул ангидрогалактозы приходится одна молекула ангидроарабинозы, согласно формуле [(С6Н10О6)6 ■ (C5Hg04)ln (теоретический состав — 88.1= ангидрогалактозы и 11.9= ангидроарабинозы). Однако молекулярные соотношения галактозы и арабинозы в арабогалактанах различного происхождения имеют значительные колебания (от 9.8 до 2.6) С8]. Литература по вопросам изучения арабогалактана довольно обширна и суммирована в специальных сборниках и статьях [21, 22, 30], а также обстоятельно изложена в последних работах шведских исследователей Бу - вена и Линдберга [".«ММв^о].
В продуктах мягкого гидролиза арабогалактана из Larix Deci- ■Daa [22] был обнаружен дисахарид 3-(3-£/-арабопиранозил-.£/-арабиноза, а в арабогалактане из Larix Occidentalis I23] наряду с вышеуказанным дисахаридом был найден еще дисахарид 6-{3-.0-галактопиранозил-.0-га - лактоза и небольшая фракция трисахарида.
Строение арабогалактана пытались определить, подвергая его исчерпывающему метилированию и гидролизу. Оставшиеся свободные гидроксилы в молекулах метилированных арабинозы и галактозы дали указание на расположение глюкозидных связей между остатками галактозы и арабинозы. Предполагают, что арабогалактан построен из весьма разветвленного остова, образованного из |3-1)-галактопиранозных единиц, ■связанных кислородной связью в положении 1—3 и 1—6. К этому остову присоединены концевые остатки арабофуранозы и галактопиранозы 'I! виде моно - и дисахаридов в положении 1—6 (или 1—3) со смежными остатками ангидрогалактозы. Например, арабиноза присоединяется «к остову галактозы следующим образом
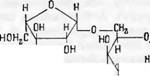
|
Збено В—Ь- apa6i факаио31 И/ |
|
/0 I1) он Збено |3=D—галактопиранозы |
|
Н |
|
-3 Гал. 1 6 |
|
, 6 Гал. 1 3 |
|
-6 Гал. 3 |
|
1 . |
|
Э Гал. |
|
1 Гал. 6 |
|
1 Гал. 6 |
|
1 Гал. 6 |
|
1 Гал. 6 |
|
1 Гал. |
|
1 Гал. |
|
1 Гал. |
|
1 Гал. |
|
(1) |
(2)
. . 6 (или 3) Гал. 1------------ 6 Гал. 1
3 (или 6)
-6 (или 3) Гал. 1— 6 Гал. 1 3 (или 6)
1
|
Гал. |
Гал.
(3)
-3 Араб. ф. 1. . . (4)
Где Гал. — р-£>-галактопираноза; Араб. — p-L-арабопираноза; Араб, ф. — P-L-арабофураноза.
В последнее время ['24] из западной лиственницы (Larixaccidentalis Nutt) с помощью электрофореза на бумаге был выделен арабогалак - тан, показавший наличие 2 компонентов (у1 и В), продвижение А было на 30°/о быстрее, чем В.
После исчерпывающего метилирования и гидролиза с НСООН (100°, 6 час.) продукты хроматографировали на угле-целите и бумаге. В результате были получены: 2-метилгалактоза (3.7 мол.°/0); 2,4-диметил- галактоза (37.5 мол.°/0); 2,6-диметплгалактоза (2.9 мол.°/0); 2,3,4-три - метил-/)-галактоза (13.7 мол.%), 2,4,6-триметил-/)-галактоза и 2,3,5- триметил-£-арабиноза (вместе 32.2 мол °/0); 2,5 димстил-^-арабиноза (3.2 мол.°/0); 2,3,4- гриметил L-арабипоза (2.6 мол.°/0).
|
Араб. 1- |
Предполагается, что 2/3 арабинозы присутствует в арабогалактане как конечные арабофуранозные единицы и [50]/3 как 3-Р-£-арабопирано - зил £-арабо<Ьураноза. Общее содержание арабинозы в арабогалактане 18—19 ш.°/0.
Полученные данные дали основание предположить наличие в арабогалактане дважды разветвленных единиц. Авторы считают, что галакта - новые остатки замещены в одинаковой степени у С2 и Св связями р-пира - нозидного типа. Не исключается также присутствие небольшого количества 1.4 связей.
26 н И, Никитин
Было также установлено [49], что цепи галактозных остатков, образующих скелет в полисахаридах А и В, очень сходны. Основу молекулы составляет разветвленный остов соединенных в положении 1.3—1.6 га - лактопиранозных единиц, с которыми связана арабиноза.
Седиментационный анализ арабогалактана дал константы седиментации для А и В, равные 4.3 и 1.4, отношение компонентов приблизительно равное 2:1, молекулярный вес соответственно определен в 100000 и 16 ООО. Эти данные согласуются с результатами, полученными ранее другими исследователями [25].
Неоднократно возникал вопрос: является ли арабогалактан действительно индивидуальным веществом определенной структуры и постоянного химического состава или просто смесью арабана и галактана. Этот вопрос еще не может быть окончательно решенным.
При дробном высаживании арабогалактана из водного раствора этиловым спиртом было выделено несколько фракций. Эти фракции не отличались друг от друга по величине редуцирующей способности, содержанию арабинозы, скорости гидролиза, оптическому вращению и элементарному составу. На основании этих данных некоторые авторы пришли к заключению, что арабогалактан является однородным полисахаридом, а не смесью арабана и галактана. Однако весьма вероятно, что он состоит из смеси нескольких видов макромолекул, очень близких по составу, с большим или меньшим содержанием арабинозы.
Значительное внимание исследователей за последние годы привлекла даурская лиственница ввиду огромных запасов ее в Советском Союзе. Н. И. Никитин с сотрудниками [26] занимались изучением химического состава этой древесины, вопросами распределения арабогалактана в древесине, местонахождения арабогалактана в ткани, сульфатной и сульфитной варкой лиственничной древесины и др. При этом было показано, что арабогалактан содержится почти исключительно в ядре лиственницы (15—30°/0) и л ишь в незначительном количестве в заболони (0.8°/,,).' Арабогалактан ядра даурской лиственницы содержит в среднем 86.6% ангидрогалактозы и 12.1°/0 ангидроарабинозы, т. е. имеет, по-видимому, тот же состав, что и арабогалактан других разновидностей лиственницы.
Арабогалактан распределяется по диаметру среза различно: количество его увеличивается от центра к периферии, достигая максимума в годичных слоях ядра, граничащих с заболонью. Содержание арабогалактана в заболони сразу резко падает и остается на одном уровне до края среза. Больше арабогалактана содержится в комле. Показано также, что в пределах годичного слоя ранняя древесина содержит больше арабогалактана, чем поздняя, локализация же арабогалактана происходит главным образом в срединных пластинках и сердцевинных лучах. В молодых частях (ветви, вершина) древесины даурской [27] и сибирской [28] лиственницы содержание арабогалактана понижено.
Этот полисахарид представляет собой ценный продукт, так как может перерабатываться путем гидролиза и сбраживания на спирт. Для сбраживания галактозы лучше применять рассу дрожжей Schizosaccharo- Myces. Теоретически от веса сахара получается больше половины спирта
С6Н12Ов - и* 2 С2НБОН + 2С02.
При гидрировании арабогалактана можно получить многоатомные спирты главным образом дульцит I29]
СбН1206 -j Н2 —> СеН1406.
Арабогалактан обладает клеящими и другими полезными свойствами.
Полисахариды типа арабогалактана содержатся не только в различных разновидностях лиственницы, но и в других хвойных породах (сосне, ели) [30], в некоторых лиственных (но в меньших количествах). Значительное количество арабогалактана было обнаружено в листьях бобовых (12°/0), бобовых стручках (30%), душистом горошке (30%), исландском мхе (10%)и др. [31Ь
Глюкоманнан является смешанным гексозаном, молекула которого построена из ангидроманнозных и ангидроглюкозных остатков в различных соотношениях, в зависимости от того, из какого растительного материала он был извлечен.
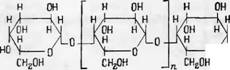
Так, из зерен Conophalus Konjak экстракцией водой при 110—125° (под давлением) был извлечен глюкоманнан (коньякманнан), состоящий из ангидроманнозы и ангидроглюкозы в соотношении 1 : 2. При гидролизе метилированного глюкоманнана образуются 2,3,4-триметил - манноза, 2,3,6-триметилманноза и 2,3,4-триметилглюкоза, что говорит о наличии связей 1—4 и 1—6. Был также выделен глюкоманнан [32] из муки коньяк и с другим соотношением глюкозы и маннозы, как 2 : 3. Из холоцеллюлозы западного гемлока [33] экстракцией 18% NaOH выделен глюкоманнан в соотношении маннозы к глюкозе как 2.5 : 1. Было определено хроматографией на бумаге продуктов ступенчатого кислотного гидролиза глюкоманнана гемлока присутствие глюкозидоманнозы, маннобиозы, маннозидоглюкозы, целлобиозы и маннотриозы. Эти результаты в сочетании с физико-химическими свойствами показали, что глюкоманнан представляет собой полимер с короткой прямой цепью, составленной из манно - и глюкопиранозных звеньев и имеющий глюкопиранозид - ную концевую группу. Звенья соединены в положении 1—4 (3-глюкозид - ными связями. Глюкоманнан западного гемлока подобен глюкоманнанам, полученным из других видов древесины [34].
Изолирование 4-Р-£>-глюкопиранозил-2)-маннопиранозьт из а-целлю - лозы белой березы дает возможность заключить о присутствии химической связи между глюкозой и остаткамхг маннозы в лиственной древесине. Все хвойные породы, как показывают исследования, содержат глюкоманнаны в форме дигетерополимера. Считают [35], что глюкоманнаны не являются продуктами деградации целлюлозы, а происходят, вероятно, из отдельной энзимной системы. Эти глюкоманнаны очень устойчивы к щелочной экстракции, особенно к экстракции КОН.
Многие исследователи [36] объясняют присутствие маннозы в экстрагированном щелочами остатке целлюлозы как следствие присутствия глю - команнанов, имеющихся почти во всех хвойных породах I37].
Из небеленой сульфитной целлюлозы Митчерлиха выделен через Си - комплекс гетерогенный глюкоманнан [8В], содержащий боковые цепп. В результате ступенчатого гидролиза выделены и идентифицированы: £)-манноза, D-глюкоза, Z)-ксилоза, следы /)-галактозы-4-((3-0-маннопира - нозил)-£>-маннопиранозы. Среди других продуктов гидролиза обнаружены глюкозидоглюкоза, глюкозидоманнозидоглюкоза, маннозидоманно - зидоманноза, трисахарид, возможно, разветвленный, содержащий два основных звена маннозы и одно — глюкозы. Глюкоманнан, выделенный из целлюлозы красной сосны [зв], по сравнению с полисахаридами, изолированными из других древесин, имеет более низкое отношение звеньев маннозы с звеньям глюкозы. Из холоцеллюлозы древесины Pinus Sil- Vestris [40] после удаления ксилана получали глюкоманнан растворением холоцеллюлозы в куприэтилендиамине. Исследование фракций показало, что отношение глюкозы к маннозе в глюкоманнане изменялось от 1 :3.1 до 1 : 7.7. При этом все фракции глюкоманнана содержали галактозу, что указывает на присутствие в препаратах глюкоманнана галакто - глюкоманнанов. Степень полимеризации, определенная осмометрическим и вискозиметрическим методами, изменялась у глюкоманнанов от 70 до 115. Другие исследования [41] показали, что молекула глюкоманнана (из этой же породы) разветвлена, имеются в ней 3 цепи на 100 остатков гексоз. Разветвления, как полагают, начинаются от С3 остатков /J-г л го - козы.
Глюкоманнан, выделенный из клубней японской орхидеи (крема - строманнан), состоит из маннозных и глюкозных остатков в соотношении 3 : 1, а выделенный из клубней Bletilla Striata — в соотношении
4 : 1. Эти глюкоманнаны имеют различные углы удельного вращения, в некоторых других свойствах они близки между собой.
Глюкофруктан, выделенный из клубней гавайского растения (Cordyline Terminalis), построен из остатков /)-фруктофуранозы и 2)-глюкопиранозы в соотношении 13 : 1. После гидролиза метилиро ванного глюкофруктана выделены 4 моля 1,3,4,6-тетрамил-/)-фруктозы,
5 молей 3,4,6-триметил-.0-фруктозы и 1 моль 2,3,4-триметил-/)-глюкозы, что дает возможность предположить следующую структуру I42]
У — 6 Гл. 1 — 2 Гл. 1 — у,
Где у=... 2 Фр. 6—2 Фр. 6—2 Фр. 1—2 Фр. Ч—2 Фр. 1—2 Фр.; Гл. =р-2)-глк>- копираноза; Фр. = |3-/)-фруктофураноза.
Из пшеничной муки [43] путем экстракции 70% спиртом выделено глюкофруктан (ал)20=21° (в воде). При гидролизе глюкофруктана получена /?-фруктоза (87.5%) и /)-глюкоза (12.5'Уо). Легкость гидролиза указывает на фуранозную форму /^-фруктозы. Продукт метилирования глюкофруктана имел(а£)28%—36° (в ацетоне), содержание групп ОСН3 равно 45.3%. После гидролиза и хроматографирования продуктов метилирования выделены 3,4-диметил-/)-фруктоза, 1,3,4-триметил-2)-фруктоза, 1,3,4,6-тетраметил-2)-фруктоза и 2,3,4,6-тетрамотил-D - глюкоза в молекулярных соотношениях 2:3:3:1. Так как глюкофруктан не редуцирует, ему можно приписать строение цепочки фруктофуранозных остатков, соединенных в положении 2-6 (3-глюкозидной связью, заканчивающейся остатком глюкопиранозы. К четным фруктофуранозным остаткам в положении 1—2 присоединены по одному остатку фруктофуранозы (3-глюкозидной связью.
Галактоманнан выделен щелочной экстракцией из внутренних оболочек зерен кентукских кофейных бобов [44]. После кислотного гидролиза 1 N H2S04 (11 час. кип.) в гидролизате найдено: 80э/о D-маннозы и 20°/о /?-галактозы. Определено, что галактоманнан состоит из повторяющихся 25 остатков /)-маннопиранозы и 5 остатков £>-галактопиранозы, связанных в положении 1—6 (в боковой цепи). Один остаток /)-манно - пиранозы занимает конечное положение. Остатки /?-маннопирапозы связаны между собой (3-глюкозидной связью в положении (в основной цепи) 1-4.
Галактоманнаиы были выделены также из камедей бобов (Cerato- Nia Siligua) с образованием при гидролизе 86% маннозы и 14°/0 галактозы; из семян люцерны, из семян растения Cyamopsis Proraloides, При гидролизе которого образуется 60°/о маннозы и 37°/0 галактозы. Удельное вращение этого полисахарида в воде (а)^5=53° указывает на а-форму глюкозидной связи. Галактоманнан способен образовать вязкие дисперсии, применяемые в качестве загустителей [45]. Полученный порошок при упаривании растворов галактоманнана (при 55°) легко диспергируется в воде. Водные дисперсии можно применять в печатных красках.

 Опубликовано в
Опубликовано в