ТЕРМООКИСЛИТЕЛЬНАЯ ДЕСТРУКЦИЯ И СТАБИЛИЗАЦИЯ
 2 декабря, 2013
2 декабря, 2013  admin
admin Механизм деструкции. Термоокислительная деструкция полиолефинов протекает по радикально-цепному механизму с вырожденными разветвлениями и подчиняется экспоненциальному, закону:
W = Ае^
где W — скорость окисления;
А, ф — константы; т — время.
Процесс вырожденного разветвления связан с образованием промежуточных продуктов, способных распадаться на свободные радикалы и зарождать новые цепи. Такими промежуточными продуктами для полиолефинов являются перекисные соединения. Схему окисления полиолефинов4-5 можно представить в следующем виде:
1. Образование радикалов или окислительных центров
TOC o "1-5" h z rh + 02-i->R+H02 (1)
2. Развитие цепи
R + 02 R02 (2)
и
R02 + RH ROOH + R (3)
3. Процесс вырожденных разветвлений
ROOH + RH _ЛRO + R + НаО (4) ‘
4. Образование неактивных продуктов
R02 - f R02 —неактивные продукты (5)
Зарождение радикалов (реакция 1) и развитие цепи (реакции 2 и 3) определяют только начальную стадию окисления полимеров, которая зависит от температуры, природы химических связей, образующих макромолекулы, наличия остатков катализаторов и структурного состава полимера.
При низких температурах скорость поглощения кислорода полимерами незначительна. По данным некоторых исследователей6, величина индукционного периода для полиэтилена линейного и разветвленного при нормальных условиях составляет свыше 2 лет. При повышении температуры до 200 °С индукционный период для этих полимеров сокращается соответственно до 50 и 30 ч. Наличие остатков катализатора также способствует сокращению периода индукции7.
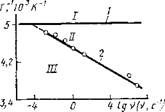
Развитие окислительной цепи (реакция 3) зависит от подвижности атома водорода, которая увеличивается при переходе от первичных к третичным связям8'9 (рис. 21). По некоторым исследованиям10,11, меньшая энергия активации окисления полипропилена по сравнению с полиэтиленом (табл. 16) объясняется не подвижностью атома водорода, расположенного у третичного углеродного атома, а главным образом подвижностью водорода в коротких боковых алифатических звеньях. Отрыв водорода от
|
Энергия активации термоокислительной деструкции полиолефинов13 |
ТАБЛИЦА 16 |
|
Энергия акти |
|
|
Полимер |
вации ккал/моль |
|
Полипропилен................................................. |
21,8 |
|
Полиэтилен линейный....................................... |
31.9 |
|
Полиэтилен разветвленный................................ |
32,7 |
|
Сополимер этилена с пропиленом.... |
30,8 |
основной цепи сопряжен с переходом соответствующего участка цепи от тетраэдрической к плоской конформации; такое изменение конформации должно привести к повышению энергии активации, а, следовательно, к снижению скорости окисления полимера.
Подвижность водорода также возрастает, если связь С—Н находится в a-положении к двойной связи4.
В результате термоокислительной деструкции происходит изменение средневесового и среднечислового молекулярного веса полимера12 (рис. 22).
Влияние структурного состава полимера на скорость окисления узучалось многими исследователями. Установлено14, что скорость окисления атактического полипропилена выше, чем изотактического кристаллического полимера. Каватиан15 также указывает, что присоединение кислорода к полиэтилену происходит в первую очередь к аморфной части полимера.
Различие в скоростях окисления аморфных и кристаллических полимеров связано с тем, что скорость диффузии кислорода в кристаллический полимер меньше, чем в аморфный.
На начальную скорость окисления полиолефинов оказывают существенное влияние концевые ненасыщенные группы и макрорадикалы, которые образуются при грануляции и формовании волокна. Кроме того, слабыми местами в полиолефинах являются участки цепи, содержащие перекисный кислород, образование которого возможно при сополимеризации мономера с кислородом воздуха, присутствующим в небольшом количестве в полимеризационной системе, а также при механо-термической
|
Рис. 21. Стойкость полипропилена Рис. 22. Изменение средневесового ч полиэтилена к термоокислительной тт и среднечислового Гмп) молеки - деструкции при 150 °С: мртго ^ noMnponuJHa в заеиси. I—полипропилен, 2 полиэтилен мости от степени деструкции. |
переработке полимеров. В полиэтилене спектральными методами обнаружены кислородсодержащие (гидроксильные, карбонильные, карбоксильные) группы (табл.17).
Как указывалось, реакции (1), (2), (3) определяют только начальную скорость окисления. В дальнейшем, по мере накопления в полиолефинах перекисных соединений, способных распадаться по связям О—О (реакция 4), энергия диссоциации которых составляет всего 35 ккал/мо'ль, окисление протекает с большей, чем в начальный период, скоростью, и это определяет кинетику реакции (рис. 23). Установлено, что распад перекисных соединений при окислении полиолефинов протекает по бимолекулярному механизму.
При глубоком окислении поглощение кислорода проходит через максимум и затем снижается, оставаясь постоянным в течение длительного времени. Торможение процесса окисления
|
ТАБЛИЦА 17 Химическая неоднородность полиэтилена различной структуры
|
|
Полиэтилен разветв-! ленный.... |
30 |
0,17 |
0,09 |
0,89 |
1 |
|
Полиэтилен линейный............................ • 1 |
2,2 |
<1 |
0,9 |
<1 |
0,25 |
полиолефинов сопровождается выделением легколетучих продуктов окисления, состоящих в основном из Н20, С02, НСООН, НСНО, которые образуются в результате распада первичных продуктов окисления (табл. 18).
|
Рис. 2г. /fccffi'1'я теле рода полиэтиленом: I—кислород: 2—K. u.t лсрод в вид гидрспгреь исных групп. |
Из таблицы видно, что летучие продукты разложения всех исследованных полиолефинов имеют практически один и тот же качественный состав; изменяется только их количественное соотношение. Так, за 4 ч окисления полипропилена при 150°С кислот образуется в 15 раз больше, чем при окислении линейного полиэтилена, формальдегида— в 13 раз больше и ацег - альдегида — в 6 раз. При, повышении температуры выход летучих продуктов «возрастает (главным образом кислот и карбонильных соединений).
Вследствие высокой вязкости системы выделение первичных продуктов окисления из полимера затруднено, поэтому продолжительность пребывания их в зоне реакции увеличивается. Кроме того, при прохождении продуктов распада через наружные слои полимера, где скорость окисления максимальна, происходит более глубокое окисление. Поэтому образующиеся при окислении полимерные радикалы не способны к значительным перемещениям, что является одной из причин возникновения пространственных структур.
Стабилизация термоокислительной деструкции. Для предотвращения термоокислительной деструкции полиолефинов применяют стабилизаторы или ингибиторы, которые или блокируют
активные радикалы R02 (реакция 2) или разрушают перекиси
|
СО |
о |
со |
||
|
О |
со |
|||
|
со |
„ |
Гр |
сч |
|
|
7 |
1 |
1 |
||
|
СО |
LO |
О0 |
||
|
со |
||||
|
сч |
со |
|||
|
о |
|
О о |
|
< Я S г; из < |
|
Летучие продукты окисления полиолефиновw при 150 3С (в миллимоль на моль мономера) |
|
X О О U |
|
3 к СП |
|
еС О |
|
о >> |
|
ч о CQ |
|
ч о CQ |
|
ю |
ю |
со |
о |
||||||
|
ю |
со |
Ю |
)_с |
||||||
|
сч |
сч |
00 |
оз |
||||||
|
j |
1 |
о |
I |
1 |
1 |
1 |
|||
|
сч |
1 |
со |
Гр |
1 о |
ю |
со |
|||
|
f—. |
+ |
со |
*• |
- |
о |
сч |
|||
|
см |
|||||||||
|
о |
|||||||||
|
о |
00 |
о |
|||||||
|
о |
СО |
||||||||
|
СЧ i |
! |
7 |
Гр 1 |
7 |
сч 1 |
1 |
I |
1 |
|
|
I 00 |
] |
1 о |
1 Гр |
сч |
1 о |
1 |
1 |
1 |
|
|
о |
|||||||||
|
со |
—« |
сч |
|||||||
|
со |
о |
Гр |
ю |
о |
|||||
|
С-1 |
•« |
г. |
о |
Ю |
|||||
|
7 |
со 1 |
7 |
сч 1 |
т |
сч 1 |
1 |
Ю 1 |
j |
|
|
1 оз |
1 о |
1 со |
1 03 |
Гр |
1 о |
1 со |
1 со |
||
|
LO |
|||||||||
|
со |
о |
||||||||
|
ю |
СО |
00 |
«о |
||||||
|
сч |
о |
||||||||
|
7 |
1 |
о 1 |
сч 1 |
о 1 |
со 1 |
1 |
1 |
1 |
|
|
1 С73 |
1 |
1 ГР |
1 00 |
1 ю |
1 о |
1 |
1 |
1 |
|
|
оз |
|||||||||
|
о |
о |
сч |
|||||||
|
СО |
со |
00 |
Гр |
о |
со |
||||
|
гг |
ю |
о |
|||||||
|
С73 1 |
сч 1 |
о 1 |
7 |
{ |
сч 1 |
сч |
1 |
Гр 1 |
|
|
1 |
1 о |
1 ю |
1 сч |
i 03 |
1 о |
i о |
1 СО |
1 С-. |
|
|
оз |
сч |
||||||||
|
сч |
о |
о |
СО |
||||||
|
‘ij |
Ю |
о |
|||||||
|
со |
ю |
00 |
со |
ю |
|||||
|
7 |
1 |
со |
сч 1 |
со 1 |
7 |
СО 1 |
1 |
[ |
1 |
|
1 Ю |
1 ю |
I Г"- |
1 сч |
1 00 |
1 00 |
1 о |
1 |
1 |
1 |
|
сч |
со |
со |
сч |
сч |
|||||
|
сч |
со |
||||||||
|
о |
о |
о |
|||||||
|
со |
со |
сч |
ю |
LO |
сч |
о |
о |
||
|
7 |
со 1 |
Гр 1 |
ю 1 |
сч 1 |
00 1 |
1 |
ю 1 |
сч 1 |
|
|
1 о |
1 Ю |
о |
1 Гр |
1 ю |
i Ю |
о |
1 о |
1 о |
1 с-. |
|
со |
Гр |
г— |
о |
Гр |
|||||
|
СО |
|
00 СО |
|
X и о и о |
|
S о. о е |
|
ч о |
|
ч о |
|
5 |
|
< |
(реакция 3), не образуя при этом активных радикалов2'4. Дезактивация радикалов R02 возможна только в том случае, если водород в молекуле ингибитора (АН) связан менее прочно, чем в полимере (RH).
Механизм стабилизации. Взаимодействие ингибитора
с полимерным радикалом R02 происходит по реакции:
|
(6) |
AH-f R02 ROOH+ А
Образующийся при этом радикал А должен быть малоактивным и не способным продолжать реакционную цепь. В качестве ингибиторов полиолефинов, действующих по механизму дезактивации свободных радикалов (R02), применяются производные фенола и аминов. В настоящее время установлено17'18, что ингибирующая активность фенолов и большинства аминов обусловлена наличием в их молекулах подвижных атомов водорода, способствующих протеканию реакции (6).
Методом электронного парамагнитного резонанса (ЭПР) доказано7’1в’20, что при распаде фенолов и аминов образуются сравнительно стабильные радикалы. Установлена2* зависимость между строением фенольных ингибиторов н их эффективностью. Двухатомные фенолы эффективнее одноатомных. о и n-Изомеры более активны, чем л-изомеры. Алкилфе - нолы. и особенно 2,4,6-триалкильные производные с СН3-группой в п-поло - жении, более эффективны, чем незамещенные фенолы. Отмечается положительное влияние галоида в n-положении к гидроксильной группе. йис-фенолы, содержащие между ароматическими ядрами атомы серы или группы —CH.,—, отличаются высокой эффективностью. Строение аминов также влияет на процесс ингибирования22. Так, для производных фенил-(3-нафтиламина, содержащего различные заместители в бензольном кольце в n-положении, показано, что прочность N—Н связи возрастает, а ингибирующая активность снижается в следующем ряду заместителей:
ОН > ОСН3 > СН3 > Н > С1 > N02
т. е. реакционная способность аминов снижается с уменьшением электроно - донорных свойств заместителей.
Ингибиторы, действующие главным образом на полиолефи - ны по механизму разрушения перекисных соединений, изучены значительно меньше. Предполагают, что соединения, содержащие серу, взаимодействуют с перекисями по следующим реакциям:
О
II
ROOH-f R— S—R"--------------- > ROH + R'—S—R'
О
|
ROOH - f R'—S—R II О |
|
ROH + R'-S—R’ I! О |
Сульфиды, содержащие по крайней мере одну алифатическую или ациклическую группу, присоединенную к атому серы, являются более эффективными ингибиторами, чем меркаптаны и дисульфиды, тогда как диарилеульфиды и днарилсульфоны неактивны. Разрушение гидроперекисей сульфидами может протекать и с образованием свободных радикалов. Это было установлено при применении в качестве ингибиторов окисления полипропилена смесей тетра - метилтиурамдисульфида, а также дифеннлсульфида с различными перекмс - ными соединениями.
Фосфорорганические соединения (тризамещенные фосфины и триалкилфосфиты) также способны взаимодействовать с гидроперекисями, превращаясь соответственно в фосфиноксиды и три - алкилфосфаты23:
ROOH - f R3P--------- > ROH + R3PO
ROOH + (R'0)3P----------- > ROH + (R'0)3PO
Следует отметить, что стабилизаторы оказывают на полимер не только ингибирующее, но также инициирующее действие4-5. Инициирование возможно в результате окисления стабилизатора по реакциям:
TOC o "1-5" h z АН - f 02 А + Н02 (7)
Хя
A+RH AH + R (8)
Стабилизатор может также инициировать окисление, реагируя с гидроперекисями24:
ROOH + АН RO + А + Н20 (9)
Таким образом ингибирующее действие стабилизатора зависит от соотношения скоростей обрыва цепи и инициирования, которые определяются подвижностью водородного атома и реакционной способностью малоактивного радикала.
Величина индукционного периода деструкции возрастает с увеличением количества стабилизатора только в том случае, если его концентрация в полимере не выше критической, т. е. такой концентрации, при которой наблюдается стационарный режим, когда при распаде стабилизатора и гидроперекиси получается одинаковое число радикалов5; критическая концен
трация ингибитора определяется соотношением
1ЛН1«Р. = <n=WRHi
где а — степень распада гидроперекиси на радикалы R02.
Такое представление о механизме действия ингибиторов окисления при стабилизации полиолефинов подтверждается экспериментальными данными25.
На рис. 24 показано изменение величины индукционного периода деструкции полиэтилена, стабилизированного фенил-п -
фенилендиамином, из которого видно, что с увеличением количества ингибитора возрастает величина индукционного периода; по мере расходования ингибитора наблюдается ускоряющийся процесс окисления, который свидетельствует о разветвленной цепной реакции.
|
Рис. 24. Влияние концентрации стабилизатора на скорость окислительной деструкции полиэтилена при 150 °С: I—без стабилизатора; 2—0.05% дифенил-п - фенилендиамина; 3—0,2% дифенил-п-фенилен- диамина. |
|
Рис. 25. Зависимость периода индукции окислительной дест - рукпии полипропилена от природы стабилизатора: 1 —дидецилсульфи д 2—2.6 - ди*. п рет - октил-4-м етилфенол', 3—см есь dude - цилсульфида и 2.6-ди-пре, а-окти.1'4 - метилфенолл. |
Эффективность ингибирующего действия стабилизаторов уменьшается с повышением температуры вследствие того, что при этом скорость инициирования процессов деструкции возрастает быстрее, чем скорость обрыва цепей.
Повышение эффективности стабилизаторов (синергизм). При введении многих стабилизаторов в полиолефины не наблюдается значительного увеличения индукционного периода, например: 2,4,6-три-грег-бутилфенола, 2,6-ди-
грег-бутил-4-фенилфенола, 4,4/-метилен-бмс- (2,6-ди-грег-бутил - фенола) и 2,6-ди-трет-октил-4-метилфенола26. При этом реакция окисления протекает нестационарно при всех концентрациях этих ингибиторов. Причина низкой эффективности перечисленных стабилизаторов заключается в том, что они стимулируют разветвление кинетических цепей окисления. Однако если в полимер добавить кроме 2,6-ди-грег-октил-4-метклфенола (рис. 25), дидецилсульфид, который также является малоэффективным стабилизатором, то индукционный период процесса
деструкции увеличивается26 до 450 мин (при 200 °С и Р0а— 300 мм рт. ст.).
Увеличение периода индукции наблюдается27 также при добавлении в полипропилен смеси пирокатехинфосфитионола с ди - (грег-бутил-я-крезил)-сульфидом (КАО-6), при суммарной концентрации ингибиторов 0,015 моль/кг. Индукционный период процесса деструкции полиэтилена также возрастает при введении в него смеси ингибиторов, состоящих из 4,4'-тио-бис - (6-трет- бутил-ж-крезола) с различными тиоэфирами28. При совместном употреблении небольших количеств (0,1%) тио-р-нафтола и ароматических углеводородов с конденсированными ядрами (0,1%), которые не показали заметной активности при раздельном применении, наблюдалось значительное уменьшение скорости окисления полиэтилена29 (табл. 19).
Эффект взаимного усиления действия ингибиторов (который часто называют синергизмом), по-видимому, заключается в дезактивации радикалов, вызывающих инициирование окисления.
Стабилизаторы термоокислительной деструкции. В настоящее время известно большое число веществ на основе производных аминов, сульфидов, фенолов, которые могут служить стабилизаторами термоокислительной деструкции полиолефинов. Однако практическое применение получили только соединения, которые характеризуются:
1) устойчивостью к действию тепла н кислорода воздуха;
2) совместимостью с полимером. При этом большую роль играет равномерное распределение стабилизатора в полиолефинах, которое может быть достигнуто, например, введением стабилизатора в процессе полимеризации;
3) невысокой летучестью;
4) отсутствием токсичности.
|
а также смесь я-грег-бутилфенилсалицилата и 2,4-дибензоилре - зорцина31 и 2,6-ди-грег-бутил-4-метилфенол, 2,2/-метилен-бис - (4,6-диалкилфенол)32, Л1,Л1'-ди-2-нафталин-я-фенцлендиамин; |
В качестве стабилизаторов для полиэтилена, удовлетворяющих перечисленным требованиям, могут применяться смесь30
2,6- ди-грег-бутил-я-крезола (I) и 4,4/-тио-бмс- (б-грег-бутил-м - крезола) (II):
|
ОН СН3 СН3 С(СН3)з С(СН3)з |
Индукционный период при 140 СС, ч
|
— |
— |
— |
10[4] |
|
Нафталин.................................. |
00 |
4 |
16 |
|
Антрацен.................................. |
fyys чАА^ |
4 |
20 |
|
Нафтацен................................. |
fWY4! ХАА. АХ |
52 |
1510 |
|
Пентацен............................ |
СХХХХ) |
28 |
3000 |
|
Перилен................................... |
ООО и |
14 |
3500 |
|
Короиен.................................. |
00 |
4 |
2000 |
|
Углеводород |
|
Формула |
|
углеводород без добавок |
|
углеводород в смеси с тио-0- нафтолом |
|
* Чистый тио-р-цафтол. |
|
Синергическое действие ароматических углеводородов в смеси с тиоУнсфтолсм при crrofилизаиии полиэтилена________________________________________ |
Для полипропилена во многих случаях рекомендуется применять те же препараты, что и для полиэтилена. Н. В. Михайлов, Л. Г. Токарева и А. Г. Попов33 исследовали около 25 различных соединений для стабилизации полипропиленового волокна*. Из них наиболее эффективными (по физико-механическим свойст
вам волокна, прогретого в течение 8 ч при 150°С) оказались
2.6- ди-7'рет'-бутил-4-метилфенол, терпенофенолы и смеси производных фенола с серусодержащими соединениями, например
2.6- ди-гре7'-бутил-4-метилфенола с дибензоилдисульфидом. Синергическим действием обладают также смеси меркаптобенз - имидазола (I) и оксидифениламина (II):
|
N I Н |
На применение серусодержащих соединений в качестве веществ, предотвращающих термоокислительную деструкцию, указывают также и другие исследователи34. Так, характеристическая вязкость полипропилена не изменяется при прогреве (140 °С) в течение 100 ч и введении в полимер до 1,5% таких соединений, как 4,4'-тио-бис-(3-метил-5-трет-бутилфенол), 2,2'-mo-6uc-(3-mpem- бутил-5-метилфенол), 4,4'-тио-б«с-(2-метил-5-тре/п-бутилфенол). Согласно австрийскому патенту35, при введении в полиолефины от 0,02 до 2%<х, 3-бензоизотиозо - лон-1-диоксида, сахарина или их А'-алкил - или арилзамещеиных (2-метил - сахарин, 2-этилсахарин, 2-феиилсахарин, 2-ацетанилсахарин) также увеличивается стойкость полимеров к термоокислительной деструкции.
В табл. 20 приведены сравнительные данные по стабилизации полипропилена ингибиторами промышленного значения36.
Из табл. 20 видны преимущества смесей стабилизаторов. Так, смесь, состоящая из 0,3% 2,2'-тио-бис-(4-метил-6-грег-бутилфе - нола) и 0,2% а-нафтилового эфира пирокатехинфосфористой кислоты, является более эффективным ингибитором полипропилена, чем каждое из этих соединений. Приведенные в табл. 20 смеси ингибиторов могут быть использованы не только для стабилизации полипропилена, но и других полиолефинов.
Разрушение полиолефинов происходит не только под влиянием тепла и кислорода воздуха, но также под действием света.

 Опубликовано в
Опубликовано в