КРИСТАЛЛИЗАЦИЯ КАК ГЛАВНЫЙ ФАЗОВЫЙ ПЕРЕХОД В ПОЛИМЕРАХ
 14 ноября, 2013
14 ноября, 2013  admin
admin Определения ф Процессы образования и роста кристаллов в полимерах
Переход полимеров из структурно жидкого в твердое состояние реализуется посредством кристаллизации. Этот процесс, являющийся фазовым переходом 1-го рода, многоступенчатый, однако полностью закристаллизовать полимер не удается. Сравнительно быстрое протекание процесса кристаллизации, приводящего к образованию довольно совершенных по своей структуре полимеров, может быть связано с наличием заготовок в их расплавах. Кристаллиты— это термодинамически стабильные структуры, и время их жизни т*—>~оо (ниже температуры плавления).
2.3.2. Процессы образования и роста кристаллов в полимерах Механизм зародышеобразования в полимерах принципиально
не отличается от механизма образования зародышей кристаллизации в низкомолекулярных веществах, которому посвящено большое количество исследований, начатых еще в конце прошлого столетия.
Классическими работами в этой области долгое время считались работы Таммана, который исследовал процессы зародышеобразования для 150 различных органических веществ. Тамман придерживался взглядов о возможности самопроизвольного зародышеобразования центров кристаллизации в переохлажденных жидкостях. Большой вклад в теорию зарождения кристаллов внесли работы Фольмера, который получил соотношение для работы образования стабильного кристаллического зародыша внутри переохлажденного расплава. Свободная энергия F образования сферического ядра радиуса г из расплава может быть выражена уравнением
Д/г=4/3яг3Д/Сб + 4лг2з, (2.27)
где Д/об — объемная свободная энергия плавления единичного объема; а — поверхностная свободная энергия единичной поверхности.
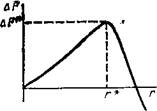
По мере того как радиус зародыша увеличивается, AF сначала увеличивается, достигает максимума при г = г* и затем уменьшается и становится отрицательным (рис. 2.12). В точке максимума г = г* = 2а/(А/об), следовательно,
kF = kF* = -^--------- —. (2.28)
3 (Д/об)2
Если воспользоваться приближенным соотношением А/0б = = АНоб(Тил—Т)/Тия9 то
_ <■ 2аТ цЛ
(2.29)
дяобд т 16rt аЗ т1
LF* = —------ ------ —, (2.30)
3 (ДЯоб)2 (ДГ)2
где разность АГ = ГПЛ—Т характеризует переохлаждение расплава, г* — радиус критического зародыша.
Зародыши с размером меньше критического нестабильны и сно - а переходят в расплав. Зародыши с размером больше критиче - ~ого могут самопроизвольно расти, так как AF с увеличением ра - иуса зародыша уменьшается. Таким образом, AF* есть тот барьер вободной энергии, который должен быть преодолен для того, что - ы образовалась стабильная новая фаза. При малых переохлажде - иях размер критического зародыша весьма большой. По мере величения переохлаждения размер критического зародыша умень - ается и вероятность его возникновения в результате статистиче - ких флуктуаций в переохлажденном расплаве возрастет.
|
|
|
|
Ри«. 2,12 Рис. 2.13
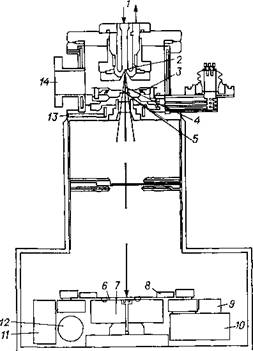
4 Рис. 2.12. Зависимость свободной энергии AF от радиуса кристаллического зародыша г
Рис. 2.13. Изменение числа п зародышей с температурой
При малых переохлаждениях, когда размер критического зародыша очень велик, зародыши могут образовываться только на поверхностях раздела, например на пылинках, поскольку работа образования зародыша на инородной поверхности всегда меньше работы его образования в свободном пространстве и зависит от смачивания инородной поверхности расплавом кристаллизующегося вещества.
Если на поверхности есть углубления или трещины, то работа образования зародыша новой фазы в таком углублении меньше, чем на плоской поверхности. Кроме того, в таких углублениях нерасплавленные кристаллические участки кристаллизующегося вещества сохраняются при таких температурах, при которых в объеме вещества или на плоской инородной поверхности они полностью перешли бы в расплав. Можно выделить четыре основных типа искусственных зародышей кристаллизации:
1) наилучшими затравками служат нерасплавившиеся или вводимые извне частицы самого кристаллизующегося вещества;
2) надежными зародышами кристаллизации являются частицы других веществ, которые изоаморфны с кристаллизующимся веществом и образуют с ним твердые растворы;
3) зародышами кристаллизации могут служить частицы веществ, способных срастаться с кристаллизующимся веществом;
4) наконец, роль искусственных зародышей кристаллизации
могут играть частицы вещества, которые на своей поверхности адсорбируют молекулы кристаллизующегося вещества.
При температуре плавления число зародышей равно нулю, а при увеличении переохлаждения число центров растет, достигая максимума, и дальше число центров уменьшается, достигая нуля (рис. 2.13).
Рост сферолитов на гомогенных зародышах начинается не одновременно в разных точках расплава, а их число и взаимное расположение не зависят от термической предыстории расплава. Гетерогенные зародыши существуют в расплаве полимера до начала процесса структурообразования. Их роль обычно играют нераспла - вившиеся микрокристаллические участки самого полимера. При охлаждении расплава кристаллизация начинается без индукционного периода и практически одновременно на всех гетерогенных зародышах. Размер и число нерасплавившихся микрокристаллических областей быстро уменьшается с повышением температуры или с увеличением длительности выдержки в расплаве, поэтому количество гетерогенных зародышей существенно зависит от термической предыстории расплава полимера. Если в расплаве не происходит разрушения гетерогенных зародышей, то при его охлаждении сферолиты возникает там же, где они находились $о плавления.
Свободная энергия образования цилиндрического гомогенного зародыша, который содержит р молекул в поперечном сечении и g молекул по длине,
Д/7 = 2|Цярзу-(-2ра|— SpA/у, (2.31>
где fu — свободная энергия плавления на одну молекулу; ои — боковая свободная поверхностная энергия на одну молекулу; oi — свободная поверхностная энергия на одну молекулу в основании
цилиндра. Полагая (и (--—Л равными нулю, находим
1р др Д
размер критического зародыша и барьер свободной энергии, который должен быть преодолен для образования стабильного зародыша. При Гпл размер критического зародыша равен бесконечности, а при понижении температуры кристаллизации он резко уменьшается и при больших переохлаждениях достигает чрезвычайно малых значений. В этом случае
|
(2.32) |
ыи 4яо 4 п 4 огГпл
Д/2у (ДЯи)2(ДГ)2 Д /„ ДЯуД Т
В случае зародышеобразования на твердой поверхности в отсутствие сохранившихся в расплаве центров кристаллизации свободная энергия образования поверхностного зародыша критических размеров меньше свободной энергии образования объемного критического зародыша на величину, зависящую от смачивания твердой поверхности полимеров:
bF*=f(Q)bF*,
где 0</(©)<1; © — краевой угол смачивания поверхности полимеров. При понижении температуры кристаллизации возрастает вероятность возникновения зародыша критических размеров и, следовательно, увеличивается скорость гомогенного зародышеобразо - вания. Однако понижение температуры кристаллизации приводит к увеличению вязкости переохлажденного расплава и уменьшению подвижности цепей. Это снижает скорость кристаллизации. Поэтому при охлаждении расплава полимера скорость кристаллообразования сначала возрастает, а затем достигает максимума и начинает уменьшаться.
Турнбулл и Фишер дали следующее выражение для числа зародышей, возникающих в единичном объеме расплава за 1 с при стационарном режиме кристаллизации:
|
|
Здесь Ed — свободная энергия активации перехода кристаллизующихся единиц через границу раздела расплав — зародыш, которая соответствует свободной энергии активации вязкого течения; No — = nkT/n и п{ — число сегментов в единичном объеме расплава. Учитывая, что AF* обратно пропорционально (Гпл—Т)2, находим, что скорость зародышеобразования равна нулю при абсолютном нуле и при Гпл и достигает максимума при какой-то промежуточной температуре. Возникшие зародыши критических размеров начинают расти, поскольку их рост сопровождается уменьшением свободной энергии. В полимерах рост зародышей приводит обычно к образованию сферолитов.
|
(2.34) |
Кинетика кристаллизации полимеров довольно хорошо описывается уравнением Аврами
а= 1 —exp (—ktn).
Здесь а — закристаллизовавшаяся к моменту времени I фракция, k и п — константы, причем значение п зависит от характера зародышеобразования и формы растущих зародышей. Общая скорость кристаллизации влияет на степень совершенства образующейся кристаллической структуры полимера.

 Опубликовано в
Опубликовано в