ДЕЙСТВИЕ ЭЛЕКТРОЛИТОВ НА МЫЛЬНЫЙ КЛЕЙ
 5 декабря, 2012
5 декабря, 2012  admin
admin Электролиты. Это химические вещества или системы, водные растворы которых проводят электрический ток. При растворении электролитов в воде молекулы их распадаются — диссоциируют на электрически заряженные атомы или группы атомов, называемых ионами.
Например, при растворении в воде поваренной соли она диссоциирует на ион Na+ и ион С1_ по уравнению
NaCl Na+ - f CI-.
Знаком (+) обозначают положительно заряженные ионы, знаком (—) —отрицательно заряженные. Процесс диссоциации является обратимым и в зависимости от условий (концентрации и температуры) он может протекать как в сторону диссоциации на ионы (распад молекул на ионы), так и в сторону ассоциации (образование молекул из ионов).
Для каждого вещества отношение количества диссоциированных молекул к их общему количеству в растворе при одинаковых условиях является величиной постоянной и называется константой диссоциации.
Различают сильные и слабые электролиты. В разбавленных растворах сильных электролитов (растворы едких щелочей, поваренной соли, минеральных кислот) константа диссоциации равна 1 (К= 1) или близка к ней, т. е. все или почти все молекулы диссоциированы на ионы.
В слабых электролитах константа диссоциации колеблется от 0 до некоторой величины, которая всегда меньше единицы.
Большинство солей органических кислот, в том числе жирных кислот (мыла), относятся к слабым электролитам.
Высаливание мыльного клея. Процесс обработки мыльного Клея электролитами, сопровождающийся разделением его на фазы, Называют высаливанием.
Сущность процесса высаливания заключается в следующем. Хлористый натрий и едкий натр как сильные электролиты действуют подавляющим образом на диссоциацию самого мыла, т. е. уменьшают количество образующихся ионов RCOO-, а также вызывают разрушение мыльного клея путем выделения из него (коагуляцией) ассоциированных молекул мыла.
Выделяемая при высаливании мыльного клея масса, содержащая меньше воды и больше собственно мыла, называется ядровой фазой, или ядром.
В результате выделения из мыльного клея ядра, содержащего не менее 60% жирных кислот, концентрация оставшегося раствора мыла уменьшается. Этот раствор называется клеевой фазой, или подмыльным клеем.
С увеличением ввода электролита в мыльный клей, т. е. с повышением в ней концентрации электролитов, больше выделяется частиц ядровой фазы и меньше остается клеевой фазы; в последней понижается содержание жирных кислот и повышается содержание электролита.
Понятие о предельной концентрации электролитов. Концентрация электролита в водной фазе мыльного раствора, при которой из него полностью выделяется мыло, называется предельной.
Для каждого электролита, как и для мыла из разной смеси жирных кислот, существует своя определенная предельная концентрация электролита.
В табл. 4 и 5 приведена предельная концентрация электролитов для высаливания мыла, сваренного из отдельных жирных кислот и из различных природных жиров.
Таблица 4
Предельная концентрация электролитов, %
Жирная кислота
|
Едкого натра для натриевого Мыла |
|
Едкого кали для калиевого мыла |
Лауриновая
Миристииовая
Пальмитиновая
Стеариновая
Олеиновая
Линолевая
Эруковая
|
Таблица 5
|
Предельную концентрацию электролита для высаливания мыла,, состоящего из смеси мыл разных жирных кислот, можно вычислить по формуле
ПрстКст + ^Рпал^пал + ПролКол 100
Где /Со —искомая предельная концентрация электролита, %;
Пр, л'—количество стеариновой кислоты в смеси жирных кислот, %;.
Прпап — количество пальмитиновой кислоты в смеси жирных кислот, %;
Пр0ц — количество олеиновой кислоты в смеси жирных кислот, %;
Лет, /Спал, Кол — соответствующие предельные концентрации электролитов - стеариповой, пальмитиновой и олеиновой кислот.
Пример. Определить предельную концентрацию электролита (NaOH) для; высаливания мыла, состоящего из следующей смеси жирных кислот: 50% стеариновой, 10% пальмитиновой и 40% олеиновой.
|
К, |
Для этого в табл. 4 находим предельную концентрацию NaOH для мыл неиндивидуальных жирных кислот и, подставив их в формулу, получим
|
= 3,59 ' |
|
Кэ |
50 - 2,9+10 • 4,6 + 40 ■ 4,2 100
|
Электролиты |
Высаливающее действие различных электролитов колеблется; в довольно широком интервале. Это видно из следующих данных:
Высаливающее действие
|
Едкий натр Хлористый натрий Углекислый » Едкое кали Хлористый калий Углекислый » |
|
1,0 0,87 0,474 1,0 0,76 0,55 |
|
Для натриевых мыл Для калиевых мыл |
Таким образом, для одного и того же высаливающего эффекта надо взять одну часть NaOH, или 1:0,87=1,15 части NaCl, или 1 : 0,474=2,11 части Na2C03 и т. д.
Мыльный клей с небольшим количеством свободной едкой щелочи (0,2—0,3%) для высаливания требует более высокой концентрации хлористого натрия, чем при полном отсутствии свободной щелочи в исходном мыльном клее.
Стабилизирующее действие малых концентраций едкой щелочи (ионов ОН") обусловлено тем, что она при высаливании препятствует гидролизу с образованием кислого мыла, раствор которого в мыльном клее чувствительнее к электролитам, чем раствор нейтрального мыла.
Понижение температуры при высаливании мыльного клея (ниже 100°С) повышает высаливающее действие электролита. При температуре более 100°С эффект высаливания электролита понижается и при очень высокой температуре мыльный клей практически не поддается высаливанию.
Содержание неомыленного жира в мыльном клее повышает чувствительность последнего к высаливающему действию электролитов: пережиренное мыло высаливается при концентрации электролита ниже предельной, но при этом загрязнения и красящие вещества адсорбируются (поглощаются) образующимися мылами. Очистительный эффект высаливания не достигается.
Содержание глицерина в мыльном клее повышает предельную концентрацию электролита: при 5% — на 0,5%, при 10% на 1%.
Снижение концентрации самого мыла (в пересчете на жирные кислоты) с 52 до 40% в мыльном клее действует так же, как уменьшение концентрации электролитов.
Фазовые превращения в мыльном клее. Нормальный мыльный клей, как указывалось выше, содержит некоторое количество электролитов, обеспечивающих соответствующую вязкость, подвижность и однородность (гомогенность) его.
Если концентрацию электролитов в мыльном клее уменьшать, то вязкость, температура затвердевания и другие свойства его будут изменяться: масса станет гуще и при снижении концентрации электролитов до определенной величины, соответствующей молекулярной массе и концентрации самого мыла, мыльный клей превращается в студнеобразную нетранспортабельную массу.
На практике это происходит в тех случаях, когда при омылении жиров задерживается подача в мыльную массу щелочи и соли, а также при неосторожной загрузке воды (струей). При этом в мыльной массе происходит местное резкое снижение концентрации электролита, в результате чего образуются комки (сгустки) так называемого среднего мыла. Это удлиняет процесс варки из-за необходимости дополнительно разваривать эти комки.
Если же содержание электролитов в мыльном клее увеличивать, то вязкость его сначала понижается, а затем увеличивается. Происходят и другие, вначале незаметные для глаз, изменения состава и свойств. Мыльный клей разжижается, мутнеет, пере
стает давать нити, гомогенность его нарушается. В мыльной массе образуются две фазы — ядровая и клеевая. При последующем - повышении концентрации электролитов происходят дальнейшие изменения в фазовом состоянии.
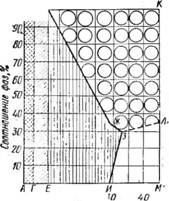
На рис. 4 приведена диаграмма фазовых превращений мыльного клея под воздействием электролитов.
Из диаграммы видно, что при концентрации электролитов & мыльном клее в пределах до 0,5'% последний представляет собой* студнеобразную плотную массу (на диаграмме эта зона ЛБВГ). При повышении концентрации электролитов • от 0,5 до 1% мыльный клей представляет собой жидкую гомогенную массу (на диаграмме это зона ГВДЕ). При концентрации электролитов выше 1 % наступает момент, когда мыльный клей мутнеет, гомогенность его нарушается и образуются две фазы-—незначительное количество ядровой и остальная, большая, часть — клеевой, еще мало отличающейся по свойствам и составу от исходного мыльного клея. Увеличение концентрации электролита до 3% вызывает дальнейшее высаливание мыльного клея; количество ядровой фазы увеличивается, а количество клеевой фазы снижается до 34% по отношению к общей мыльной массе (на диаграмме это зона
ЕДЖИ). При концентрации 3,0% в точке Ж зарождается новая фаза — водная (раствор электролита). При дальнейшем повышении концентрации электролита до 3,5% из системы полностью исчезает клеевая фаза; мыльная масса в это время состоит примерно из 70% ядровой фазы и 30°/0 водной. В этой точке (3) концентрация электролита в водной фазе достигает предельной. На диаграмме зона ДЖЗЛК. является ядровой фазой, а зона ИЗЛМ — водной (раствор электролитов — подмыльный щелок).
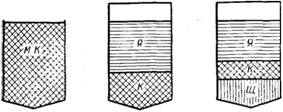
На рис. 5 приведена диаграмма различного фазового состояния мыльного клея.
При хорошем перемешивании и температуре около 100°С в результате действия на мыльный клей электролитов могут образоваться следующие фазовые системы: I — мыльный клей (однофазная); II — ядро — подмыльный клей (двухфазная); III — Ядро — подмыльный клей — подмыльный щелок (трехфазная) и - IV — ядро — подмыльный щелок (двухфазная).
|
Б В Д |
|
0.5 1J0 . . ■ лпчнрнтртщя Электролитов, %, |
|
Рис. 4. Диаграмма фазовых превращений мыльного клея - под действием электролитов. |
Характеристика фаз при высаливании. Свойства и состав ядровой, клеевой и водной фаз, получаемых при высаливании мыльного клея, зависят от молекулярной массы и йодного числа жировой смеси мыла; от характера жировой смеси (нейтральные
жиры, расщепленные жиры, синтетические жирные кислоты, жирозаменители); от концентрации электролита в мыльной массе при высаливании; от температуры при высаливании.
Ядровая фаза (ядровое мыло) содержит от 60 до 65'% мыЛа (в пересчете на жирные кислоты). Остальное количество приХодится на водный раствор электролитов и глицерин.
|
Рис. 5. Различное фазовое состояние мыльного клея при высаливании в мыловаренном котле: |
|
Щ |
|
Ш |
МК—мыльный клей; Я — ядровая фаза (ядровое мыло); К — клеевая фаза (подмыльный клей); Щ — водная фаза (подмыльный щелок).
Каждая жировая смесь при высаливании мыльного клея имеет свой предел содержания жирных кислот в ядровой фазе. Минимальное содержание — в начале высаливания, максимальное — к концу.
Чем выше концентрация электролита при высаливании, тем меньше воды содержится в ядровой фазе и больше мыла. С другой стороны, чем выше молекулярная масса жировой смеси, т. е. чем больше в ней ядровых жиров, тем большее количество воды удерживается ядровой фазой и, следовательно, меньше в ней собственно безводного мыла. Например, ядровая фаза мыла, сваренного из жировой смеси, в которую входят одни высокомолекулярные жирные кислоты, содержит 60—62% мыла (в пересчете на жирные кислоты). При добавлении в эту смесь 10—20% жирных кислот с более низкой молекулярной массой (клеевых жиров) концентрация ядровой фазы повышается до 64—65% мыла (в пересчете на жирные кислоты).
Клеевая фаза (подмыльный клей) содержит мыла всегда меньше, чем исходным мыльный клей перед высолкой. Концентрация мыла в клеевой фазе также зависит от молекулярной массы смеси жирных кислот. В смеси из одних ядровых жиров нижний предел содержания жирных кислот всегда выше, чем у мыла, сваренного из смеси ядровых и клеевых жиров. Наименьшее содержание жирных кислот в подмыльном клее составляет примерно 10%, наибольшее — на несколько процентов меньше, чем в исходном мыльном клее.
Водная фаза (подмыльный щелок) содержит растворенное мыло преимущественно низкомолекулярных жирных кислот в
пределах от 0,05 до 1% (иногда выше), едкий натр 0—0,1 °/о, углекислый натрий 0,5—1'%, сернокислый натрий до 0,5%, хлористый натрий до предельной концентрации. Общая концентрация всех электролитов соответствует предельной с колебаниями ± 1 % ■ В подмыльном щелоке глицерин содержится в незначительном количестве (следы) при переработке расщепленных жиров и до 15% при варке мыла из нейтральных жиров. В водную фазу переходит значительная часть загрязнений сырья и материалов.
Приведенный состав фаз при высаливании соответствует температуре проведения процесса, близкой к 100°С. Если высаливание вести при более низкой температуре, то предельная концентрация электролитов понижается; при этом одновременно изменяются состав фаз и их вязкость. Содержание мыла и электролитов в ядровой фазе уменьшается.
Подмыльный клей ниже оптимальной концентрации, слитый из котла и охлажденный примерно до 20° С. самопроизвольно (без дополнительного ввода электролитов) высаливается и разделяется на ядровую и водную (подмыльный щелок) фазы. '
В свою очередь подмыльный щелок, отделившийся высалива - тшем при температуре ниже 100°С, имеет концентрацию электролитов ниже предельной. Охлаждение этого щелока до температуры примерно 20°С сопровождается выделением значительной части растворенного в нем мыла, а также некоторых загрязнений.
Фракционирование мыл при высаливании. При высаливании мыльного клея, сваренного из смеси жирных кислот с разной молекулярной массой, происходит незначительное их фракционирование. При этом в ядровую фазу переходит больше мыла высокомолекулярных жирных кислот, в то время как подмыльный клей обогащается мылами низкомолекулярных жирных кислот. Так, например, при разделении мыльного клея, сваренного из 80% животных топленых жиров и 20% кокосового масла и имеющего среднюю молекулярную массу жирных кислот 258,5, в ядровую фазу перешло мыло со средней молекулярной массой 259,6, а в клеевую — 252,4.
Распределение электролитов между ядровой и водной фазами. Концентрация электролита в ядровой фазе после полного высаливания мыльного клея составляет от '/s до '/ю концентрации, найденной в водной фазе (подмыльном щелоке), и не распределяется пропорционально содержанию воды в этих фазах. Это связано с тем, что мыло способно адсорбировать (поглощать) некоторое количество электролитов.
Распределение глицерина между ядром и подмыльным щелоком. Глицерин, выделившийся в результате омыления триглицери - дов, в основном переходит в водную фазу, за исключением небольшого количества, удерживаемого мылом.
Для практических расчетов принимают, что при полной высол - ке глицерин распределяется между ядровой фазой и подмыльным щелоком пропорционально количеству воды в каждой из фаз. Тогда приближенная зависимость между концентрацией глицерина в ядре и подмыльном щелоке может быть представлена уравнением
* = 0,32i/,
Где х — концентрация глицерина в ядре, %;
У— концентрация глицерина в подмыльном щелоке, %;
0,32 — коэффициент распределения глицерина между ядровой и водной фазами.
Пример. 1. Найти содержание глицерина в ядровой фазе, если в подмыльном щелоке после высаливания содержится его 8%.
Подставив известную величину у в формулу, получим, что глицерина в. ядре находится
Х = 0,32 • 8 = 2,56%.
2. Известно, что в ядровой фазе глицерина содержится 1%, тогда в подмыльном щелоке, согласно формуле, содержание глицерина должно быть:
_ Х 1___
У~ 0,32 ~ 0,32 - '
Высаливание мыльного клея разными электролитами. При
Высаливании калиевого мыла хлористым натрием происходит частичное замещение катиона калия на катион натрия с превращением калиевого мыла в натриевое, и наоборот.
Количественные соотношения образующихся в смеси натриевых и калиевых мыл при этих процессах зависят от состава жирных кислот и концентрации разноименных электролитов.
Понятия об оптимальных условиях при частичном высаливании мыльного клея. Под оптимальными условиями при частичном выСаливании мыльного клея понимают сумму факторов, которые обеспечивают наиболее быстрое и полное разделение фаз на ядро и подмыльный клей при отстаивании.
Оптимальная концентрация электролита зависит от содержания жирных кислот в мыльном клее перед высолкой, от жирно - кислотного состава мыла и от температуры. Сочетание всех этих факторов определяет оптимальные условия при высаливании.
Для нахождения оптимальной концентрации электролитов при высаливании необходимо учитывать изменения физико-химических свойств фаз, происходящие под действием электролитов, и влияние ■этих свойств на скорость разделения фаз.
На диаграмме фазовых превращений мыльного клея (см. рис. 4) в точке Д начинается образование двух фаз: ядровой и клеевой. Ядровая фаза содержит минимум мыла (около 60% жирных кислот) и электролитов, вследствие чего вязкость ее также минимальная. Клеевая фаза в этой точке содержит максимум мыла (всего на 1—2% меньше жирных кислот, чем в исходном мыльном клее) и минимум электролитов (несколько выше концентрации их в исходном мыльном клее). Вследствие этого вязкость и плотность клеевой фазы еще мало отличаются от тех же свойств ядровой фазы. При этих условиях время, необходимое для разделения фаз, значительно.
При дальнейшем повышении концентрации электролитов в ■мыльной массе содержание мыла и электролитов в ядровой фазе также увеличивается и одновременно повышается ее вязкость. Изменения, происходящие в клеевой фазе, заключаются в том, что В ней уменьшается содержание мыла и увеличивается содержание электролитов. При этом плотность клеевой фазы повышается, а вязкость снижается.
Таким образом, благодаря возрастающей разнице в вязкости И плотности ядровой и клеевой фаз время, необходимое для их Разделения, соответственно сокращается.
Практически установлено, что при дальнейшем повышении концентрации электролитов в мыльной массе, например до уровня, при котором образуются три фазы (ядровая, клеевая и водная), время разделения ядровой и клеевой фаз снова увеличивается. Это объясняется тем, что значительное повышение вязкости ядровой фазы в точке образования трех фаз (на рис. 4 точка Ж) Задерживает отделение клеевой фазы, несмотря на максимальную разницу плотностей между клеевой и ядровой фазами.
Следовательно, оптимальной является концентрация электролитов в мыльной массе, несколько меньшая той, которая ведет к образованию трехфазного состояния. Оптимальная концентрация обеспечивает условия, при которых требуется минимальное время для полного разделения фаз с получением ядра и подмыльного клея.

 Опубликовано в
Опубликовано в