Характеристика методов хроматографии
 5 ноября, 2013
5 ноября, 2013  admin
admin Одним из ярких важных научных достижений XX века является хроматографический метод, открытый русским ученым М. С. Цветом в 1903 г. (о жизни и деятельности Михаила Семеновича Цвета можно прочитать в монографии [1]) и благодаря высокой эффективности нашедший чрезвычайно широкое применение. Хроматограф - один из первых научных приборов, побывавших на других планетах, он применялся для анализа состава атмосферы Марса.
Хроматография является методом не только разделения сложных смесей (аналитическая хроматография) [2], но и определения физико-химических характеристик веществ и методом концентрирования (препаративная хроматография) [3]. Препаративная разделительная колонка должна иметь достаточно большую допустимую удельную нагрузку. С этой целью поперечное сечение колонки следует увеличить и заполнить колонку подходящей насадкой. Для того чтобы разделенные вещества можно было легко выделить в чистом виде, подвижная фаза (а в случае распределительных систем и растворенная в подвижной фазе неподвижная фаза) должна быть летучей. Степень разделения в препаративной хроматографии всегда меньше, чем в аналитической, и из-за неизбежного использования длинных разделительных колонок длительность анализа также всегда больше [4].
Универсальные способности делают хроматограф незаменимым прибором для контроля протекания технологических процессов - особенно на тех производствах, где в реакции вовлекаются сложные смеси [5]. Например, на нефтехимических предприятиях расходы на приобретение хроматографа окупаются за одну неделю.
С помощью хроматографии решаются следующие задачи [6]:
• Оценка качества исходного сырья и материалов. Необходимо учитывать, что применяемые в производстве и переработке полимеров сырье и материалы относятся к высокомолекулярным и термически неустойчивым системам, которые не могут быть проанализированы прямым хроматографическим методом, поскольку не могут быть переведены в парообразное состояние. Но в то же время такие продукты, как мономеры, растворители, стабилизаторы фенольного и аминного типа, пластификаторы, модификаторы и др., обладают достаточной летучестью и термостабильностью, и для их анализа применяются газохроматографические методы.
• Определение влаги в сырье и материалах с помощью прямых и косвенных хроматографических методов. Прямые методы основаны
на отделении воды от компонентов анализируемой смеси в хроматографической колонке с последующим измерением концентрации воды катарометром. Косвенные методы основаны на связывании воды в летучие органические соединения, количество которых измеряется хроматографическим методом с применением пламенноионизационного детектора,
• Оценка качества полупродуктов по составу и контроль процессов их производства, в том числе процессов полимеризации и поликонденсации.
• Контроль качества готовой продукции. Особенности определения летучих примесей, которые содержатся в эластомерах и латексах, связаны с гетерогенностью системы и физическим состоянием образца и сводятся к количественному выделению их из пробы. Выделение примесей может осуществляться как вне хроматографа, так и непосредственно в нем. В первом случае используют методы экстракции (для анализа малолетучих соединений типа полимеров и высокомолекулярных добавок), растворения с последующим осаждением полимера (выделение летучих соединений из растворимых образцов и анализ
маточного раствора, получаемого после осаждения полимера из раствора органическим растворителем, например, при анализе стабилизаторов фенольного типа), отгонки с водяным паром (при определении остаточных мономеров), термической десорбции (при воздействии температуры и потока газа на полимер десорбированные примеси собирают в охлажденной ловушке и анализируют полученный конденсат), сочетание жидкостной и газовой хроматографии. Во втором случае наиболее часто используют методы прямого ввода проб в [хроматограф, снижающие продолжительность и трудоемкость опера - ший за счет исключения стадии подготовки образца, количество испытуемого материала, увеличивающие точность определения, а также шетод термической десорбции, обладающий высокой чувствительностью.
V Определение микроструктуры полимеров осуществляют методами реакционной и пиролитической газовой хроматографии, а также пу - рем сочетания химических реакций, проводимых вне хроматографа, с Последующим газохроматографическим анализом продуктов реакции. Кля этой же цели используют хроматографические анализаторы эле- рентного состава, разделяющие оксиды азота, углерода и воду, обращающиеся при сжигании образца.
■ Измерение молекулярной массы полимеров с помощью методов ■бращенной газовой и гельпроникающей хроматографии. Поскольку Рервый метод трудоемок в связи с необходимостью приготовления ■ррбента для каждого измерения, он применяется только для определения молекулярной массы и ММР низкомолекулярной части каучу - ■ов и олигомеров.
Щ Измерение объемов удерживания стандартных соединений при Рспользовании в качестве сорбента или неподвижной жидкой фазы иолимеров при различных температурах вблизи температурных переродов исследуемых полимеров позволяет оценить значение темпера - руры стеклования и исследовать кинетику кристаллизации полимера.
■Качественная оценка газопроницаемости. Для этого используют ■двухкамерные устройства, в которые помещают исследуемый ■образец. Пробу газа после диффузии через испытуемый материал ■отбирают шприцем и вводят в хроматограф. С этой целью разработан
■ специальный прибор - хромопласт, работающий как в статическом, |так и в динамическом режиме.
р Исследование и контроль загрязнения окружающей среды (возду - ка производственных помещений, промышленных выбросов и сточных вод, санитарно-химическая оценка полимерных материалов).
Энциклопедия полимеров (Т. З,С.838) приводит наиболее полную схему, обобщающую возможности хроматографии в сочетании с другими методами исследования полимеров. Ее дополняет обзор новых хроматографических методов для анализа полимеров [7].
Хроматография - метод разделения веществ и определения их физико-химических характеристик, основанный на различных скоростях движения зон веществ в потоке одной фазы, движущейся относительно другой, а также на различной способности компонентов анали зируемой смеси распределяться между двумя несмешивающимися фазами, одна из которых - слой с большой поверхностью, а другая - поток {элюент). При перемещении смеси веществ потоком инертного газа или жидкости (подвижная фаза) вдоль слоя сорбента (неподвижная фаза) соединения различной природы перемещаются с различными скоростями, зависящими от степени их взаимодействия с обеими фазами. При достаточной длине слоя сорбента это приводит к образованию в подвижной фазе отдельных зон каждого компонента смеси. Раствор, выделяющийся из слоя неподвижной фазы и содержащий растворенные компоненты смеси, называют элюатом [8, 9, 10].
Объем элюента, необходимый для извлечения из колонки максимальной концентрации вещества, называют объемом удерживания VR. Время от момента ввода пробы в колонку до момента выхода из нее максимальной концентрации определяемого вещества называют временем удерживания tR. Объем удерживания равен произведению времени удерживания на объемный расход элюента W при температуре и давлении колонки:
VR = iR-W,
В хроматографии высота полосы, эквивалентная теоретической тарелке (ВЭТТ), определяется для одного компонента при заданной скорости элюента, постоянной температуре и постоянном соотношении фаз по записанной хроматограмме:
h = Lw2f(16t$y
где Z-длина колонки; w-ширина пика у основания, равная отрезку, отсекаемому на основании двумя касательными, проведенными к пику.
Как и в дистилляции, в хроматографии используют понятие числа эквивалентных теоретических тарелок п:
п = L/h ~ 16 tR /w2.
Однако если два компонента имеют одинаковые значения к’, их нельзя разделить даже на колонке с 10000 тарелками. Величина к! называется объемным 3 или массовым, отношением распределения и равна отношению времен удерживания в неподвижной и подвижной фазах:
к’ = tR’/10 = (tR-tJ/to,
Поэтому для описания разделительной колонки лучше использовать эффективную высоту //, эквивалентную теоретической тарелке, или эффективное число теоретических тарелок N:
H = h(l +к)2/к'2 =Lw2/(16tg-)2;
N = пка / (I + к')2 = 16 /W ■
Эффективная высота, эквивалентная теоретической тарелке, или число тарелок являются для каждой пробы константами, если в колонке под держиваются постоянные условия.
Величины хроматографического удерживания могут быть найдены в специальной литературе, справочниках, а также в автоматизированных банках данных [11].
Разделение двух полос определяется расстоянием между максимумами пиков (выраженным как разность времен удерживания) и средней арифметической шириной обоих пиков у основания:
R=2 (Ir2 - tR]) / (Wj + W]).
В хроматографии стремятся не к наибольшему, а только к оптимальному разделению, т. е. пики должны отстоять друг от друга на требуемом расстоянии. Разделение двух пиков целесообразнее улучшать, увеличивая относительное удерживание, а не число тарелок. Удвоение числа тарелок, достигаемое в результате удвоения длины колонки, улучшает разделение примерно в 1,4 раза. При этом удваивается время удерживания и вместе с ним продолжительность анализа. Разделительную систему всегда следует выбирать таким образом, чтобы относительное удерживание было как можно большим, т. е. чтобы разделительная система была очень селективной.
|
Рис.3.1 |
В «магическом треугольнике» хроматографии можно проводить оптимизацию только в одном направлении, причем чем больше проводят оптимизацию в одном направлении, тем дальше удаляются от двух других параметров. Еще не описана такая система, в которой высокое разрешение сочеталось бы с большой предельной допустимой нагрузкой и возможностью быстрого разделения.
Хроматографические сорбционные методы различаются по следующим признакам: в зависимости от агрегатного состояния среды, в которой производится разделение, различают газовую, газожидкостную и жидкостную хроматографию. В качестве подвижной фазы используют газ [12], флюид [13] или жидкость [14, 15]. По-видимому, в будущем будет также возможно использовать в качестве подвижной фазы поток ионов или других заряженных частиц.
В качестве неподвижной фазы можно использовать: твердую фазу (адсорбент), жидкую фазу, нанесенную на твердую фазу, газовую фазу, расположенную на поверхности твердого тела, в том числе в его микропорах. Неподвижные фазы могут различаться также по природе сорбционного взаимодействия с молекулами разделяемой смеси, которое может заключаться:
О в концентрировании вещества на границе раздела фаз вследствие адсорбции;
О в удержании вещества вследствие хемосорбции;
О в избирательном растворении компонентов смеси - абсорбция;
О в задержании одних растворенных веществ и пропускании других в зависимости от размеров и формы их молекул - молекулярные сита.
В зависимости от природы взаимодействия компонентов с подвижной и неподвижной фазами различают следующие основные типы хроматографии:
• Адсорбционная хроматография (газоабсорбционная и жидкостно-адсорбционная) - основана на различии в адсорбции веществ данным адсорбентом - твердым веществом с развитой поверхностью и активными центрами, способными к обратимому взаимодействию с молекулами разделяемой смеси.
растворимость компонентов смеси в подвижной фазе (газ или жидкость) и несмешивающейся с ней жидкости, неподвижно закрепленной на пористом инертном наполнителе. В равновесных условиях различие в растворимости приводит к различному соотношению концентраций в обеих фазах, определяемому коэффициентом распределения. Выбирая системы для разделения методом распределительной хроматографии, можно ориентироваться на уже известные системы распределения, применяемые при экстракционном разделении. Более полярный компонент системы обычно наносят на носитель, а менее полярный служит элюентом. Методом распределительной хроматографии целесообразнее всего проводить разделение соединений, полярность которых слишком велика, чтобы их можно было разделить с помощью адсорбционной хроматографии. Однако этим методом можно разделить и неполярные вещества, например многоядерные ароматические углеводороды. Анализ пластификаторов, неионогенных поверхностно-активных веществ можно провести как с помощью распределительной, так и адсорбционной хроматографии,
• Ионообменная хроматография. Неподвижная фаза - ионит, характеризуемый различными константами ионообменного равновесия по отношению к компонентам разделяемой смеси. Применяется в анализе природных и сточных вод, атмосферных осадков, газовых выбросов, технологических растворов и материалов, фармацевтических препаратов, биологических жидкостей, продовольствия и др. [16]. Анализируемыми объектами могут быть жидкие, твердые и газообразные образцы (в последнем случае требуется соответствующая подготовка пробы). Метод может применяться для определения как низких, так и высоких концентраций ионов.
подвижной фазой служат полимерные окислители или восстановители (например, смолы с окислительно-восстановительными свойствами, молекулы которых содержат звенья гидрохинона или метиленового голубого), способные активно окислять или восстанавливать компоненты подвижной фазы.
• Хромато-мембоанные методы основаны на использовании капиллярных эффектов в пористых гидрофобных средах. В них хроматографический механизм межфазного обмена совмещается с принципом раздельного прохождения потоков двух фаз через зону массо - обмена - пористые мембраны. Применяются для непрерывного разделения веществ в системах жидкость-жидкость и жидкость-газ.
• Электрофорез. Компоненты смеси ионов на твердом носителе (например, фильтровальная бумага или колонка с наполнителем, насыщенные проводящим буферным раствором) мигрируют с различными скоростями и разделяются на зоны под действием постоянного или переменного электрического поля, прикладываемого к носителю.
• Гелъ-фильтрапия и гелыгроникающая хроматография основаны на разделении веществ по размерам молекул (молекулярное “просеивание”) с использованием гелей, приготовленных из соединений с известным размером пор или известной пористостью.
• Осадочная хооматогоаФия основана на различной способности разделяемых компонентов выпадать в осадок на твердой неподвижной фазе [18].
• Полевая (несорбнионяаяУ хроматография - движение концентрационных зон хроматографируемых веществ (частиц) в потоке подвижной фазы, которая движется в поперечно направленном поле сил [19]. Ее разновидностью может выступать оптическая хроматография [20]. Несмотря на то, что основные уравнения для оценки характеристик этого метода выводятся на основе лучевой оптической модели, для него действительны такие понятия, как время удерживания, селективность, число теоретических тарелок, коэффициент разделения, оптимальные условия разделения. Один из примеров использования метода - определение соотношения между скоростью движения сферических частиц полистирола и интенсивностью приложенных радиальных сил при отсутствии каких-либо других воздействий
на поток. Установлено, что радиальная сила максимальна в точке фокуса луча и пропорциональна энергии лазера и квадрату размера частиц при условии, что их диаметр много меньше диаметра лазерного* луча. Теоретически возможно, путем увеличения энергии лазера и уменьшения скорости потока, различать частицы, отличающиеся по диаметру менее чем на 1 %.
По форме проведения процесса различают методы колоночной (микроколоночной), капиллярной и плоскостной хроматографии (рис.3.2). . В колоночном варианте сорбентом заполняют специальные трубки - колонки, а подвижная фаза движется внутри колонки благодаря перепаду давления. В капиллярной хроматографии тонкий слой сорбента нанесен на внутренние стенки капилляра. В плоскостной (тонкослойной) хроматографии тонкий слой гранулированного сорбента или пористая пленка наносится на пластинку, перемещение подвижной фазы происходит благодаря капиллярным силам.
Для повышения чувствительности обнаружения широко используются методы концентрирования. Весьма перспективны неэлю - ентные хроматографические методы концентрирования, а именно: фронтальная и вытеснительная хроматография, хроматотермография, элюентно-тепловытеснительные варианты и др. [21].
|
Рис.3.2. Виды хроматографических процессов -55- |
Для получения воспроизводимых результатов следует тщательно фиксировать условия и режим хроматографирования [22]. Запись рекомендуется вести следующим образом: марка прибора, тип детектора, длина и внутренний диаметр колонки, газ-носитель и его
|
|
|
Рис.3.3. Схема блоков газового (жидкостного) хроматографа |
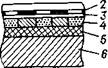
Принципиальная схема газового или жидкостного хроматографа показана рис.3.3 - Установка и стабилизация скорости потока газа и очистка газа-носителя и дополнительных газов (если они необходимы для питания детектора), а также измерение скорости потока газа выполняются системой подготовки газов 1. Особенно важное значение имеет установка и стабилизация расхода газа-носителя, оказывающего непосредственное влияние на параметры удерживания и размеры пиков на хроматограмме. Дозирующее устройство 2 позволяет вводить в поток газа-носителя непосредственно перед колонкой определенное количество анализируемой смеси в газообразном состоянии. Поток газа-носителя вносит анализируемую пробу в колонку 3, где осуществляется разделение смеси. Выходящий из колонки газовый поток содержит зоны отдельных компонентов, разделенные зонами чистого газа-носителя и отличающиеся от них по электропроводности, плотности и другим параметрам. Измерение этих параметров на выходе из колонки непрерывно регистрируется детектором 4, который преобразует разницу в физических или физико-химических свойствах бинарных смесей компонент - газ-носитель по сравнению с чистым газом-носителем в электрический сигнал. Величина сигнала зависит как от природы компонента, так и от содержания его в анализируемой смеси. Необходимые температурные режимы колонки, детектора и дозирующих устройств достигаются помещением их в термостат, управляемый терморегулятором 5. Сигнал детектора, преобразованный усилителем 7, записывается в виде хроматограммы автоматическим потенциометром 8. Конструктивно испаритель, термостат, колонку и детектор объединяют’ в блоке анализатора.
Если хроматограф используется для препаративных целей, в него входит узел 6 для сбора отдельных компонентов (коллектор фракций) [23]. Устройства для сбора отдельных фракций необходимы для того, чтобы можно было определить растворенные составные части пробы. Однако при наличии современных чувствительных детекторов они практически не нужны; только в особых случаях (например, при измерении радиоактивности и др.) собирают отдельные фракции, либо имеющие постоянный объем, либо собранные за определенный промежуток времени.
Хроматографический анализ прежде всего дает возможность получить информацию о числе компонентов в исследуемой смеси. Обычно считается, что каждый пик на хроматограмме соответствует отдельному компоненту, а площадь каждого пика характеризует относительное содержание данного компонента. Следует учитывать, что число пиков на хроматограмме смеси неизвестного состава необязательно соответствует числу содержащихся в ней компонентов, поскольку из-за совпадения характеристик удерживания пики соединений могут налагаться, некоторые вещества при данных условиях анализа могут распадаться или необратимо удерживаться в колонке. Основными характеристиками пиков являются удаленность их центров тяжести от точки, отмечающей момент ввода образца в хроматограф {tg) а также ширина пика Шо5 (рис.3.4, 3.5). Положение пиков можно характеризовать либо временем выхода соответствующих компонентов образца, либо удерживаемым объемом. Степень хроматографиче
ского разделения обычно оценивают отношением расстояния между максимумами пиков двух веществ к сумме их полуширины.
Качественный состав смеси определяют путем сопоставления времен удерживания данного компонента и эталона - вещества известной структуры. При строгом соблюдении всех условий анализа время удерживания является такой же физико-химической характеристикой вещества, как его плотность, показатель преломления и т. д.
|
Рис.3.5. Определение параметров не полностью разделенных пиков |
Обычно используют так называемое исправленное время удерживания tR' - интервал между выходом максимумов пиков несор - бирующегося вещества и исследуемого соединения (рис.3.4). При постоянной скорости движения диаграммной ленты времена удерживания обычно описывают в единицах длины. Совпадение времен удерживания эталона и определяемого соединения может указывать на их идентичность. Эталон чаще всего добавляется в исследуемую смесь (метод метки), при этом число пиков на хроматограмме не должно изменяться, а интенсивность пика одного из компонентов должна увеличиться. Идентификация считается достаточно достоверной, если такое совпадение наблюдается при использовании по крайней мере трех неподвижных жидких фаз различной полярности.
А
Рис, 3.4. Определение параметров хроматографического пика: 1 - ввод пробы; 2 - пик несорбирую - щегося компонента; 3 - пик сор-
бирующегося компонента
Для количественного определения разделенных компонентов зависимость сигнала детектора (отклонение показаний самописцев или прибора индикатора) от концентрации компонента устанавливают с помощью калибровки. При этом фиксируют зависимость высоты пика, произведения высоты на время удерживания или, чаще всего, площади пика от количества стандартного вещества, подаваемого в Колонку. Расчет производится путем деления избранного параметра Пика на сумму соответствующих параметров всех пиков на хроматограмме:
Сл = • 100% ,
Однако такой метод дает правильные результаты только при близком химическом строении анализируемых веществ (изомеров или членов одного гомологического ряда). При точных расчетах вводят поправочные коэффициенты, которые определяют при хроматографировании специально приготовленных смесей известного состава.
Площадь хроматографического пика П - Шо 5 • Н
где Н - высота пика; Шо,5 - ширина пика на половине его высоты.
При расчете площадей неполностью разделенных пиков (рис.3.5) применяют соотношение:
П = 0,5Ш0,5 *2Н.

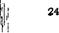
 Опубликовано в
Опубликовано в