СИСТЕМЫ ХРАНЕНИЯ И ПОДГОТОВКИ. РЕАГЕНТОВ (СХПР)
 17 декабря, 2016
17 декабря, 2016  Mihail Maikl
Mihail Maikl 8.1. ОБЩАЯ ХАРАКТЕРИСТИКА СХПР
В предыдущих главах были рассмотрены проблемы создания собственно ЭХГ. Как отмечалось, одно из принципиальных отличий ЭХГ от гальванических элементов и аккумуляторных батарей состоит в том, что активные вещества — топливо и окислитель не заложены в источнике, а подводятся непрерывно к электродам извне в течение всего периода работы генератора. Поэтому обязательной составной частью любого типа ЭУ на основе ЭХГ является система хранения и подготовки реагентов.
Эти системы могут быть классифицированы следующим образом:
1. СХПР с газообразными реагентами, в которых топливо и окислитель хранятся в виде сжатых газов и подаются непосредственно в ЭХГ.
2. СХПР с криогенными реагентами, в которых топливо и окислитель хранятся в ожиженном состоянии и перед подачей в ЭХГ газифицируются.
3. СХПР с реагентами в химически связанном состоянии, в которых топливо и окислитель хранятся в виде жидких или твердых водородсодержащих (кислородсодержащих) соединений и перед подачей в ЭХГ из них предварительно выделяется чистый водород (кислород) путем соответствующего химического процесса.
Несколько особняком стоит в этой классификации СХП водорода, в которой он предварительно сорбирован некоторыми интерметаллическими соединениями и выделяется в газообразном состоянии при их дегидрировании.
В схемно-конструктивном отношении наиболее простой является СХПР с газообразными реагентами, так как они хранятся в готовом к подаче в ЭХГ виде. Такая СХПР, в принципе, состоит из баллонов высокого давления (15—50 МПа) и системы редуцирования.
Наиболее существенным недостатком, ограничивающим применение баллонной системы хранения, является большая относительная масса металлических баллонов 23* 355
|
Тип и материал баллонов |
гсст |
Давление, МПа |
|
Б-150 (из - углеродистой стали) |
ГОСТ 949-73 |
15 |
|
Б-200 (из углеродистой стали) |
ГОСТ 949-73 |
20 |
|
Б-150Л (из легированной стали) |
ГОСТ 949-73 |
15 |
|
Б-200Л (из легированной стали) |
ГОСТ 949-73 |
20 |
|
Б-320Л (из легированной стали) |
ГОСТ 12247-66 |
32 |
|
Б-400Л (из легированной стали) |
ГОСТ 12247-66 |
4 0 |
|
Б-500 (из стали 20ХНГФА, |
ТУ ВНИТИ 861-69 |
50 |
|
армированные стеклопласты- |
||
|
ком) |
на 1 м3 газа. По этой причине для большинства задач стандартные баллоны не подходят.
В настоящее время как в нашей стране, так и за рубежом имеются облегченные баллоны на 30—50 МПа, которые могут быть использованы для хранения реагентов. Они изготавливаются из специальных легированных сталей с высоким пределом прочности и армированы стекловолокном. Стекловолокно имеет значительно большее сопротивление на разрыв, чем сталь, поэтому удается получить более прочный и легкий корпус.
Очевидно, что с повышением давления снижается объем баллонов. Однако повышение давления сильно усложняет их заправку газом (требуются специальные компрессорные станции), усложняется транспортировка, снижаются сроки хранения заправленных баллонов и, следовательно, ухудшаются технические свойства всей энергоустановки.
В табл. 8.1 приведены характеристики отечественных баллонов высокого давления при значениях удельного расхода в ЭХГ кислорода 0,4 кг/(кВт-ч) и удельного расхода водорода 0,05 кг/(кВт-ч).
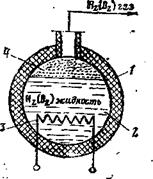
Наиболее компактна и схемно достаточно проста СХПР с криогенным хранением реагентов — криостат и система газификации (рис. 8.1); однако в этом варианте возникает проблема удержания реагентов в сжиженном состоянии при длительном хранении для предотвращения потерь реагента.
Основное преимущество этого способа хранения перед баллонным — небольшая масса. Газы в сжиженном состоянии имеют максимальную объемную плотность, однако необходимость мощной теплоизоляции и газовой «подушки» над жидкостью резко снижает объемные характеристики. В то время как массовые характеристики 356
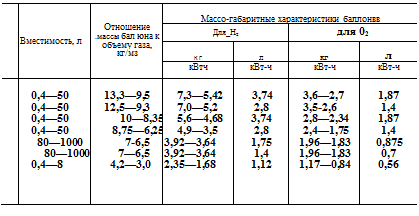
могут быть в 2—3 раза лучше, чем у баллонов, их объемные близки к характеристикам баллонов (табл. 8.2) и даже несколько ниже.
 Существенным недостатком криогенной системы являются потери газа на испарение вследствие неизбежного теплопритока, составляющие в зависимости от конструкции криостата 1—2% общей массы газа в сутки. Поэтому криогенный способ хранения используется в ЭУ, в которых по условиям эксплуатации СХПР могут быть заправлены непосредственно перед началом работы, а длительность непрерывной работы составляет несколько сотен часов, для которых существенную роль играет незначительная масса (например, космических аппаратах), или в мощных ЭУ, часть энергии которых можно затратить на ожижение испаряющихся газов (например, на подводных лодках) .
Существенным недостатком криогенной системы являются потери газа на испарение вследствие неизбежного теплопритока, составляющие в зависимости от конструкции криостата 1—2% общей массы газа в сутки. Поэтому криогенный способ хранения используется в ЭУ, в которых по условиям эксплуатации СХПР могут быть заправлены непосредственно перед началом работы, а длительность непрерывной работы составляет несколько сотен часов, для которых существенную роль играет незначительная масса (например, космических аппаратах), или в мощных ЭУ, часть энергии которых можно затратить на ожижение испаряющихся газов (например, на подводных лодках) .
Более сложные системы представляют собой СХПР с реагентами в химически связанном состоянии, вклю-
Рис. 8.1. Схема криогенного хране-
ния реагентов.
/ — теплоизоляция: 2 — сжиженный газ;
3 — нагреватель; 4 — газовая подушка.
|
Таблица 8.2. Массовые и объемные характеристики криогенного хранения реагентов
|
чающие хранилища исходных соединений, реакторы, в которых реализуется разложение этих соединений на рабочий реагент (например, водород, кислород) и остаточный продукт, а также, при необходимости, агрегаты (узлы) очистки реагента от примесей, образующихся в результате процесса разложения. Такие СХПР применяются в автономных ЭУ, в которых невозможно или нецелесообразно по эксплуатационным условиям использовать СХПР с газообразными или криогенными реагентами.
Водород и кислород в химически связанном состоянии находятся в огромном количестве неорганических и органических соединений. Однако лишь некоторые из них являются источниками чистых газов, выделяющихся при взаимодействии с другими веществами или при относительно небольших затратах энергии.
Исходными веществами являются в основном широко распространенные, достаточно дешевые, пригодные для длительного хранения и транспортировки вещества, которые дают возможность получать чистые, пригодные к использованию в ЭХГ газы наиболее простыми технологическими средствами, не требующими значительных энергозатрат и чрезмерно высоких параметров (температур, давлений).
Исходные соединения могут быть газообразными, жидкими или твердыми.
Процессы получения газов можно подразделить на две группы:
1) происходящие под воздействием тепла и катализатора;
2) требующие взаимодействия с другими веществами при нормальной или повышенной температуре.
К первой группе относятся процессы получения водорода диссоциацией аммиака, получение кислорода 358
разложением хлоратов и перхлоратов щелочных металлов или разложением перекиси водорода.
Ко второй группе относятся процессы конверсии бензина и метанола, гидролиз гидридов металлов, гидролиз надперекисных соединений.

 Опубликовано в
Опубликовано в