Получение кислорода из перекиси водорода
 30 декабря, 2016
30 декабря, 2016  Mihail Maikl
Mihail Maikl Перекись водорода Н202 имеет высокое содержание кислорода <47%). однако обычно используют промышленный продукт с содержанием перекиси 85—95%. Это объясняется высокой стоимостью чистой перекиси водорода и сложностью ее хранения (100%-ная перекись водорода разлагается со взрывом при ПО—150°С).
Использование перекиси водорода в качестве источника кислорода для ЭХГ с технологической точки зрения наиболее заманчиво по сравнению с другими источниками кислорода по следующим соображениям:
1) отсутствие вредных (с точки зрения работы ЭХГ) продуктов реакции;
2) простота подачи жидкого реагента в зону реакции и регулирования скорости выделения кислорода.
Разложение перекиси водорода идет в присутствии катализатора согласно уравнению реакции
Н202+Н20+72024-97,98 кДж/моль.
Наиболее активными катализаторами разложения перекиси являются соединения тяжелых металлов и металлов переходной группы, в присутствии которых реакция идет с огромными объемными скоростями. Вследствие большого тепловыделения скорость разложения возрастает еще больше и достигает 30—60 с-1.
![]()
![]()
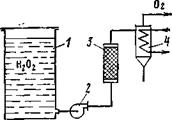 Выход кислорода при гидролизе надперекиси натрия состав - Из резервуара 1 перекись насосом 2 подается в реактор 3, где происходит ее разложение; образовавшаяся парогазовая смесь направляется в холодильник - конденсатор 4, где происходит ее охлаждение и отделение кислорода от влаги. Очищенный кислород направляется в ЭХГ. Как видно, схема достаточно проста, однако некоторые свойства перекиси водорода резко снижают достоинства этого способа хранения кислорода. Как подтверждено многочисленными исследованиями, чистая перекись водорода любой концентрации, находящаяся в совершенно чистом, изготовленном из каталитически неактивного материала сосуде, является весьма устойчивым соединением (например, 90%-ный раствор перекиси водорода при -)-30°С разлагается лишь на 0,5% в год). Однако катализаторами разложения могут быть самые различные соединения, как органические, так и неорганические, причем даже незначительные количества этих веществ заметно катализируют процесс. В связи с этим возникают огромные трудности с хранением и транспортировкой перекиси водорода любой концентрации. Основные требования — это чистота исходного продукта, тары и строгое соблюдение правил транспортировки и хранения. Однако практически невозможно избежать попадания в перекись загрязняющих катализаторов. Для предотвращения разложения, а иногда и взрыва, особенно возможного при температурах выше -|-40оС, в перекись водорода вводят некоторое количество так называемых стабилизаторов — веществ, замедляющих каталитическое разложение. Наиболее широко применяются следующие соединения: станнат натрия №2Сп0з-ЗН20, пирофосфат натрия Na4P207-ЮН20 оксихинолин (оксич). Эти вещества связывают и нейтрализуют действие тех или иных ионов загрязнений. Выбирают стабилизаторы или их смесь исходя из условий применения, хранения, типа вероятных загрязнений и условий разложения.
Выход кислорода при гидролизе надперекиси натрия состав - Из резервуара 1 перекись насосом 2 подается в реактор 3, где происходит ее разложение; образовавшаяся парогазовая смесь направляется в холодильник - конденсатор 4, где происходит ее охлаждение и отделение кислорода от влаги. Очищенный кислород направляется в ЭХГ. Как видно, схема достаточно проста, однако некоторые свойства перекиси водорода резко снижают достоинства этого способа хранения кислорода. Как подтверждено многочисленными исследованиями, чистая перекись водорода любой концентрации, находящаяся в совершенно чистом, изготовленном из каталитически неактивного материала сосуде, является весьма устойчивым соединением (например, 90%-ный раствор перекиси водорода при -)-30°С разлагается лишь на 0,5% в год). Однако катализаторами разложения могут быть самые различные соединения, как органические, так и неорганические, причем даже незначительные количества этих веществ заметно катализируют процесс. В связи с этим возникают огромные трудности с хранением и транспортировкой перекиси водорода любой концентрации. Основные требования — это чистота исходного продукта, тары и строгое соблюдение правил транспортировки и хранения. Однако практически невозможно избежать попадания в перекись загрязняющих катализаторов. Для предотвращения разложения, а иногда и взрыва, особенно возможного при температурах выше -|-40оС, в перекись водорода вводят некоторое количество так называемых стабилизаторов — веществ, замедляющих каталитическое разложение. Наиболее широко применяются следующие соединения: станнат натрия №2Сп0з-ЗН20, пирофосфат натрия Na4P207-ЮН20 оксихинолин (оксич). Эти вещества связывают и нейтрализуют действие тех или иных ионов загрязнений. Выбирают стабилизаторы или их смесь исходя из условий применения, хранения, типа вероятных загрязнений и условий разложения.

 Опубликовано в
Опубликовано в