Исследование работы кислородного электрода
 5 ноября, 2016
5 ноября, 2016  Mihail Maikl
Mihail Maikl Здесь не будет рассматриваться механизм протекания реакции восстановления кислорода на электроде, так как этому явлению посвящена обширная литература, из которой можно отметить обзор А. Демьяновича [6.17]. В то же время нет оснований считать, что на кислородном электроде, находящемся в контакте с ИОМ, процесс протекает особенным образом. Целью является показать подход к исследованию кислородного электрода в ТЭ с ИОМ и представить некоторые экспериментальные данные.
Кислородные электроды в нашем случае аналогичны водородным и представляют собой пористые углерод - фторопластовые подложки толщиной 0,7—1 мм, активированные платиновой чернью (чистой или с фторопластовой суспензией); удельная поверхность Pt, определенная по методу БЭТ, составляет примерно 20 м2/г. Мембранно-электродный блок образуется в результате термического прессования ИОМ и электродов.
Поляризация кислородного электрода i]0 определяется
как разность общей поляризации и поляризаций омической и водородного электрода. Методы определения последних двух поляризаций обсуждались ранее.
В свою очередь поляризацию кислородного электрода представим в виде
4o, = 4n+W (6-5)
Где т]п — поляризация перехода; т|дИф— поляризация диффузии;
-a)TzrltlJ°~ ТІ - а) ПІ' ІП і 7 І' Є3’6)
Обычно уравнение (6.6) записывается в фор|*е так Называемого уравнения Тафеля
![]() ц — а+Ь gJ.
ц — а+Ь gJ.
Это уравнение справедливо при %^kTjnF. Таким образом, если построить поляризацию перехода в координатах г)п; lg/, можно определить а и Ь, входящие в уравнение (6.7). Для большей наглядности удобнее представлять тафелевскую зависимость в координатах U, lg I, где
(6.8)
 |
 |
так как характер зависимости при этом не меняется.
 |
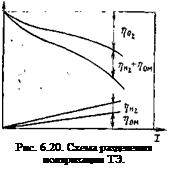
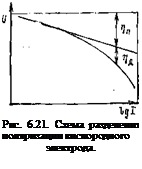
В области, где характеристика ТЭ отклоняется от линейной, имеет место поляризация диффузии; на катоде ТЭ с ИОМ изменение концентрации электролита в приэлектродной области произойти не может. Метод разделения поляризации ТЭ представлен на рис. 6.20, а на рис. 6.21—разделение поляризации кислородного электрода. Так как напряжение на рис. 6.21 скорректи-
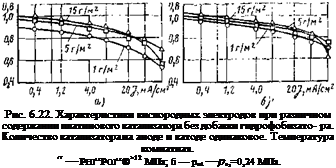
ровано на поляризацию водородного электрода и омическую, то оно фактически представлено по отношению к неполяризуемому водородному электроду в том же растворе. Предполагаем, что во всей области токов механизм реакции не изменяется. На рис. 6.22 представлены характеристики кислородных электродов при различном количестве катализатора без добавки фторопласта. Для всех кривых dU/dl составляет примерно 60 мВ, что соответствует литературным данным для высокодисперсной платины в 1 н. растворе H2SO4. Вид-
|
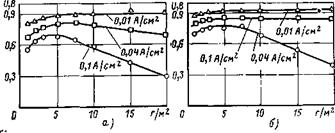
Рис. 6.23. Зависимость напряжения ТЭ (омическая поляризация IR не учитывается) от плотности тока и содержания чистого платинового катализатора. Количество катализатора на аноде и катоде одинаковое. Температура комнатная. а - р.. — — 0,12 МПа; б — р — — 0,24 МПа. Н 2 ‘-'2 U 2 |
но, что при больших содержаниях платинового катализатора в области больших токов происходит наибольшее отклонение от прямой линии вследствие затруднений в доставке кислорода. На рис. 6.23 представлены зависимости напряжения от плотности тока и содержания чистой платиновой черни для двух давлений водорода и кислорода. Из этих зависимостей видно, что для обеспечения больших плотностей тока необходимо снижение диффузионной поляризации, которое обеспечивается гидрофобизацией катализатора.
Как уже было отмечено ранее, введение фторопласта в катализатор осуществляется добавкой соответствующего количества фторопластовой суспензии в смесь, фильтруемую сквозь подложку. На рис. 6.24 представлена зависимость напряжения на ТЭ при различных плотностях тока от содержания фторопласта, определенного по соотношению рфт = ОфТ/Л4рг при М? t = 3 г/м2. Как и следовало ожидать, для малых количеств катали-
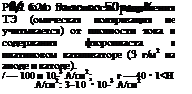 |
 |
затора эта зависимость чрезвычайно слабо выражена в отличие от больших (20 г/м2) количеств черни
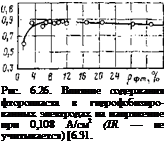
(рис. 6.25). Таким образом, примерно 20% фторопласта в катализаторе являются оптимальными; дальнейшее повышение содержания фторопласта не приводит к сколько-нибудь заметному изменению характеристик ТЭ, однако процесс равномерного нанесения гидрофобизи - рованного катализатора на подложку в этом случае становится более затруднительным. Аналогичная зависимость (рис. 6.26) представлена также и в работе [6.3], правда, без указания содержания количества платиновой черни.
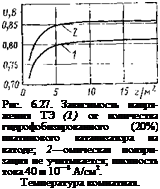
На рис. 6.27 представлены результаты исследования зависимости напряжения ТЭ от количества гидрофоби - зированного катализатора на катоде при 20%-ном содержании фторопласта. Видно, что повышение количества платиновой черни свыше 10—15 г/м2 не приводит к улучшению электрических характеристик. ,
Из представленных экспериментальных данных видно, что при больших плотностях тока поляризация диффузии вызывает значительное снижение электрических характеристик ТЭ. Введение фторопласта в катализатор снижает эту поляризацию, однако полностью устранить ее таким образом невозможно вследствие того, что генерация тока происходит на чистой платине, как находящейся в контакте с поверхностью ИОМ, так и внедренной в ее объем вблизи границы раздела ИОМ —
ЗИ
 |
 |
электрод. Ясно, что в этих случаях доступ кислорода в зону электрохимической реакции ограничен либо пленкой воды, либо слоем ИОМ. Эффективным способом снижения поляризации диффузии в ТЭ с ИОМ является повышение давления кислорода, так как в этом случае требования к поддержанию перепада давления газ— электролит (ТЭ с жидким электролитом) или газ — газ (элементы с матричным электролитом) отсутствуют. Бы-
ла произведена оценка влияния давления и температуры на диффузионный ток и показано, что каждой температуре процесса соответствует давление, ниже которого диффузионная поляризация становится неоптимальной.
Для определения толщины пленки воды (или любого другого диффузионного сопротивления, приведенного к воде) конкретного элемента (на 1 см2 геометрической поверхности) воспользуемся системой уравнений, описывающих протекание процессов на катоде ТЭ 16.18]:
![]() RT
RT
(1-а) п?
житель; А — стехиометрический коэффициент кислорода; Со — концентрация кислорода на поверхности воды; D — коэффициент диффузии.

![]()
![]()
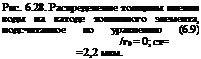 При составлении системы уравнений предполагалось, что закон распределения толщины пленки соответствует Кривой Гаусса.
При составлении системы уравнений предполагалось, что закон распределения толщины пленки соответствует Кривой Гаусса.
На рис. 6.28 представлена функция распределения толщины пленки воды (расчет проводился на ЭВМ), отвечающая реальной характеристике ТЭ во всем исследуемом диапазоне токов.
Рассмотренные в настоящем параграфе методы исследования ТЭ с ИОМ позволяют произвести анализ их характеристик без введения специальных измерительных устройств или изменения конструкции, что особенно важно при разработке батарей ТЭ различного назначения.

 Опубликовано в
Опубликовано в